Oxohalide - Oxohalide
Moleküler Oksohalojenürleri ( oksihalojenürleri ) bir grup kimyasal bileşiklerin her ikisi de burada oksijen ve halojen atomları, birbirine bağlı kimyasal element tek bir A içinde molekülü . AO m X n , X = F , Cl , Br , I genel formülüne sahiptirler . A elemanı, bir ana grup elemanı, bir geçiş elemanı veya bir aktinit olabilir . Oksohalid veya oksihalid terimi, aynı genel kimyasal formüle sahip, ancak iyonik bir yapıya sahip mineralleri ve diğer kristalli maddeleri de belirtebilir .
Sentez
Oksohalidler, oksitler ve halojenürler arasındaki ara bileşikler olarak görülebilir . Üç genel sentez yöntemi vardır:
- Bir halojenürün kısmi oksidasyonu: 2 PCl 3 + O 2 → 2 POCl 3 . Bu örnekte, oksidasyon durumu iki artar ve elektrik yükü değişmez.
- Bir oksidin kısmi halojenlenmesi: 2 V 2 O 5 + 6 Cl 2 + 3 C → 4 VOCl 3 + 3 CO 2
- Oksit ikamesi: [CrO 4 ] 2− + 2 Cl - + 4 H + → CrO 2 Cl 2 + 4 H 2 O
Ek olarak, halojen değişim reaksiyonları ile çeşitli okzohalidler yapılabilir ve bu reaksiyon, POFCl 2 ve CrO 2 FCl gibi karışık okzohalidlerin oluşumuna da yol açabilir .
Özellikleri
Oksit veya halojenür ile ilgili olarak, bir A elementinin belirli bir oksidasyon durumu için, iki halojen atomu bir oksijen atomunun yerini alırsa veya tam tersi , molekül üzerindeki toplam yük değişmez ve merkezi atomun koordinasyon numarası bir azalır. . Örneğin, hem fosfor oksiklorür , POCl 3 hem de fosfor pentaklorür , PCl 5 , +5 oksidasyon durumunda nötr kovalent fosfor bileşikleridir . Bir oksijen atomu basitçe bir halojen atomu ile değiştirilirse, yük +1 artar, ancak koordinasyon numarası değişmez. Bu, bir kromat veya dikromat tuzu ve potasyum klorür karışımının konsantre sülfürik asit ile reaksiyonu ile gösterilir .
- [Cr 2 O 7 ] 2− + 4 Cl - + 6 H + → 2 CrO 2 Cl 2 + 3 H 2 O
Üretilen kromil klorürün elektrik yükü yoktur ve reaksiyon karışımından damıtılabilen uçucu bir kovalent moleküldür.
Yüksek oksidasyon durumlarındaki elementlerin oksohalidleri , karşılık gelen oksit veya halide benzer oksitleme gücüne sahip güçlü oksitleyici maddelerdir . Oksohalitlerin çoğu kolaylıkla hidrolize edilir . Örneğin, kromil klorür, yukarıdaki sentetik reaksiyonun tersi yönde kromata hidrolize edilir. Bu reaksiyonun itici gücü, A-Cl bağlarından daha güçlü olan AO bağlarının oluşmasıdır. Bu , reaksiyon için Gibbs serbest enerji değişimine olumlu bir entalpi katkısı sağlar.
Pek çok okzohalid Lewis asidi olarak hareket edebilir . Bu özellikle , bir Lewis bazından bir veya daha fazla elektron çifti kabul edildiğinde 5 veya 6 koordinatına dönüşen koordinasyon numarası 3 veya 4 olan oksohalitlerde böyledir . Gibi Oxohalide anyonlar [VOC 4 ] 2- oxohalide asit-baz kompleksleri (VOC olarak görülebilir 2 Lewis bazları olarak hareket eden daha fazla halojenür iyonları ile). Diğer bir örnek, VOC olduğu 2 oluşturan köşeli bipyramidal kompleks VOC 2 (N (CH 3 ) 3 ) 2 , baz trimetilamin .
Titreşim spektrumları birçok Oksohalojenürleri detayında atanmıştır. Bağıl bağ güçleri hakkında yararlı bilgiler verirler. Örneğin, CrO içinde 2 F 2 , CrO germe titreşim 1006 cm olan -1 ve 1016 cm -1 ve Cr-F germe titreşim 727 cm olan -1 ve 789 cm -1 . Fark, O ve F atomlarının farklı kütlelerinden kaynaklanamayacak kadar büyüktür. Aksine, Cr – O bağının Cr – F bağından çok daha güçlü olduğunu gösterir. M – O bağları genellikle çift bağ olarak kabul edilir ve bu M – O bağ uzunluklarının ölçümleriyle desteklenir. A ve O elementlerinin kimyasal olarak bir σ bağı ve bir π bağı ile birbirine bağlandığını ima eder .
Yüksek oksidasyon durumlarındaki elementlerin oksohalidleri, liganddan metale yük transferi (LMCT) geçişleri sayesinde yoğun şekilde renklendirilir .
Ana grup elemanları
-
Karbon grubu : Karbon , karbon monoksitin klor ile karbonla katalize edilmiş reaksiyonu ile endüstriyel olarak üretilen oksohalidler COX 2 , X = F , Br ve çok toksik fosgen (X = Cl) oluşturur . Organik kimyada karbonil bileşiklerinin oluşumu için yararlı bir reaktiftir . Örneğin,
- COCl 2 + 2 ROH → CO (OR) 2 + 2 HCl
- Pnictojenler : Azot , oksidasyon durumları 3, NOX, X = F , Cl , Br ve 5, NO 2 X, X = F , Cl'de nitrojen ile iki dizi oksohalit oluşturur . Azot oksitlerin halojenlenmesiyle yapılırlar. NO 2 F'nin nitrat iyonu NO 3 - ile izoelektronik olduğuna dikkat edin . Sadece fosforun (V) oksohalitleri bilinmektedir.
-
Kalkojenler : Kükürt gibi oksidasyon grubu +4 form Oksohalojenürleri, tionil klorür , SOClz 2 gibi ve oksidasyon durumunda + 6, sülfüril florür , SO 2 F 2 , sülfüril klorür , SO 2 Cl 2 ve tionil tetraflorür , SOF 4 . Hepsi kolayca hidrolize edilir. Gerçekte, su molekülleri gaz halindeki ürünlere dönüştürüldüğünden tiyonil klorür bir dehidrasyon ajanı olarak kullanılabilir ve geride susuz katı klorür bırakır.
- MgCl 2 · 6H 2 O + 6 SOCl 2 → MgCl 2 + 6 SO 2 + 12 HCl
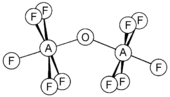
Selenyum ve tellür benzer bileşikler ve ayrıca okso-köprülü türler F 5 AOAF 5 (A = S, Se, Te) oluşturur. S, Se ve Te için sırasıyla 142.5, 142.4 ve 145.5 ° AOA açısı ile doğrusal değildirler. Tellür anyon [TeOF 5 ] - olarak bilinen teflate büyük katyonlar ile Stabil tuz oluşturma için faydalı olan bir büyük ve oldukça stabil bir anyon olduğu.
- Halojenler : Halojenler , X = Cl, Br ve I ile XO 2 F , XO 3 F ve XOF 3 formülleriyle çeşitli oksoflorürler oluşturur . IO 2 F 3 ve IOF 5 de bilinmektedir.
- Asil gazlar : XeOF 4
Geçiş metalleri ve aktinitler
Aşağıda geçiş metallerinin bilinen oksoalitlerinin bir seçimi gösterilmektedir ve literatürde daha ayrıntılı listeler mevcuttur. X, çeşitli halojenürleri, çoğunlukla F ve Cl'yi gösterir.
| Paslanma durumu | Oxohalides |
|---|---|
| 3 | VOCl, VOBr, FeOCl |
| 4 | [TiOCl 4 ] 2− , Cl 3 TiOTiCl 3 , VOCl 2 , [VOCl 4 ] 2− |
| 5 | VOX 3 , VO 2 X, [CrOF 4 ] - , [CrOF 5 ] 2− , MnOCl 3 , TcOCl 3 , VOF 3 , VOCl 3 , NbOCl 3 |
| 6 | CrO 2 CI 2 , [CrO 3 CI] - , REOX 4 , Reo 2 F 2 , OsOF 4 , CrO 2 F 2 , MoOCl 4 MoO 2 Cı 2 , WO 2 Cl 2 , DCP 4 |
| 7 | MnO 3 Cl, ReOF 5 , Reo 2 F 3 , Reo 3 Cl, OsOF 5 |
| 8 | OsO 2 F 4 , OsO 3 F 2 |
Metalin yüksek oksidasyon durumları, oksijenin flor gibi güçlü bir oksitleyici ajan olması gerçeğiyle belirlenir . Brom ve iyot nispeten zayıf oksitleyici maddelerdir, bu nedenle daha az oksobromit ve oksiyodit bilinmektedir. D ile bileşikler için yapılar 0 konfigürasyon ile tahmin edilir Vsepr teori . Bu nedenle, CrO 2 Cı 2 olan dört yüzlü , OsO 3 F 2 olan köşeli bipyramidal , XeOF 4 olan kare piramit ve OsOF 5 olan oktahedral . D 1 kompleks ReOCl 4 kare piramit şeklindedir.
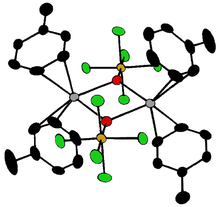
Bileşikler [Ta 2 OX 10 ] 2- ve [M 2 OCl 10 ] 4- (M = W, Ru, Os), iki MX sahip 5 , bir köprü oluşturan oksijen atomu ile birleştirilmiş grupları. Her metal bir oktahedral ortama sahiptir. Olağandışı doğrusal M-O-M yapısı, moleküler orbital teorisi açısından rasyonelleştirilebilir , bu da metal ve oksijen atomları arasında d π - p π bağının varlığını gösterir . Oksijen köprüleri, M (cp) 2 (OTeF 5 ) 2 (M = Ti, Zr, Hf, Mo veya W; cp = η 5 −C 5 H 5 ) veya [AgOTeF 5 - (C 6 ) gibi daha karmaşık konfigürasyonlarda mevcuttur. 'H 5 CH 3 ) 2 ] 2 .
Gelen aktinid serisi, uranil gibi bileşikler UO 2 Cl 2 ve [UO 2 Cl 4 ] 2- , iyi bilinen ve UO doğrusal içerirler 2 kısmı. Neptunyum ve plütonyum için benzer türler mevcuttur .
Mineraller ve iyonik bileşikler
Bizmut okzoklorür (BiOCl, bismoclite ), mineral oksoalidin nadir bir örneğidir. Kristal yapı , bir sahiptir dörtgen simetri ve Cl oluşan katman olarak düşünülebilir - , Bi 3+ ve O 2 amacıyla Cı-Bi-O-Bi-Cı-Cı-Bi-O-Bi iyonları, Cl. Bu katmanlı, grafit benzeri yapı, nispeten düşük sertlikte bismoklit ( Mohs 2–2.5) ve diğer pek çok okzohalid minerali ile sonuçlanır. Bu diğer mineraller , cıva içeren minerallerin ayrışmasıyla oluşan terlinguaite Hg 2 OCl'yi içerir . Birkaç aşamada orijinal bir kurşun sülfit birikintisinden oluşan Mendipit , Pb 3 O 2 Cl 2 , ikincil bir oksoalid mineralinin başka bir örneğidir.
Demir , antimon , bizmut ve lantan elementleri , MOCl genel formülünün okzoklorürlerini oluşturur. MOBr ve MOI, Sb ve Bi için de bilinir. Kristal yapılarının çoğu belirlendi.
Ayrıca bakınız
Referanslar
Kaynakça
- Greenwood, Norman N .; Earnshaw, Alan (1997). Elementlerin Kimyası (2. baskı). Butterworth-Heinemann . ISBN 978-0-08-037941-8 .
- Housecroft, CE ve Sharpe, AG Inorganic Chemistry , 2. baskı, Pearson Prentice-Hall 2005. ISBN 0-582-31080-6
- Shrivr, DF and Atkins, PW Inorganic Chemistry , 3rd edn. Oxford University Press, 1999. ISBN 0-19-850330-X
- Wells, AF (1962). Yapısal İnorganik Kimya (3. baskı). Oxford: Clarendon Press. s. 384–392. ISBN 0-19-855125-8 . .