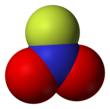
nitril florür - Nitryl fluoride
|
|
|||
| tanımlayıcılar | |||
|---|---|---|---|
|
3B model ( JSmol )
|
|||
| Kimyasal Örümcek | |||
| ECHA Bilgi Kartı |
100.030.007 |
||
| AT Numarası | |||
|
PubChem Müşteri Kimliği
|
|||
| ÜNİİ | |||
|
CompTox Panosu ( EPA )
|
|||
|
|||
|
|||
| Özellikleri | |||
| N O 2 F | |||
| Molar kütle | 65.0039 g/mol | ||
| Erime noktası | −166 °C (−267 °F; 107 K) | ||
| Kaynama noktası | −72 °C (−98 °F; 201 K) | ||
| Bağıntılı bileşikler | |||
|
Diğer anyonlar
|
nitril klorür , nitril bromür | ||
|
Diğer katyonlar
|
nitrosil florür , sülfüril florür | ||
|
Aksi belirtilmediği sürece, veriler standart durumdaki malzemeler için verilmiştir (25 °C [77 °F], 100 kPa'da). |
|||
|
|
|||
| Bilgi kutusu referansları | |||
Nitril florür , NO 2 F, renksiz bir gazdır ve florlama maddesi olarak kullanılan güçlü oksitleyici bir maddedir ve roket iticilerinde bir oksitleyici olarak önerilmiştir (asla uçulmamıştır).
Düşük kaynama noktası ile tutarlı, iyonik olmayan moleküler bir türdür . Yapı, 135 pm'lik kısa bir NF bağ uzunluğuna sahip düzlemsel nitrojene sahiptir .
Hazırlık
Henri Moissan ve Paul Lebeau 1905 yılında nitril fluorür kaydedilmiş hazırlanması florlaştırma bir nitrojen dioksit . Bu reaksiyon yüksek derecede ekzotermiktir ve bu da kontamine ürünlere yol açar. En basit yöntem flor gazını önler ancak kobalt(III) florür kullanır :
- NO 2 + CoF 3 → NO 2 F + CoF 2
CoF 2 , CoF 3 olarak yeniden oluşturulabilir . Diğer yöntemler tarif edilmiştir.
termodinamik özellikler
Bu gazın termodinamik özellikleri IR ve Raman spektroskopisi ile belirlendi. FNO 2'nin standart oluşum ısısı -19 ± 2 kcal/mol.3'tür.
- BSE arasında tek moleküllü ayrışma denge 2 500 Kelvin büyüklük en az altı siparişler, 1000 Kelvin iki büyüklük ile reaktiflerin tarafında yer almaktadır.
- Homojen termal bozunma, 1200 kelvin'in altındaki sıcaklıklarda incelenemez.
- Denge, artan sıcaklıkla reaktanlara doğru kayar.
- Nitril florürdeki NF bağının 46.0 kcal'lik ayrışma enerjisi, normal NF tekli bağ enerjisinden yaklaşık 18 kcal daha azdır. Bu NO “yeniden düzenlenmesi enerji” atfedilebilir 2 radikali; olduğu NO 2 BSE radikal 2 kuru NO daha az kararlıdır 2 molekülü. Kalitatif olarak, konuşma, NF bağ “tükenmiş” tek elektron serbest NO bir rezonans üç elektron bağ oluşturur 2 Böylece kcal 18 bir kazanç molekülü stabilize.
Reaksiyonlar
Nitril florür, organik nitro bileşikleri ve nitrat esterleri hazırlamak için kullanılabilir .