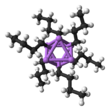
n -Bütillityum - n-Butyllithium
|
|||
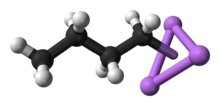 Butil ve lityum arasındaki delokalize bağların yakından görünümü
|
|||
| İsimler | |||
|---|---|---|---|
|
IUPAC adı
butillityum, tetra- μ 3 -bütil-tetrallityum
|
|||
| Diğer isimler
NBL, BuLi,
1-litiyobütan |
|||
| tanımlayıcılar | |||
|
3B model ( JSmol )
|
|||
| chebi | |||
| Kimyasal Örümcek | |||
| ECHA Bilgi Kartı |
100.003.363 |
||
|
PubChem Müşteri Kimliği
|
|||
| ÜNİİ | |||
|
CompTox Panosu ( EPA )
|
|||
|
|||
|
|||
| Özellikler | |||
| Cı- 4 , H 9 Li | |||
| Molar kütle | 64.06 g·mol -1 | ||
| Dış görünüş | genellikle çözelti olarak
elde edilen kararsız renksiz sıvı |
||
| Yoğunluk | 0.68 g / cm ' 3 , çözücü tanımlanmış | ||
| Erime noktası | −76 °C (−105 °F; 197 K) (<273 K) | ||
| Kaynama noktası | ayrışır | ||
| Reaksiyon | |||
| çözünürlük | Dietil eter , sikloheksan | ||
| Asit (s K a ) | 50 | ||
| Yapı | |||
| çözelti içinde tetramerik | |||
| 0 D | |||
| Tehlikeler | |||
| Ana tehlikeler | piroforik (havada kendiliğinden yanar), aşındırıcı LiOH'ye ayrışır |
||
| NFPA 704 (ateş elmas) | |||
| Bağıntılı bileşikler | |||
|
İlgili organolityum
reaktifleri |
sek -butillityum ters -butillityum hegzillityum metillityum |
||
|
Bağıntılı bileşikler
|
lityum hidroksit | ||
|
Aksi belirtilmedikçe, veriler standart durumdaki malzemeler için verilmiştir (25 °C [77 °F], 100 kPa'da). |
|||
|
|
|||
| Bilgi kutusu referansları | |||
n -Bütillityum Cı 4 H 9 (kısaltması Li , n -BuLi ) bir bir organolityum reaktifi . Polibütadien veya stiren-bütadien-stiren (SBS) gibi elastomerlerin üretimindebir polimerizasyon başlatıcısıolarak yaygın olarak kullanılır. Ayrıca,farmasötik endüstrisinde olduğu gibi organik bileşiklerin sentezinde güçlü bir baz ( süper baz )olarak geniş çapta kullanılır.
Butillityum, pentan , heksanlar ve heptanlar gibi alkanlarda çözeltiler (%15, %25, 1.5 M , 2 M, 2.5 M, 10 M, vb.) olarak ticari olarak mevcuttur . Dietil eter ve THF içindeki çözeltiler hazırlanabilir, ancak depolama için yeterince kararlı değildir. Butillityum ve diğer organolityum bileşiklerinin dünya çapında yıllık üretim ve tüketiminin 2000 ila 3000 ton arasında olduğu tahmin edilmektedir.
Butillityum renksiz olmasına rağmen, n -butillityum alkanlarda genellikle soluk sarı bir çözelti olarak bulunur. Bu tür çözümler, uygun şekilde depolanırsa süresiz olarak stabildir, ancak pratikte eskime üzerine bozulurlar. İnce beyaz çökelti ( lityum hidroksit ) çökelir ve renk turuncuya döner.
Yapı ve yapıştırma
n -BuLi hem katı halde hem de çözeltide bir küme olarak bulunur. Toplanma eğilimi organolityum bileşikleri için yaygındır. Agregalar, lityum ve butil zincirinin terminal karbonu arasındaki lokalize kovalent bağlarla bir arada tutulur. n- BuLi durumunda , kümeler tetramerik (eter içinde) veya heksameriktir ( sikloheksan içinde ). Küme çarpıtılmış olan küban-tipi küme Li ile C , H 2 alternatif köşe Ar grupları. Li olarak eşdeğer bir açıklama tetramer tarif 4 yüzlü bir tetrahedron [ile içiçe Cı , H 2 R] 4 . Küme içindeki bağlanma, diboran'ı tanımlamak için kullanılanla ilişkilidir, ancak sekiz atom söz konusu olduğundan daha karmaşıktır. Elektron eksikliği olan karakterini yansıtan n -butillityum, Lewis bazlarına karşı oldukça reaktiftir .
Nedeniyle arasındaki büyük fark elektronegatiflik arasında karbon ( 2.55 ) ve lityum ( 0.98 ), Cı-Li bağı yüksek polarize edilir. Yük ayrımının %55-95 olduğu tahmin edilmektedir. Pratik amaçlar için, n -BuLi, genellikle bütil olarak tepkimeye kabul edilebilir anyon , n -Bu - , ve bir lityum katyonu , Li + .
Hazırlık
n -BuLi için standart preparasyon , 1-bromobütan veya 1-klorobütanın Li metali ile reaksiyonudur :
- 2 Li + C 4 H 9 X → C 4 H 9 Li + LiX (X = Cl, Br)
Bu reaksiyon için kullanılan lityum %1-3 sodyum içeriyorsa , reaksiyon, saf lityum kullanılmasından daha hızlı ilerler. Bu preparasyon için kullanılan çözücüler arasında benzen , sikloheksan ve dietil eter bulunur. BuBr öncü olduğunda, ürün, az miktarda oktan ile birlikte hem LiBr hem BuLi içeren karışık bir kümeden oluşan homojen bir çözeltidir . BuLi, LiCl ile daha zayıf bir kompleks oluşturur, böylece BuCl'nin Li ile reaksiyonu bir LiCl çökeltisi üretir .
Hava ile bozunmaya duyarlı olan butillityum çözeltileri titrasyon ile standardize edilir . Popüler bir zayıf asit, son noktada koyu renkli bir dilityo türevi veren bifenil -4-metanoldür.
Uygulamalar
Butillityum, esas olarak anyonik bir başlatıcı olarak değerlendirilir polimerizasyon bölgesinin dienler gibi, bütadien . Reaksiyona "karbolitasyon" denir:
- C 4 H 9 Li + CH 2 =CH−CH=CH 2 → C 4 H 9 −CH 2 −CH=CH−CH 2 Li
İzopren bu şekilde stereospesifik olarak polimerize edilebilir. Stiren-bütadien polimerlerinin üretimi için butillityum kullanımı da ticari öneme sahiptir . Etilen bile BuLi'ye eklenecektir.
Reaksiyonlar
Butillityum (s güçlü bir baz olan K bir ≈ 50), fakat aynı zamanda güçlü bir nükleofil ve indirgeyici diğer reaktanlara bağlı olarak,. Ayrıca, güçlü bir nükleofil olmasının yanı sıra, n- BuLi , lityum merkezlerine bağlanarak kümeleri kısmen ayrıştıran eterler ve üçüncül aminler gibi aprotik Lewis bazlarına bağlanır . Güçlü bir baz olarak kullanımına metalleşme denir . Reaksiyonlar tipik olarak ortaya çıkan organolityum türevleri için iyi çözücüler olan tetrahidrofuran ve dietil eter içinde gerçekleştirilir (aşağıya bakınız).
metalasyon
n- BuLi'nin en kullanışlı kimyasal özelliklerinden biri , çok çeşitli zayıf Brønsted asitlerini deprotone etme yeteneğidir . t -Butillityum ve s -bütillityum daha temeldir. n- BuLi, özellikle konjugat bazının elektron delokalizasyonu veya bir veya daha fazla heteroatom (karbon olmayan atomlar) ile stabilize olduğu durumlarda birçok CH bağını protonsuzlaştırabilir (yani metalatlayabilir ). Örnekler asetilenler (içerir lH -CC-R), metil sülfitler ( lH -CH 2 , SR), tiyoasetaller ( lH -CH (SR), 2 , örneğin, ditian ), methylphosphines ( lH -CH 2 PR 2 ), furan , tiyofenler ve ferrosen (Fe ( H -C 5 H 4 ) (Cı- 5 , H 5 )). Bunlara ek olarak , sırasıyla alkoksitler, amidler, enolatlar ve diğer lityum tuzlarını üretmek için alkoller, aminler, enolize edilebilir karbonil bileşikleri ve herhangi bir açık asidik bileşik gibi tüm daha asidik bileşikleri deprotone edecektir . Stabilitesi ve oynaklık ve bütan gibi kaynaklanan proton giderme reaksiyonları uygundur, ancak aynı zamanda, çünkü üretilen bir yanıcı gaz hacminin büyük ölçekli reaksiyonlar için bir sorun olabilir.
- LiC 4 H 9 + RH → C 4 H 10 + RLi
n- BuLi'nin kinetik bazlığı çözücü veya yardımcı çözücüden etkilenir. Tetrahidrofuran (THF), tetrametiletilendiamin (TMEDA), heksametilfosforamid (HMPA) ve 1,4-diazabisiklo[2.2.2]oktan ( DABCO ) gibi Li + kompleksi oluşturan ligandlar , Li-C bağını daha da polarize eder ve metalasyonu hızlandırır. Bu tür katkı maddeleri, ünlü bir örneği dilithioferrosen olan lityumlu ürünün izolasyonuna da yardımcı olabilir.
- Fe(C 5 H 5 ) 2 + 2 LiC 4 H 9 + 2 TMEDA → 2 C 4 H 10 + Fe(C 5 H 4 Li) 2 (TMEDA) 2
Schlosser bazı , butillityumun potasyum t -butoksit ile işlenmesiyle üretilen bir süper bazdır . Kinetik olarak butillityumdan daha reaktiftir ve genellikle zor metalasyonları gerçekleştirmek için kullanılır . Butoksit anyonu lityum ile kompleks oluşturur ve ilgili lityum reaktifinden daha reaktif olan butilpotasyum üretir.
Bir baz olarak n -bütillityum kullanımına bir örnek, bir metil karbamat oluşturmak için metil karbonata bir aminin eklenmesidir; burada n -bütillityum, aminin protonunu gidermeye hizmet eder:
- n -BuLi + R 2 NH + (MeO) 2 CO → R 2 NCO 2 Me + LiOMe + BuH
Halojen-lityum değişimi
Butillityum, karşılık gelen organolityum türevini oluşturmak için bir değişim reaksiyonunda bazı organik bromürler ve iyodürlerle reaksiyona girer. Reaksiyon genellikle organik klorürler ve florürlerle başarısız olur:
- C 4 H 9 Li + RX → C 4 H 9 X + RLi (X = Br, I)
Bu lityum-halojen değişim reaksiyonu, çeşitli RLi bileşiklerinin, özellikle aril lityum ve bazı vinil lityum reaktiflerinin hazırlanması için kullanışlıdır . Bu yöntemin faydası, önemli ölçüde tepkime karışımı içinde mevcudiyeti ile, ancak, sınırlı n -BuBr veya N RLi ile reaksiyona girebilen -BuI, oluşan reaktif ve yarışarak dehidrohalojenasyon ki burada, reaksiyonlar , n -BuLi a olarak hizmet temel:
- 2 C 4 H 9 Br + RLi → 2 C 4 H 9 R + LiBr
- 2 C 4 H 9 Li + R'CH=CHBr → 2 C 4 H 10 + R'C≡CLi + LiBr
İyot-lityum değişimi brom-lityum değişiminden birkaç kat daha hızlı olduğundan, bu yan reaksiyonlar RI için RBr'den önemli ölçüde daha az önemlidir. Bu nedenlerle, aril, vinil ve primer alkil iyodürler için tercih edilen alt tabakalar, ve t -BuLi yerine n -BuLi, çoğunlukla oluşan beri kullanılmaktadır t -BuI hemen yok edilir t bir dehidrohalojenasyon reaksiyonunda-BuLi (böylece gerektiren t -BuLi'nin iki eşdeğeri ). Alternatif olarak, vinil lityum reaktifleri, vinil halojenürün (örn. sikloheksenil klorür) lityum ile doğrudan reaksiyonu veya kalay-lityum değişimi ile üretilebilir (bir sonraki bölüme bakın).
Transmetalasyonlar
İlgili bir reaksiyon ailesi, iki organometalik bileşiğin metallerini değiştirdiği transmetalasyonlardır . Bu tür reaksiyonların birçok örneği, kalay ile lityum değişimini içerir :
- C 4 H 9 Li + Me 3 SnAr → C 4 H 9 SnMe 3 + LiAr (burada Ar, aril ve Me metildir)
Ürün kalay bileşikleri (Cı olmasıyla kalay lityum değişim reaksiyonları, organolityum reaktif maddelerinin elde edilmesinde halojen lityum değişimi üzerinde önemli bir avantaja sahiptir 4 H 9 SnMe 3 Yukarıdaki örnekte) daha az reaktif lityum reaktifler için olan olduğundan daha karşılık gelen halojen lityum değişim halojenür ürünleri (Cı- 4 H 9 Br ya da Cı- 4 , H 9 CI). Bu tür değişim reaksiyonlarına giren diğer metaller ve metaloidler cıva , selenyum ve tellürün organik bileşikleridir .
karbonil ilaveleri
n- BuLi dahil olmak üzere organolityum reaktifleri, spesifik aldehitlerin ve ketonların sentezinde kullanılır . Böyle bir sentetik yol, bir organolityum reaktifinin iki ikameli amidlerle reaksiyonudur :
- R 1 Li + R 2 CONMe 2 → LiNMe 2 + R 2 C(O)R 1
THF'nin Bozulması
THF, özellikle TMEDA varlığında, oksijene bitişik dört protondan birinin kaybıyla butillityum tarafından deprotone edilir . Bütan üretmek için bütillityum tüketen bu işlem, asetaldehit ve etilen enolatı vermek için bir halka açıklığını indükler . Bu nedenle, BuLi'nin THF içindeki reaksiyonları , kuru buz ve asetondan oluşan bir dondurma banyosu tarafından uygun şekilde üretildiği gibi, tipik olarak -78 °C gibi düşük sıcaklıklarda gerçekleştirilir . Daha yüksek sıcaklıklar da (−25 °C veya hatta −15 °C) kullanılır.
termal ayrışma
Isıtıldığında, "β-hidrojenler" içeren diğer alkillityum reaktiflerine benzer şekilde n- BuLi, 1-büten ve lityum hidrit (LiH) üretmek için β-hidrit eliminasyonuna uğrar :
- C 4 H 9 Li → LiH + CH 3 CH 2 CH=CH 2
Emniyet
Alkil-lityum bileşikleri, aktivite kaybını önlemek ve güvenlik nedenleriyle inert gaz altında depolanır. n -BuLi su ile şiddetli reaksiyona girer:
- C 4 H 9 Li + H 2 O → C 4 H 10 + LiOH
Bu ekzergonik ve ekzotermik bir reaksiyondur. Oksijen varsa, üretilen bütan tutuşacaktır.
BuLi CO ile reaksiyona girer 2 lityum pentanoat elde edilmiştir:
- C 4 H 9 Li + CO 2 → C 4 H 9 CO 2 Li
Ayrıca bakınız
- Propynillithium , organometalik bir bileşik.
Referanslar
daha fazla okuma
- FMC Lityum üreticisinin ürün sayfaları
- Çevre Kimyası dizini
- Weissenbacher, Anderson, Ishikawa, Organometaliks , Temmuz 1998, p681.7002, Chemicals Economics Handbook SRI International
- FMC Lithium tarafından EPA'ya sunulan HPV test planı
- Ovaska, TV e-EROS Organik Sentez için Reaktifler Ansiklopedisi " n -Butillityum." Wiley ve oğulları. 2006. doi : 10.1002/047084289X.rb395
- Greenwood, NN; Earnshaw, A. Elementlerin Kimyası , 2. baskı. 1997: Butterworth-Heinemann, Boston.