tert -Bütillityum - tert-Butyllithium

|
|
|
|
|
|
| İsimler | |
|---|---|
|
Tercih edilen IUPAC adı
tert -bütillityum |
|
| tanımlayıcılar | |
|
3B model ( JSmol )
|
|
| 3587204 | |
| Kimyasal Örümcek | |
| ECHA Bilgi Kartı |
100.008.939 |
| AT Numarası | |
|
PubChem Müşteri Kimliği
|
|
| BM numarası | 3394 |
|
CompTox Panosu ( EPA )
|
|
|
|
|
|
| Özellikler | |
|
LiC 4H 9 |
|
| Molar kütle | 64.055 g mol -1 |
| Dış görünüş | renksiz katı |
| Yoğunluk | 660 mg cm- 3 |
| Kaynama noktası | 36 - 40 °C (97 - 104 °F; 309 - 313 K) |
| tepki verir | |
| Asit (s K a ) | 45-53 |
| Tehlikeler | |
| GHS piktogramları |
    
|
| GHS Sinyal kelimesi | Tehlike |
| H225 , H250 , H260 , H300 , H304 , H310 , H314 , H330 , H336 , H411 | |
| P210 , P222 , P223 , P231 + 232 , P370 + 378 , P422 | |
| NFPA 704 (ateş elmas) | |
| Alevlenme noktası | -6,6 °C (20,1 °F; 266.5 K) |
| Bağıntılı bileşikler | |
|
Bağıntılı bileşikler
|
n -bütillityum |
|
Aksi belirtilmedikçe, veriler standart durumdaki malzemeler için verilmiştir (25 °C [77 °F], 100 kPa'da). |
|
|
|
|
| Bilgi kutusu referansları | |
tert- Butillityum a, kimyasal bileşik ile , formül (CH 3 ) 3 cli. Bir organolityum bileşiği olarak , benzen de dahil olmak üzere birçok karbon molekülünü deprotone edebilengüçlü bir baz olduğu için organik sentezde uygulamaları vardır. tert- Butillityum, ticari olarak hidrokarbon çözeltileri olarak mevcuttur; genellikle laboratuvarda hazırlanmaz. Sentezi ilkolarak 1941'de RB Woodward tarafından rapor edildi.
Yapı ve yapıştırma
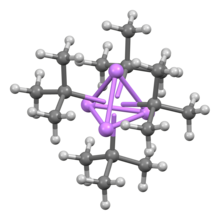
Diğer organolityum bileşikleri gibi, tert -butillityum da bir kümedir. n -butillityum hem heksamer hem de tetramer olarak bulunurken , tert- Butillityum kübik yapılı tetramer olarak bulunur . Organolityum kümelerinde bağlanma, sigma delokalizasyonunu ve önemli Li-Li bağını içerir.
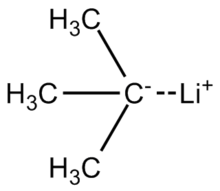
Tert -bütillityumdaki lityum-karbon bağı yüksek oranda polarizedir ve yaklaşık yüzde 40 iyonik karaktere sahiptir . Molekül , bu iki rezonans yapısı tarafından temsil edildiği gibi, bir karbanyon gibi reaksiyona girer . (C–Li bağı üzerindeki polarite hesaplamaları göz önüne alındığında, tek bir t -bütillityum molekülünün "gerçek" yapısı , muhtemelen, merkezi karbon atomunun ~%50 kısmi bir kısmi sahip olduğu, gösterilen iki rezonans katkısının yaklaşık ortalamasıdır. lityum atomu ~%50 kısmi pozitif yüke sahipken negatif yük.)
Kimyasal özellikler
n -bütillityuma benzer şekilde , tert -bütillityum, lityumun halojenlerle değiştirilmesi ve aminlerin ve aktifleştirilmiş C-H bileşiklerinin protonsuzlaştırılması için kullanılabilir.
Bu bileşik ve diğer alkillityum bileşiklerinin eter çözücüler ile reaksiyona girdiği bilinmektedir; yarı ömrü ve ters -butillityum 60 dakika 0 ° C'de dietil eter , 40 dakika -20 ° C , tetrahidrofuran (THF), -70 ° C'de ve yaklaşık 11 dakika ° C dimetoksietan . Bu örnekte, tert -butillityum'un (THF) ile reaksiyonu gösterilmektedir:
Bu çözücüler tarafından bozunmayı en aza indirmek için, tert -bütillityum içeren reaksiyonlar genellikle Trapp çözücü karışımı gibi özel çözücüler içinde çok düşük sıcaklıklarda gerçekleştirilir .
Emniyet
tert -butillityum piroforik bir maddedir, yani havaya maruz kaldığında kolayca alev alır. (Bir piroforik malzemenin kesin bir tanımı, "54,55 °C (130,19 °F) altında havada kendiliğinden tutuşan[lar]" şeklindedir.) Yaygın ticari müstahzarlarda kullanılan solventlerin kendileri yanıcıdır. Bu bileşikle kanül transferi kullanarak çalışmak mümkün olsa da, iğne veya kanülün ucundaki tert -butillityum kalıntıları alev alabilir ve kanülü lityum tuzları ile tıkayabilir. Bazı araştırmacılar bu "pilot ışık" etkisini ürünün "taze" olduğunun ve zaman veya yanlış saklama/işleme nedeniyle bozulmadığının bir işareti olarak kabul ederken, diğerleri iğne ucunu veya kanülü kısa bir cam tüp içine yerleştirmeyi tercih ediyor. inert bir gazla yıkandı ve her bir uçta septa ile kapatıldı. Tert -butillityum içeren ciddi laboratuvar kazaları meydana geldi. Örneğin, 2008 yılında personel araştırma asistanı Sheharbano Sangji ait laboratuvarda Patrick Harran de California Üniversitesi, Los Angeles , ciddi ile ateşlenir bir yangında yanmış sonucu hayatını kaybetti tert -butillityum.
Tert -butillityum dietil eter ve tetrahidrofuran gibi eterlerle karıştırıldığında büyük ölçekli reaksiyonlar kaçak reaksiyonlara, yangınlara ve patlamalara yol açabilir . Hidrokarbon çözücülerin kullanımı tercih edilebilir.
Bu bileşiğin havadaki oksijen ve nem ile şiddetli reaksiyona girmesini önlemek için havasız teknikler önemlidir:
- t -BuLi + O 2 → t -BuOOLi
- t -BuLi + H 2 O → t -BuH + LiOH




