Enol - Enol
Enoller veya daha resmi, alkenols , reaktif bir yapı türü ya da olan ara ürün olarak organik kimyada bir şekilde temsil edilir alken ( olefin bir ile) hidroksil grubunun alken bir ucuna bağlanmış çift bağı . Terimleri enol ve alkenol olan birleşik sözcük "-en" / "alken" ve belirten "ol" soneki türeyen hidroksil grubu arasında alkoller ilk dönem terminal "-e" bırakarak. (Enol üretilmesi genellikle, bir hidrojen bitişik kaldırılmasını içerir a -) karbonil grubu-yani için deprotonasyon bir şekilde kendi kaldırma proton H + . Bu proton aşamalı sürecin sonunda geri döndürülmediğinde, sonuç, enolat olarak adlandırılan bir anyondur (sağdaki resimlere bakın). Gösterilen enolat yapıları şematiktir; daha modern bir temsil , enolattaki elektronlar tarafından oluşturulan ve işgal edilen moleküler orbitalleri ele alır. Benzer şekilde, enol oluşumuna çoğu kez hidroksi grubunun bir silil enol eter gibi bir eter olarak "yakalanması" veya maskelemesi eşlik eder .
Olarak organik kimya , keto-enol tautomerizm bir belirtmektedir kimyasal denge a arasındaki keto formu, (a keton ya da bir aldehit ) ile bir enol (bir alkol ). Keto ve enol formlarının birbirlerinin totomerleri olduğu söyleniyor . İki formun karşılıklı dönüşümü, bir alfa hidrojen atomunun hareketini ve bağ elektronlarının yeniden düzenlenmesini içerir ; dolayısıyla, izomerizm , tatomerizm olarak nitelendirilir.
Enolizasyon
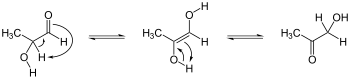
Bir a-hidrojene sahip organik esterler , ketonlar ve aldehitler ( karbonil grubuna bitişik CH bağı ) sıklıkla enolleri oluşturur. Reaksiyon, bir protonun karbondan oksijene göçünü içerir:
- RC (O) CHR ' 2 RC (OH) = CR' 2
Ketonlar söz konusu olduğunda, dönüşüm keto-enol tautomerizmi olarak adlandırılır, ancak bu ad genellikle daha genel olarak tüm bu tür totomerizasyonlara uygulanır. Genellikle denge sabiti o kadar küçüktür ki, enol spektroskopik olarak saptanamaz.
İki (veya daha fazla) karbonil içeren bazı bileşiklerde, enol formu baskın hale gelir. 2,4-pentanedionun davranışı bu etkiyi göstermektedir:
| karbonil | Enol | K enolizasyon |
|---|---|---|
| CH 3 CHO | CH 2 = CHOH | 5,8 x 10 −7 |
| CH 3 C (O) CH 3 | CH 3 C (OH) = CH 2 | 5,12 x 10 −7 |
| CH 3 CO 2 CH 3 | CH 2 = CH (OH) OCH 3 | 4x10 −20 |
| C 6 H 5 C (O) CH 3 | Cı 6 H 5 C (OH) = CH 2 | 1 x 10 −8 |
| CH 3 C (O) CH 2 , C (O) CH 3 | CH 3 C (O) CH = C (OH) CH 3 | 0.27 |
Enoller, C = C-OH bağlantılı vinil alkol türevleridir . Organik karbonillerin protonsuzlaşması, güçlü bir nükleofil olan enolat anyonunu verir . Keto formunu tercih etmenin klasik bir örneği vinil alkol ve asetaldehit arasındaki dengede görülebilir (K = [enol] / [keto] ≈ 3 × 10 −7 ). Olarak 1,3-diketonlar gibi, asetilaseton (2,4-pentandion), enol biçimi tercih edilir.
Bir enolün keto formuna asitle katalize edilen dönüşümü O'dan karbona proton transferiyle ilerler. İşlem molekül içi olarak gerçekleşmez, ancak çözücü veya diğer aracıların katılımını gerektirir.
Ketonizasyonun stereokimyası
R 'ise 1 ve R 2 (sayfanın üst not eşitliği) farklı ikame ediciler, alfa pozisyonunda oluşan yeni bir stereomerkez olduğunda da keto formu için bir enol dönüştürür. Üç R grubunun doğasına bağlı olarak, bu durumda ortaya çıkan ürünler diastereomerler veya enantiyomerler olacaktır .
Enedioller
Enedioller, C = C çift bağının her karbonu üzerinde bir hidroksil grubu bulunan alkenlerdir. Normalde bu tür bileşikler, asilinler ile dengede bulunan istenmeyen bileşenlerdir . Özel bir durum olan katekol C = C alt-birimi, bir aromatik halkanın bir parçası olur. Bununla birlikte, diğer bazı durumlarda, enedioller, karbonil gruplarını çevreleyerek stabilize edilir. Bunlar stabilize enediols denilen vardır reductones . Bu tür türler glikokimyada önemlidir, örneğin Lobry de Bruyn-van Ekenstein dönüşümü .
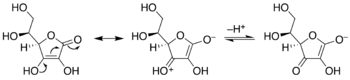
 Keto-enediol tautomerizasyonları. Merkezde Enediol; asilino izomerleri solda ve sağda. Örn. olduğu hidroksiasetondan sağda gösterildiği,.
Keto-enediol tautomerizasyonları. Merkezde Enediol; asilino izomerleri solda ve sağda. Örn. olduğu hidroksiasetondan sağda gösterildiği,.
Fenoller
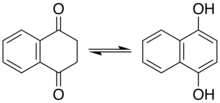
Fenoller bir tür enolü temsil eder. Bazı fenoller ve ilgili bileşikler için keto tautomer önemli bir rol oynar. Resorsinol reaksiyonlarının çoğu örneğin keto tautomeri içerir. Naftalin-1,4-diol, diketon tetrahidronaftalin-1,4-dion ile gözlemlenebilir bir denge içinde bulunur.
Biyokimya
Keto – enol tautomerizmi, biyokimyanın çeşitli alanlarında önemlidir .
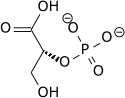
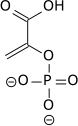
Fosfoenolpiruvatın yüksek fosfat transfer potansiyeli , fosforile bileşiğin daha az termodinamik olarak uygun enol formunda "tutulmasından" kaynaklanırken, defosforilasyondan sonra keto formunu alabilir.
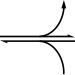
Enzim enolaz dehidrasyonunu katalize 2-fosfogliserik asit enol fosfat ester. PEP metabolizması piruvik asit ile piruvat kinaz (PK) oluşturur adenosin trifosfat ile (ATP) alt-tabaka düzeyinde fosforilasyon .
|
|

|
||||
| H 2 O | ADP | ATP | ||||
|

|
|||||
| H 2 O | ||||||
Reaktivite
Enollerde çift bağın terminali nükleofiliktir . Elektrofilik organik bileşiklerle reaksiyonları, çok çeşitli önemli yaşam süreçlerinde (yani biyokimyada , enzimle katalize edilmiş reaksiyonlarda ara maddeler olarak) enol bazlı ara maddelerin muazzam öneminin yanı sıra modern sentetik organik kimyanın merkezi (örn. , aldol uygulamalarında ve ilgili reaksiyonlarda).
Enolates
Enolize edilebilir ketonların, aldehitlerin ve esterlerin deprotonasyonu , enolatları verir . Enolatlar, oksijene elektrofillerin eklenmesiyle yakalanabilir. Sililasyon, silil enol eteri verir . Asilasyon, vinil asetat gibi esterler verir .
Kararlı enoller
Genel olarak, enoller, C = O çift bağının C = C çift bağına göre olumlu olmasından dolayı keto eşdeğerlerinden daha az kararlıdır. Bununla birlikte, enoller kinetik veya termodinamik olarak stabilize edilebilir.
Kinetik olarak kararlı enoller
Kinetik olarak kararlı enoller çok yavaş bir şekilde keto şekline geri döner. Keto formu termodinamik olarak tercih edilir, ancak enol kinetik olarak kararlı olacak kadar uzun süre hayatta kalır. Enol oluşumu gibi, enolden keton oluşumu da asit veya baz tarafından katalize edilir. İkisi de olmadan, enol formunun biraz uzun bir ömrü vardır. Örneğin, etilen glikolü düşük basınçta 900 ° C'ye ısıtmak, asetaldehidin enolü olan vinil alkolü verecektir. Asetaldehit hala enol formuna göre tercih edilir, ancak katalizör olmadan oluşum çok yavaş ilerler.
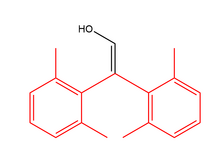
Enoller, karbon atomunun protonlanması çok zorsa da kararlı olabilir. Sterik engelleme bir protonlama maddesini bloke edebilir ve protonasyon olmadan keton oluşamaz. Sağdaki örnekte, iki benzen halkası enolü proton saldırısından korur, böylece enol kinetik olarak kararlıdır.
Termodinamik olarak kararlı enoller
Termodinamik olarak kararlı enoller, enolün yer değiştirmesi ve rezonans ile stabilize edilir. Bu etkilere izin veren işlevsel gruplar ekleyerek bunları oluşturabiliriz. Bazı 1,3-dikarbonil bileşikleri , enol formunda nispeten kararlıdır. (1,3) düzenlemesi ile enoller, iki karbonil grubu ile birleştirilir. Tautomerizasyon yoluyla , iki enol hızlı denge içindedir. 1,3-dikarbonillerdeki diğer bir stabilize edici faktör, molekül içi hidrojen bağlanmasıdır. Bu faktörlerin ikisini de asetilasetonda görebiliriz. Molekül içi hidrojen bağı, uygun altı üyeli bir halka oluşturur.
Ek olarak, bir enol oluşumu bir konjuge rezonans sistemi yaratırsa, artan rezonans da daha uygundur ve enolü stabilize edebilir. Aşağıdaki örnekte, keton formunda, iki halka tek bir rezonans sistemi oluşturamaz, ancak enol formu tüm molekülü tamamen konjuge bir sistem haline getirerek daha fazla rezonans ve stabilite ekler.
En kararlı enoller fenollerdir . Enol formu aromatiklik ile stabilize edilir, bu da bir C = O bağının bir C = C bağına sahip olmasının avantajından büyük ölçüde daha ağır basmaktadır. Sonuç olarak, bu moleküller yalnızca fenol formunda bulunur ve fenolün "ketonu" gözlenmez.
Ayrıca bakınız
- Alkenal
- Enolaz
- Keton
- Ynol
- Su çözeltilerinde başka bir keton ve aldehit formu olan Geminal diol
- Bölge seçiciliği