Disülfür diklorür - Disulfur dichloride
|
|||
|
|
|||
| İsimler | |||
|---|---|---|---|
|
IUPAC adı
disülfür diklorür
|
|||
|
Sistematik IUPAC adı
diklorodisülfan |
|||
| Diğer isimler
Bis[kloridokükürt]( S – S )
dimerik sülfenik klorür |
|||
| tanımlayıcılar | |||
|
3B model ( JSmol )
|
|||
| Kimyasal Örümcek | |||
| ECHA Bilgi Kartı |
100.030.021 |
||
| AT Numarası | |||
| ağ | kükürt+monoklorür | ||
|
PubChem Müşteri Kimliği
|
|||
| RTECS numarası | |||
| ÜNİİ | |||
| BM numarası | 3390 | ||
|
CompTox Panosu ( EPA )
|
|||
|
|||
|
|||
| Özellikleri | |||
| S 2 Cl 2 | |||
| Molar kütle | 135.04 g/mol | ||
| Görünüm | Açık kehribardan sarı-kırmızıya, yağlı sıvı | ||
| Koku | keskin, mide bulandırıcı, rahatsız edici | ||
| Yoğunluk | 1.688 g / cc 3. | ||
| Erime noktası | −80 °C (−112 °F; 193 K) | ||
| Kaynama noktası | 137.1 °C (278.8 °F; 410.2 K) | ||
| HCl kaybı ile ayrışır | |||
| çözünürlük | etanol , benzen , eter , kloroform , CCl 4 içinde çözünür | ||
| Buhar basıncı | 7 mmHg (20 °C) | ||
| -62,2 · 10 -6 cm 3 / mol | |||
|
Kırılma indisi ( n D )
|
1.658 | ||
| yapı | |||
| C 2 , gazlı bez | |||
| 1.60 D | |||
| Tehlikeler | |||
| Güvenlik Bilgi Formu | ICSC 0958 | ||
|
AB sınıflandırması (DSD) (eski)
|
Toksik ( T ) Zararlı ( Xn ) Aşındırıcı ( C ) Çevre için tehlikeli ( N ) |
||
| R cümleleri (modası geçmiş) | R14 , R20 , R25 , R29 , R35 , R50 | ||
| S-ifadeleri (modası geçmiş) | (S1/2) , S26 , S36/37/39 , S45 , S61 | ||
| NFPA 704 (ateş elması) | |||
| Alevlenme noktası | 118,5 °C (245,3 °F; 391,6 K) | ||
| 234 °C (453 °F; 507 K) | |||
| Ölümcül doz veya konsantrasyon (LD, LC): | |||
|
LC Lo ( yayınlanan en düşük )
|
150 ppm (fare, 1 dk) | ||
| NIOSH (ABD sağlığa maruz kalma sınırları): | |||
|
PEL (İzin Verilebilir )
|
TWA 1 ppm (6 mg/m 3 ) | ||
|
REL (Önerilen)
|
C1 ppm (6 mg / m 3 ) | ||
|
IDLH (Ani tehlike)
|
5 sayfa/dk | ||
| Bağıntılı bileşikler | |||
|
İlgili kükürt klorürler
|
Sülfür diklorür Tiyonil klorür Sülfüril klorür |
||
|
Bağıntılı bileşikler
|
Disülfür diflorür Disülfür dibromür |
||
|
Aksi belirtilmedikçe, veriler standart durumdaki malzemeler için verilmiştir (25 °C [77 °F], 100 kPa'da). |
|||
|
|
|||
| Bilgi kutusu referansları | |||
Disülfit diklorür olan inorganik bileşik bir kükürt ve klor ile formül G 2 CI 2 .
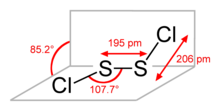
Bu bileşik için bazı alternatif isimler, kükürt monoklorür ( ampirik formülü SCI ile ima edilen isim ), disülfür diklorür (İngiliz İngilizcesi Yazımı ) ve kükürt monoklorürdür (İngiliz İngilizcesi Yazımı ). S 2 Cl 2 Cl−S−S−Cl formülünün ima ettiği yapıya sahiptir, burada Cl a −S−S ve S−S−Cl b düzlemleri arasındaki açı 90°'dir. Bu yapı gauche olarak adlandırılır ve H 2 O 2 için olana benzer . Nadir bir izomer G 2 Cl 2 S = SCL 2 ; S, bu izomer formları, geçici 2 Cı 2 UV ışınlarına maruz kalmaktadır (bakınız thiosulfoxides ).
Sentez, temel özellikler, reaksiyonlar
Saf disülfür diklorür, su ile reaksiyona girerek nemli havada "duman" olan sarı bir sıvıdır. İdealleştirilmiş (ancak karmaşık) bir denklem:
- 16 S 2 Cl 2 + 16 H 2 O → 8 SO 2 + 32 HCl + 3 S 8
Elementel kükürtün kısmi klorlanmasıyla üretilir. Reaksiyon, oda sıcaklığında kullanılabilir oranlarda ilerler. Laboratuvarda, klor gazı, elementel kükürt içeren bir şişeye yönlendirilir. Disülfür diklorür oluştuğunda, içerikler altın sarısı bir sıvı haline gelir:
- S 8 + 4 Cl 2 → 4 S 2 Cl 2 , ΔH = -58.2 kJ/mol
Fazla klor , sıvının daha az sarı ve daha turuncu-kırmızı olmasına neden olan kükürt diklorür üretir :
- S 2 Cl 2 + Cl 2 ↔ 2 SCl 2 , ΔH = −40.6 kJ/mol
Reaksiyon geri alınabilir ve bekletildiğinde, SCL 2 serbest bırakır klor disülfit diklorid dönüş. Disülfür diklorür, kısmen polisülfan oluşumunu yansıtan büyük miktarlarda kükürt çözme yeteneğine sahiptir :
- S 2 Cl 2 + n S → S 2+n Cl 2
Disülfür diklorür, fazla elementel kükürtten damıtılarak saflaştırılabilir.
S 2 Cı 2 de klorlanması sonucu ortaya çıkar CS 2 sentezinde olarak tiofosgen .
Reaksiyonlar
S 2 Cı 2 hidrolize için sülfür dioksit ve element kükürt. Hidrojen sülfür ile işlendiğinde, aşağıdaki ideal formülde belirtildiği gibi polisülfanlar oluşur:
- 2 H 2 S + S 2 Cl 2 → H 2 S 4 + 2 HCl
Heptasülfür imid (S 7 NH) ve ilgili S−N halkaları S 8−x (NH) x (x = 2, 3) vermek üzere amonyak ile reaksiyona girer .
Uygulamalar
S 2 Cl 2 , C−S bağlarını tanıtmak için kullanılmıştır. Varlığında alüminyum klorid (AlCb 3 ), S 2 Cı 2 benzen ile tepkimeye girer için vermek difenil sülfid:
- S 2 Cl 2 + 2 C 6 H 6 → (C 6 H 5 ) 2 S + 2 HCl + 1/8 S 8
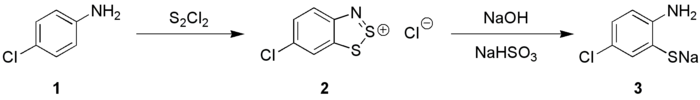
Anilinler (1) S ile tepkimeye 2 Cı 2 1,2,3-benzodithiazolium tuzları (2), (vermek üzere NaOH varlığında Herz Reaksiyon transforme edilebilir) orto için -aminothiophenolates (3), bu türler ön tioindigo boyalar.
Aynı zamanda , yaygın olarak "hardal gazı" olarak bilinen sülfür hardalı hazırlamak için , 60 °C'de etilen ile reaksiyona girerek (Levinstein işlemi) kullanılır:
- S 2 Cl 2 + 2 C 2 H 4 → (ClC 2 H 4 ) 2 S + 1/8 S 8
S diğer kullanımları 2 Cı 2 kükürt boyaları, böcek öldürücüler, ve sentetik kauçuklar imalatını içerir. Ayrıca kauçukların soğuk vulkanizasyonunda, bitkisel yağlar için polimerizasyon katalizörü olarak ve yumuşak ahşabın sertleştirilmesinde kullanılır.
Güvenlik ve düzenleme
Bu madde, Çizelge 3 Kısım B – Kimyasal Silahlar Sözleşmesinin (CWC) Ön Madde Kimyasalları'nda listelenmiştir. Planlanmış kimyasalları üreten ve/veya işleyen ve/veya tüketen tesisler, OPCW (Kimyasal Silahların Yasaklanması Örgütü) tarafından kontrol, raporlama mekanizmaları ve denetime tabi olabilir.