Sodyum peroksit - Sodium peroxide

|
|
|
|

|
|
| İsimler | |
|---|---|
| Diğer isimler
Disodyum dioksit
Flocool Solozone Disodyum peroksit |
|
| tanımlayıcılar | |
|
3B model ( JSmol )
|
|
| Kimyasal Örümcek | |
| ECHA Bilgi Kartı |
100.013.828 |
| AT Numarası | |
|
PubChem Müşteri Kimliği
|
|
| RTECS numarası | |
| ÜNİİ | |
| BM numarası | 1504 |
|
CompTox Panosu ( EPA )
|
|
|
|
|
|
| Özellikler | |
| Na 2 O 2 | |
| Molar kütle | 77.98 g/mol |
| Dış görünüş | sarı ila beyaz toz |
| Yoğunluk | 2.805 g / cc 3. |
| Erime noktası | 460 °C (860 °F; 733 K) (çözünür) |
| Kaynama noktası | 657 °C (1.215 °F; 930 K) (çözünür) |
| şiddetle tepki verir | |
| çözünürlük | asitte çözünür bazda çözünmez etanol ile reaksiyona girer |
| -28,10 · 10 -6 cm 3 / mol | |
| Yapı | |
| altıgen | |
| Termokimya | |
|
Isı kapasitesi ( C )
|
89.37 J/(mol·K) |
|
Std molar
entropi ( S |
95 J/(mol·K) |
|
Std
oluşum entalpisi (Δ f H ⦵ 298 ) |
-515 kJ·mol -1 |
|
Gibbs serbest enerjisi (Δ f G ˚)
|
-446,9 kJ/mol |
| Tehlikeler | |
| Güvenlik Bilgi Formu | Harici MSDS |
|
AB sınıflandırması (DSD) (eski)
|
|
| R cümleleri (modası geçmiş) | R8 , R35 |
| S-ifadeleri (modası geçmiş) | (S1/2) , S8 , S27 , S39 , S45 |
| NFPA 704 (ateş elması) | |
| Alevlenme noktası | Yanıcı değil |
| Bağıntılı bileşikler | |
|
Diğer katyonlar
|
Lityum peroksit Potasyum peroksit Rubidyum peroksit Sezyum peroksit |
|
Sodyum oksit Sodyum süperoksit |
|
|
Bağıntılı bileşikler
|
Sodyum hidroksit Hidrojen peroksit |
|
Aksi belirtilmediği sürece, veriler standart durumdaki malzemeler için verilmiştir (25 °C [77 °F], 100 kPa'da). |
|
|
|
|
| Bilgi kutusu referansları | |
Sodyum peroksit , Na 2 O 2 formülüne sahip inorganik bileşiktir . Bu sarımsı katı, fazla oksijende ateşlenen sodyumun ürünüdür. Güçlü bir temeldir. Bu metal peroksit , Na 2 O 2 · 2H 2 O 2 4H 2 O, Na 2 O 2 2H 2 O, Na 2 O 2 2H 2 O 2 ve Na 2 O 2 8H dahil olmak üzere çeşitli hidratlarda ve peroksihidratlarda bulunur. 2 O. Hazırlanması basit olan oktahidrat, susuz malzemenin aksine beyazdır.
Özellikler
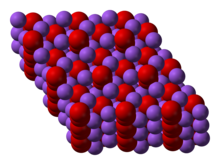
Sodyum peroksit altıgen simetri ile kristalleşir. Isıtma üzerine, altıgen form 512 °C'de bilinmeyen simetrili bir faza geçişe uğrar. 657 ° C kaynama noktasının üzerinde daha fazla ısıtma ile, bileşik Na için parçalanır 2 O serbest, O 2 .
- 2 Na 2 O 2 → 2 Na 2 O + O 2
Hazırlık
Oktahidrat, sodyum hidroksitin hidrojen peroksit ile işlenmesiyle üretilir.
Sodyum peroksit, ayrı bir aşamada oksijeni emen sodyum oksit üreten bir işlem olan 130-200 °C'de metalik sodyumun oksijenle reaksiyona girmesiyle büyük ölçekte hazırlanabilir :
- 4 Na + O 2 → 2 Na 2 O
- 2 Na 2 O + O 2 → 2 Na 2 O 2
Platin veya paladyum tüp içinde katı sodyum iyodür üzerinden ozon gazı geçirilerek de üretilebilir . Ozon, sodyum peroksit oluşturmak için sodyumu oksitler. İyot hafif bir ısıtma işlemi süblimleştirilir. Platin veya paladyum reaksiyonu katalize eder ve sodyum peroksit tarafından saldırıya uğramaz.
kullanır
Sodyum peroksit , reaksiyona göre sodyum hidroksit ve hidrojen peroksit verecek şekilde hidrolize olur.
- Na 2 O 2 + 2 H 2 O → 2 NaOH + H 2 O 2
Kağıt ve tekstil üretimi için odun hamurunu ağartmak için sodyum peroksit kullanıldı. Şu anda esas olarak, örneğin çeşitli cevherlerden minerallerin çıkarılması gibi özel laboratuvar işlemleri için kullanılmaktadır. Sodyum peroksit, Solozone ve Flocool'un ticari adlarıyla geçebilir . Kimya müstahzarlarında, oksitleyici bir ajan olarak sodyum peroksit kullanılır. Oksijen ve sodyum karbonat üretmek için karbon dioksit ile reaksiyona girerek oksijen kaynağı olarak da kullanılır:
- 2 Na 2 O 2 + 2 CO 2 → 2 Na 2 CO 3 + O 2
Bu nedenle özellikle tüplü teçhizatta, denizaltılarda vb. faydalıdır. Lityum peroksit ve potasyum süperoksit benzer kullanımlara sahiptir.

