Adenozin difosfat reseptör inhibitörü - Adenosine diphosphate receptor inhibitor
Adenozin difosfat ( ADP ) reseptör inhibitörleri bir olan ilaç sınıfı içinde trombosite karşı maddelerin tedavisinde kullanılan, akut koroner sendrom (AKS) riskinde olan hastalarda ya da önleyici tedavisinde tromboembolizm , miyokardiyal enfarktüs ya da inme . Bu ilaçlar P2Y 12 trombosit reseptörleriniantagonizeeder ve dolayısıyla ADP'nin P2Y 12 reseptörünebağlanmasını önler. Bu, trombosit agregasyonunda bir azalmaya yol açarak trombüs oluşumunu engeller. P2Y 12 reseptörü,kan trombositlerinde bulunanyüzeye bağlı bir proteindir . G proteinine bağlı purinerjik reseptörlere (GPCR)aittirlerveADPiçin kemoreseptörlerdir .
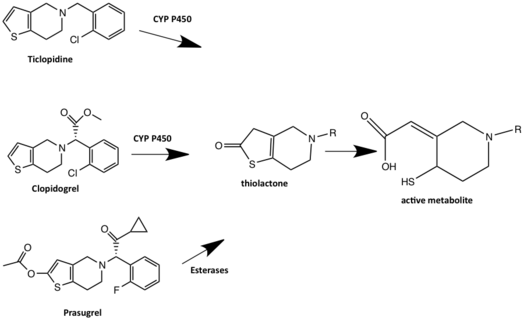
Bu sınıfa giren ilk ilaç tiklopidindir ancak yan etkileri nedeniyle günümüzde pek kullanılmamaktadır. Tiklopidin , klopidogrel ve prasugrel (Efient), P2Y 12 reseptörünün geri dönüşümsüz inhibisyonuna neden olan tienopiridinlerdir . Bunların tümü , P2Y 12 reseptörünü inhibe etmek için in-vivo aktif bir metabolite dönüştürülmesi gereken ön ilaçlardır . Diğer taraftan, böyle yeni ilaçlar tikagrelor (Brilinta®) ve cangrelor (Kengrexal®) olmayan tienopiridinler ve geri çevrilebilir şekilde önleyebildikleri P2Y olan 12 daha hızlı başlangıcı ve kaymasına metabolik aktivasyonu ve ekranın gerek kalmadan reseptörü üzerinde doğrudan etki anlamına gelir.
Bu ilaçlar, özellikle ACS'li veya perkütan koroner girişim (PCI) geçiren hastalarda trombosit inhibisyonunu arttırmak için sıklıkla aspirin (asetilsalisilik asit) ile kombinasyon halinde uygulanır .
Tarih
ADP inhibitörlerinin zamanından önce, antitrombotik olayları tedavi etmek için piyasadaki tek antiplatelet ajan aspirindi. Bununla birlikte, yüksek riskli hastalarda tekrarlayan iskemik olaylar nedeniyle, diğer önemli sinyal yollarını hedef alan antiplatelet ilaçların geliştirilmesi için bir temel vardı.
Araştırmacılar benzer ilaçların en fazla aradığı 1972 yılında başlatılan ADP inhibitörlerinin geçmişi antienflamatuvar ajan tinoridin, antienflamatuar ve bir tienopiridin analjezik iki yıl önce yayınlanan edilmişti etkileri. Tiyenopiridin kimyası bilgisine dayanarak, önemli sayıda tienopiridin türevleri sentezlendi. Türevler, farelerde ve sıçanlarda in -vivo ve ex-vivo olarak test edildi , ancak testlerin sonuçları, herhangi bir anti-inflamatuar veya analjezik etki göstermedi, bunun yerine, beklenmeyen antiplatelet ve antitrombotik etkiler gösterdiler. O zamanlar trombosit agregasyonu, tromboz ve kardiyovasküler olaylar arasındaki bağlantı tartışmalı olduğundan yeni antiplatelet ajanların taranması çok nadirdi . Ancak en aktif türev olan tiklopidin, daha fazla geliştirme için seçildi. Tiklopidin, trombosit inhibisyonunu artıran ve böylece gerçek koroner sendrom ve diğer kardiyovasküler hastalıkların tedavisinde kullanılan ilk nesil tienopiridindi. Tiklopidinin bildirilen ciddi yan etkileri nedeniyle ikinci ve üçüncü tiyenopiridinler, klopidogrel ve prasugrel geliştirilmiştir.
Tiklopidin ve klopidogrel, 1978'de tiklodipin ve 1998'de klopidogrel piyasaya sürüldüğünde, bu iki ana antitrombotik ilacın etki mekanizması tam olarak anlaşılmamıştı. Gösterilen, bunların ADP ile indüklenen trombosit agregasyonunun güçlü inhibitörleri olduklarıydı, ancak P2Y 12 reseptörü tanımlanmamıştı. Ayrıca, tiklopidin ve klopidogrelin ön ilaçlar olduğu açıktı, bu da bunların in vitro olarak inaktif oldukları ve bu nedenle in vivo olarak aktive edilmeleri için metabolizmaya ihtiyaç duydukları anlamına gelir . Bu ilaçların aktif metabolitlerinin izole edildiği ve karakterize edildiği 2000 yılına kadar değildi. Yaklaşık bir yıl sonra ADP için P2Y 12 trombosit reseptörü tanımlandı. Bu keşiflerin ardından aktif metabolitler ve bunların oluşumundan sorumlu enzimler aşamalı olarak tanımlandı. Böylece tiklopidinin keşfinden 30 yıldan fazla bir süre sonra ve klopidogrelin keşfinden 10 yıldan fazla bir süre sonra bu iki ilacın etki mekanizması açıklanmıştır.
geliştirme
tiyenopiridinler
tiklopidin
İlk P2Y 12 inhibitörleri, tienopiridin ailesindendi. ADP ile indüklenen trombosit agregasyonunu ve aktivasyonunu bloke eden dolaylı antagonistlerdir. Bu sınıfın ilk ilacı tiklopidindi ve 1972'de Porcor'da (şimdi Sanofi ) keşfedildi . Tinoridine dayalı yeni bir anti-inflamatuar ilaç taranırken keşfedildi. Hem in vivo hem de ex vivo kemirgen modellerinde test edilmiş bir fenotipik tarama yaklaşımıyla tarandı . Yüksek antiplatelet aktivite gösterdi.
Tiklopidinin iyi vaatleri vardı ve klinik denemeler için seçildi. 1978'de Fransa'da pazarlandı ve inmenin birincil ve ikincil önlenmesi için ABD pazarına ulaştığında 1991'de küresel oldu.
Hayvanlarda daha iyi aktivite/ toksisite oranına sahip başka bir tienopiridin analoğu arayışı , tiklopidin klinik öncesi denemelere girer girmez başladı . Tiklopidin nedeniyle ciddi hematolojik bozuklukları olan hastaların raporlarından sonra yeni bir analog bulmak daha acil hale geldi .
klopidogrel
İkinci nesil bir tienopiridin olan klopidogrel, 1987'de klinik öncesi denemelere başladı ve 1998'de küresel pazara ulaştı. Etki mekanizması ve öncüsü tiklopidin hala bilinmiyordu. Bilinen tek şey, in vitro herhangi bir aktivite göstermedikleri için ön ilaç oldukları, uzun etki süreleri nedeniyle trombositleri geri dönüşümsüz olarak etkiledikleri ve aktif metabolitin kimyasal ve biyolojik olarak kararsız olduğuydu. 2000 yılına kadar aktif metabolit keşfedilmedi ve trombosit hedefi bir yıl sonra, ADP'nin P2Y 12 reseptörü keşfedildi .
Klopidogrel, tiklopidinden daha iyi aktivite/toksisite oranına sahip olmasına rağmen, hastaların %30'unda klopidogrel direnci olduğundan aktivitesiyle ilgili problemler vardı. Klopidogrel direncindeki ana faktör, hastaların %30-55'inde görülen CYP2C19 polimorfizmidir. Bu, klopidogrelin aktif metabolitine zayıf bir şekilde dönüştürülmesine yol açan enzimin fonksiyon kaybına yol açmıştır. Metabolit kendisi çok kararsız olduğu ve bu nedenle de bir parçası olarak depolanamaz kimyasal kütüphane . Bu, CYP aracılı metabolizmaya daha az dayanan bir bileşik olan prasugrel'in geliştirilmesine yol açtı.
prasugrel
Prasugrel, üçüncü nesil tienopiridin, ilaç şirketleri Daiichi Sankyo/Eli Lilly tarafından 2009 yılında piyasaya sürüldü. Prasugrel, öncülleri gibi bir ön ilaçtır ancak metabolizması, esteraz tarafından bir tiolaktona metabolize edildiği bağırsaklarda başlar, bu aktif olmayan ara ürün daha sonra, esas olarak CYP3A4 ve CYP2B6 tarafından aktif metabolite CYP aracılı halka açılmasına uğrar . Böylece prasugrel, klopidogrel direncine maruz kalmaz.
Yeni nesil ADP reseptör inhibitörleri
tikagrelor
Odak , bir metabolit olmayan ve daha hızlı etki başlangıcı olan bir P2Y 12 inhibitörü bulmaya gitti . ATP'nin ADP'nin neden olduğu trombosit agregasyonunu rekabetçi bir şekilde antagonize ettiği biliniyordu, ancak ATP çok kararsız. Dikkat, daha yüksek potens ve stabiliteye sahip ATP analogları yaratmaya gitti. Bu analoglar, trifosfat gruplarının tutulması nedeniyle çok kısa yarı ömre sahipti ve bu nedenle IV verilmesi gerekiyordu. Bu analogların modifikasyonu, seçici ve stabil bir fosfat olmayan P2Y 12 reseptör antagonisti olan tikagrelorun keşfedilmesine yol açtı . Ticagrelor, siklopentil-triazolopirimidin (CPTP) sınıfına aittir. Ticagrelor, 2010 yılında Avrupa'da, 2011 yılında ABD'de piyasaya çıktı.
kangrelor
Cangrelor, ticagrelor gibi başka bir ATP analoğu, enzimatik bozulmaya karşı stabildir. Tienopiridinler gibi aktif bir metabolite parçalanmadığı için hızlı bir etki başlangıcına sahiptir. AstraZeneca , Aralık 2003'te cangrelor için özel lisans aldı . 2009'da, kangrelorun plaseboya karşı test edildiği 3. aşama denemesinin sponsoru çekildi. Cangrelor gelişimi, geçici analiz inceleme komitesinin (IARC) denemenin düzenleyici onay için gerekli olan “ikna edici” klinik etkinliği göstermeyeceğine karar vermesinin ardından sponsor geri çekilince bir süreliğine durduruldu. Ancak Champion phoenix çalışması (biyofarmasötik şirketi The Medicines Company sponsorluğunda), çift kukla, çift kör, plasebo kontrollü bir çalışma olup, oldukça acil veya elektif PCI uygulanan 11.145 hasta, PCI gösterilmeden önce kangrelor veya klopidogrel almak üzere rastgele atanmıştır. Bu cangrelor, PCI sırasında iskemik olayların oranını önemli ölçüde azalttı. Cangrelor, stent trombozu gelişimini klopidogrelden daha fazla azalttı. Bu bulgular 2013'te yayınlandı. Cangrelor , Haziran 2015'te intravenöz uygulama için bir antiplatelet ilaç olarak FDA onayı aldı.
Hareket mekanizması
Moleküler hedef ADP reseptör inhibitörleri aktif metaboliti P2Y olan 12 reseptörü. P2Y 12 reseptörü, G-bağlı bir reseptördür ve adenozin difosfat tarafından aktive edilir . ADP , adenil siklazın inhibisyonuna yol açan ve böylece hücre içi cAMP seviyelerini azaltan P2Y 12 reseptörüne bağlanır . cAMP'nin bu azalması , glikoprotein IIb/IIIa reseptörlerinin aktivasyonuna yol açan vazodilatör ile uyarılan fosfoproteinin fosforilasyonunu azaltır . Glikoprotein IIb/IIIa reseptörlerinin aktivasyonu, tromboksan üretimini ve uzun süreli trombosit agregasyonunu arttırır . Tiklopidin, klopidogrel ve prasugrel, P2Y 12 reseptörünün geri dönüşümsüz trombosit inhibitörleri olan tienopiridin ön ilaçlarıdır . Cangrelor ve tikagrelor, P2Y 12 reseptörünün konformasyonunu değiştiren ve bu nedenle reseptörün geri dönüşümlü trombosit inhibisyonu ile sonuçlanan doğrudan etkili P2Y 12 inhibitörleridir . Tienopiridinler karaciğerde ve bağırsakta aktif metabolitlere metabolize edilir.
Metabolizma
Tiklopidin bir ön ilaçtır ve en az beş ana yolla metabolize edilir. Tanımlanmış ve antiplatelet aktiviteye sahip olduğu gösterilen bir aktif metabolit vardır. Bu aktif metabolit, CYP'ye bağlı bir yolla oluşturulur. CYP2C19 ve CYP2B6 için tiklopidin metabolik dönüşüme katkıda önerilen enzimlerdir tıyolakton karaciğer içinde bir ara madde, 2-okso-tiklopidin. Tiolakton ara ürünü daha sonra oksidasyon aktivasyonunun meydana geldiği CYP oksidasyonu yoluyla tiklopidin aktif metabolitine dönüştürülür . Ancak bu yolakta yer alan CYP enzimleri bilinmemektedir. Aktif metabolit oluşumunda ek metabolitler tanımlanmıştır ve bunlar dihidrotienopiridinyum (M5) ve tienodihidropiridinyum metabolitleridir (M6). Bu metabolitler, tiklopidinin toksik yan etkilerinden sorumlu olabilir.
Klopidogrel, iki yolla metabolize edilen bir ön ilaçtır. Yollardan birinde , klopidogrel dozunun çoğu (% 85), esterazlar tarafından inaktif bir karboksilik asit türevine hidrolize edilir ve glukoridinasyon ve ardından renal atılım yoluyla hızla temizlenir . Klopidogrelin diğer yolu, P2Y 12 reseptörünü inhibe eden aktif metaboliti üretmek için iki aşamalı hepatik CYP450 metabolik aktivasyonunu gerektirir . CYP1A2, CYP3A4, CYP3A5 ve CYP2C19, klopidogrel metabolizmasında yer alan ana enzimler olarak kabul edilir. İlk klopidogrel 2-okso-klopidogrel'e metabolize olur ve bu da bir tiyol olan aktif metabolizmaya hidrolize olur . Tiyol formları disülfid bir köprü sistein P2Y içinde 12 bu şekilde reseptör ve P2Y geriye çevrilemez şekilde bağlanan 12 reseptörü. Klopidogrel'in P2Y 12 reseptörünün CYS17 veya CYS270'ine kovalent olarak bağlanması ve dolayısıyla agonistin bağlanmasını bloke etmesi önerilmektedir . Bazı klopidogrel kullanıcıları kusurlu CYP2C19 aktivitesine ve dolayısıyla klopidogrel aktivitesinde azalma riskine yol açan zayıf CYP2C19 metabolizmasına sahiptir. Bunun nedeni, ön ilacın aktif ilaca metabolize olmamasıdır. CYP2C19 inhibitörleri olan ilaçlar, klopidogrel ile etkileşime girebilir ve klopidogrel aktivitesini azaltabilir. Rabeprazol ve pantoprazol dışındaki tüm proton pompası inhibitörleri, hepatik CYP450 enzimi tarafından metabolize edilir ve bu nedenle klopidogrel metabolizması ile etkileşime girebilir. Omeprazolün, bir CYP2C19 inhibitörü olduğu için, diğer protein pompa inhibitörlerinden daha yüksek ilaç-ilaç etkileşimi potansiyeline sahip olduğu düşünülmektedir.
Prasugrel, üçüncü nesil bir tienopiridin ve bir ön ilaçtır. Tiklopidin ve klopidogrel farklı olarak, prasugel aktivasyonunun, bir ara madde hidrolize tâbi tutulmasını içerir , tiyolakton daha sonra tek bir CYP-bağımlı basamağında, aktif metabolit haline dönüştürülür. R-138727 (tiyol ara ürünü) olan aktif metabolit, ya P2Y 12 reseptörüne geri dönüşümsüz olarak bağlanır ya da inaktif bir metabolite metabolik olarak metillenir. R-138727, S-metilasyon yoluyla metabolik olarak inaktive edilir. Prasugrel, klopidogrel gibi CYP2C19 tarafından metabolize edilmez ve genetik CYP varyantları, prasugrelin aktif metabolitleri üzerinde önemli bir etkiye sahip değildir. Prasugrel, klopidogrelden daha hızlı etki başlangıcına ve aktif metabolit ile daha fazla reseptör blokesine sahiptir.
Ticagrelor, oral uygulamadan sonra aktif olan P2Y 12 reseptörünün ilk geri dönüşümlü inhibitörüydü . Ticagrelor, herhangi bir metabolik aktivasyona ihtiyaç duymadan oral olarak aktiftir. Hızla emilir ve neredeyse ana bileşiği kadar güçlü olan en az bir aktif metabolite enzimatik bozunmaya uğrar. Ticagrelor, ACS tedavisi için şu anda mevcut ilaçlara kıyasla gelişmiş farmakokinetik ve farmakodinamik profillere sahiptir . Ayrıca, klopidogrelin etkisini etkilediği bilinen CYP2C19 genotipleri , tikagrelorun etkisini etkilememiştir.
Cangrelor ilk döner P2Y olan 12 inhibitörü olduğu kutu intravenöz ve çok hızlı bir başlama ve geçerli ilaçlara göre avantaj sağlar ve cangrelor ağız P2Y bu sınırlamaların üstesinden gelmek için izin olabilir, konum 12 inhibitörü. Bu, özellikle ağızdan ilaç alamayan hastalarda (örn. bilinci kapalı, kusan veya sedasyonlu hastalar) antiplatelet tedavi için çekici bir seçenek haline getirir. Tikagrelor gibi aktif olması için metabolik dönüşüm gerektirmez ve bu nedenle P2Y 12 reseptörünü doğrudan inhibe edebilir .
İlaç tasarımı
Yapı-aktivite ilişkisi (SAR)
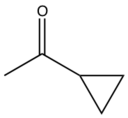
Prasugrel, metabolizma düşünülerek geliştirildi. Bu, ester grubunu metabolik olarak stabil ketonla (grup R1) değiştirerek yapıldı. Ayrıca tiyofen 2-pozisyonunda (grup R2) ester grubunun eklenmesi, aktivasyonun ilk adımını CYP2C19'dan esterazlara kaydırdı ve bu nedenle prasugrel, klopidogrel gibi CYP2C19 tarafından metabolize edilmez.
| bileşik | R1 | R2 | R3 |
| klopidogrel | C | Cl | |
| prasugrel | F |
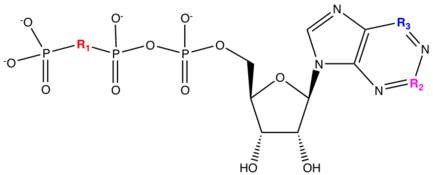
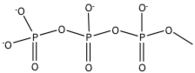
Cangrelor ve ticagrelor , tienopiridinlerin sahip olduğu güvenlik (kanama) ve yanıt vermeyen sorunları hedef almak için geliştirilmiş yeni tersinir P2Y 12 reseptörleri sınıflarıdır . Adenozin trifosfat ( ATP ) gibi doğal ligandların trombosit agregasyonunu engellediği gösterildi ve zayıf bir antagonist olarak tanımlandı . Cangrelor ve ticagrelor , adenozin trifosfata (ATP) benzeyen kimyasal bir yapıya sahip nükleotit analoglarıdır . ATP, kardiyovasküler dokularda proagregatuvar ADP, AMP veya adenosine metabolize edilebilir. Fosfor β (Pβ) ve fosfor γ (Pγ) arasındaki anhidrit oksijenin di-Kloro veya di-Floro-metilen ile değiştirilmesi, ATP'ye eşdeğer ve benzer bir pKa'ya sahip bir bileşiğe yol açar . Bu değiştirme nedeniyle, ATP'nin pro-agregasyona metabolizmasından kaçınılabilir. Zincir uzunluğuna S-propil ekleyerek aktivite üzerinde büyük bir etkisi oldu. Adenozinin C4 pozisyonunda mono-ikameli alkil aminin eklenmesi, aktivitede on kat artışa ve ayrıca etkinin dengelenmesi ile ilişkili alkilamin ikame edicisinin uzunluğuna yol açtı. Metilsülfaniletilamino grubunu C4 pozisyonuna ve trifloropropilsülfanilin zincir uzunluğuna eklenmesi, etkinliği arttırılmış ilaç kangrelorunun oluşumuna yol açar. Cangrelor, %10'dan daha az bir geri kazanıma sahip olan bileşik lC ile karşılaştırıldığında 20 dakika sonra sıçanda ADP'nin neden olduğu trombosit agregasyonunun ortalama %78'lik bir geri kazanımına sahiptir.
| bileşik | pIC50 | R1 | R2 | R3 |
|---|---|---|---|---|
| ATP | 3.6 | Ö | C | C-NH2 |
| 1 A | 3.5 | C | C-NH2 | |
| 1B | 8.6 | C-NH2 | ||
| 1C | 9.1 | |||
| kangrelor | 9.4 |
Tersine çevrilebilir oral ilaç tikagrelor ihtiyacını karşılamak için kangrelorun fosfat zinciri bir aspartik asit ile değiştirildi , bu da potenste 300 kat azalmaya neden oldu. Pürin triazolopirimidin ile değiştirilerek tikagrelorun potensi kangrelor ile aynı seviyeye getirildi. Glikosidik bağın olası kararsızlığını önlemek için şeker riboz birimi de bir siklopentil grubu ile değiştirildi . Yapının sol tarafındaki grup, yan halka R1 ile değiştirildi. Nötr yan zincir, R1 = CONH 2 ve R1 = CH 2 , OH afinitesi düşük bir kayıpla kabul edildi ve metabolizma kaymıştır olan safra için karaciğer metabolizması. Bu nedenle, farmakokinetik özelliklerin optimizasyonunu basitleştiren in vitro hepatik mikrozomal testler kullanılabilir. 5 konumunda fenil siklopropilamin ikamesinin eklenmesi, yüksek afiniteler verdi. Bu kaynaktan birinci bileşik ölçülebilir ağızdan sahip olduğu bulunmuştur biyolojik sıçanlarda (R1 CH = 2 OH). R2'nin varyasyon, örneğin R1, grupların izin giriş farmakokinetik özelliklerini artırmak için afinite üzerinde küçük bir etkisi vardı = OCH 2 CH 2 OH. De florin giriş fenil halkası ve daha geliştirilmiş metabolik stabilite için potansiyel alkil zinciri tiyoeter sonunda. Tioeter alkil zincirindeki florları S-propile geri değiştirerek tikagrelor formülasyonuna yol açar.
| bileşik | pIC50 | R1 | R2 | R3 | R4 | R5 |
|---|---|---|---|---|---|---|
| ATP | 3.6 | C | Ö | C-NH2 | C | |
| 2A | 7.0 | C | Ö | |||
| 2B | 9.3 | N | C | |||
| 2C | COOH = 9.3 CONH 2 = 7.7
CH 2 , OH 7.1 = |
COOH, CONH 2 veya
CH 2 , OH |
N | C | ||
| 2B | COOH=9.6
CONH 2 = 8.8 CH 2 , OH, 8.3 = H=8.6 OCH 2 , CH 2 , OH 8.5 = |
COOH, CONHz 2, CH 2 , OH, H ya da
OCH 2 , CH 2 , OH |
N | C | ||
| 2E | 9.2 | OCH 2 , CH 2 , OH | N | C | ||
| tikagrelor | 8.3 | OCH 2 , CH 2 , OH | N | C |
klinik kullanım
Trombositlerin aktivasyonu ve ardından trombositlerin agregasyonu, normal hemostazın korunmasında çok önemli bir role sahiptir . Bu sistemdeki bozukluk serebrovasküler , kardiyovasküler ve periferik vasküler hastalıklara yol açabilir ve burada felç, kararsız angina ve miyokard enfarktüsüne yol açabilir . Bir damar hasar gördüğünde, ADP hasarlı hücrelerden ve aktive trombositlerden salınır ve daha fazla trombosit agregasyonunu indükler.
tiklopidin
Birinci nesil tienopiridin P2Y 12 reseptör blokeri tiklopidin, trombotik trombositopenik purpura , aplastik anemi ve nötropeni gibi yüksek yan etki insidansının ardından klinik kullanımdan çekilmiştir . Klopidogrel, daha az gastrointestinal yan etkiye ve daha iyi hematolojik güvenliğe sahip olduğundan, ilacın klinik kullanımı klopidogrel tarafından hızla gölgede bırakıldı .
klopidogrel
İkinci nesil tienopiridin P2Y 12 reseptör bloker klopidogrel, iskemik serebrovasküler, kardiyak ve periferik arteriyel salınımın tedavisi için faydalı olan etkili bir trombosit önleyici maddedir. Diğer tienopiridin ilaçları gibi, ilaç da klinik kullanımda sıklıkla aspirin ile kombine edilmiştir. Klinik olarak onaylanmış klopidogrel dozu, 300 mg yükleme dozu PO ve günde 75 mg idame dozu PO'dur.
Uzun yıllar boyunca siklooksijenaz-1 (COX-1) inhibitörü aspirin ve klopidogrel ile ikili tedavi rutin bir uygulamaydı ve merkezi bir rol oynayan trombosit biyolojisini güçlü bir şekilde manipüle etme kabiliyetine sahip oldukları için trombotik olayların önlenmesi için ana antitrombosit ajanlar olarak hizmet ettiler. trombozun bir parçası. Bununla birlikte, bu ajanların kullanımı, artan kanama riskine maruz kalma , klopidogrel süresini ve dozajını çok önemli hale getirme gibi bir dizi önemli sınırlamaya tabidir. Ayrıca, klopidogrel'e yanıt tek tip değildir ve düşük yanıt, majör olumsuz kardiyovasküler olaylara yol açabilir .
Yeni nesiller
Yeni nesil P2Y 12 blokerleri, bu sorunları ele almayı amaçladı ve hastalar için sonuçlarda iyileşme vaat etti. Yakın zamanda geliştirilen bu P2Y 12 blokerleri (ticagrelor, kangrelor, prasugrel ve elinogrel), P2Y 12 reseptörünü daha verimli bir şekilde antagonize ederek trombositlerin daha tutarlı ve daha güçlü inhibisyonunu sağlar . Bununla birlikte, bu daha güçlü trombosit inhibisyonu, daha yüksek kanama riski pahasına gelir.
Üçüncü kuşak bir tienopiridin olan Prasugrel, vücutta klopidogrel ve tiklopidinden daha etkin bir şekilde metabolize olur ve bu nedenle trombosit aktivasyonunu daha fazla engeller. Çalışmalar, prasugrel'in stent trombozu ve miyokard enfarktüsü riskini klopidogrelden çok daha fazla azalttığını göstermiştir. Prasugrel'in klinik olarak onaylanmış dozu, 60 mg yükleme dozu PO ve günde 10 mg idame dozu PO'dur.
Tikagrelor, klopidogrelden çok daha güçlü bir trombosit agregasyonu inhibitörüdür, ancak hastalarda dispne ataklarının artmasıyla ilişkilidir. Bu ataklar hafif ila orta şiddette olabilir. Tikagrelorun onaylanmış klinik dozu, 180 mg yükleme dozu PO ve günde 90 mg idame dozudur.
Klinik kullanımda P2Y 12 reseptörünü hedefleyen tek ebeveyn ilacı cangrelordur.
Etkileşimler
CYP2C19 enzimi , klopidogrel kadar proton pompası inhibitörlerini (PPI) metabolize eder . Çeşitli raporlar, negatif bir klopidogrel-omeprazol ilaç etkileşimi olduğunu belirtmiştir . Bazı çalışmalar , bir proton pompası inhibitörü (PPI) olan omeprazol ile tedavi gören hastalarda trombositler üzerindeki klopidogrel aktivitesinin önemli ölçüde engellendiğini bulmuştur . Başka bir çalışma da lansoprazolün klopidogrel aktivitesi üzerinde engelleyici etkileri olduğunu gösterdi . Bununla birlikte, diğer çalışmalar, PPI'nin pantoprazol veya esomeprazol alımının klopidogrel'e verilen yanıtın bozulmasıyla ilişkili olmadığını göstermiştir.
2009'da Amerika Birleşik Devletleri gıda ve ilaç idaresi ( FDA ) ve Avrupa İlaç Ajansı (EMA), o sırada Initial Cohort Studies tarafından yapılan gözlemler nedeniyle klopidogrel ve ÜFE'lerin, özellikle omeprazolün kombinasyonunu önermedi. Bununla birlikte, daha yeni retrospektif kohort çalışmaları , klopidogrel-PPI etkileşimlerinin neden olduğu olumsuz kardiyovasküler olayları göstermemiştir. Bu nedenle, ilaç etkileşiminin mortalite üzerindeki etkisine dair kesin bir kanıt yoktur .
Gastrointestinal kanama riski yüksek olan hastalarda risk, olası olumsuz kardiyovasküler etkilerden daha ağır basmaktadır. Bu nedenle, bu hastalara klopidogrel ile pantoprazol gibi daha az CYP2C19 inhibe eden PPI'ları birleştirmeleri önerilmelidir.
Klopidogrel direnci
Klopidogrel direnci yıllar içinde ortaya çıkmış ve AKS'li veya PCI geçiren hastaların tedavisi için büyük bir endişe kaynağı olmuştur. Klopidogrel direncinin farklı popülasyonlar ve etnik gruplar arasında %4-44 arasında değiştiği bildirilmektedir . Klopidogrel direncine maruz kalan hastalar, klopidogrelin aktif metabolitinin azalmış seviyelerine bağlı olarak daha düşük trombosit inhibisyonu aktivitesi gösterirler. Bu, örneğin iskemik ve tromboembolik komplikasyonlar gibi bir dizi klinik olayla sonuçlanır. Bu hastalar zayıf veya yanıt vermeyen olarak kabul edilir.
Klopidogrel, aktif bir metabolit haline gelmesi için enzimlerin yardımıyla iki aşamalı bir metabolizasyona ihtiyaç duyan bir ön ilaçtır. Klopidogrel metabolizmasındaki önemli enzimlerden biri, biyotransformasyonun her iki aşamasında da yer alan CYP2C19'dur. CYP2C19 enziminin bir polimorfizmi, klopidogrel tepkisini etkiler, dolayısıyla enzimatik aktiviteyi azaltır ve dolayısıyla klopidogrelin aktif metabolitini azaltır.
Klopidogrel direncinin ana sorunu, diğer ilaçlarla, özellikle de proton pompa inhibitörü omeprazol ile etkileşimdir. Omeprazol ve klopidogrel, aynı CYP metabolik yolu ile metabolize edilir. Sonuç olarak, omeprazolün birlikte kullanımıyla klopidogrelin düşük yanıtlılığının, bu iki ilaç arasındaki CYP2C19 enziminin rekabetinden kaynaklandığı öne sürülmüştür.
Klopidogrel direncinin nasıl yenileceğine ilişkin klinik yaklaşımlar arasında daha yüksek dozlarda klopidogrel, fosfodiesteraz inhibitörü silostazol ile birlikte kullanım veya prasugrel ve tikagrelor gibi yeni bir antiplatelet ajana geçiş yer alır. Yine de, yukarıdaki bu yöntemlerle ilgili en büyük endişe, kanama riskinin artmasıdır. Bu nedenle, hızlı etki başlangıcı, bireyler arasında yanıtta daha az değişkenlik ve gelişmiş güvenlik profili olan yeni bir antiplatelet ajana duyulan ihtiyaç kritik öneme sahiptir.
Gelecek görünüşü
ADP inhibitörlerinin gelişimi sürekli olarak ilerlemektedir ve daha da iyi P2Y 12 antagonistleri arayışı halen devam etmektedir. AKS'li veya PCI uygulanan hastalarda aterotrombotik olayların ikincil önlenmesinin temel taşı, aspirin ve klopidogrel ile ikili antitrombosit tedavidir. Bununla birlikte, aterotromboz olayları hala meydana gelir. Mevcut antiplatelet ilaçların sınırlamaları, kanama riskini ve trombosit inhibitör yanıtının bireyler arası değişkenliğini içerir.
Amaç, kanama gibi güvenlik endişelerini azaltırken terapötik faydaları en üst düzeye çıkarmak için optimal terapötik pencereyi belirlemektir . Sonuç olarak, ADP inhibitörlerinin karşılanmayan ana hedefi, hızlı etki başlangıcı, yüksek düzeyde antiplatelet aktivitesi, ancak kanama riskini azaltan güçlü bir geri dönüşümlü antiplatelet ajan geliştirmektir. Günde bir kez oral profil ve optimize edilmiş hedef seçiciliği ile birlikte bu zorlu hedef, muhtemelen bu alanda önemli bir atılım olacaktır.
Vicagrel, Eylül 2017 itibariyle bu sektördeki en son gelişmedir. Klopidogrelin yeni bir asetat analoğu olup, geliştirilmiş antiplatelet etkinliği ve ayrıca kanama riskini azaltması beklenmektedir. Vicagrelin ön farmakokinetik çalışmaları, klopidogrelden daha yüksek bir biyoyararlanım göstermiştir ve bu da vicagrelin çok daha düşük terapötik etkili dozuna işaret etmektedir. Vicagrelin klopidogrel üzerindeki avantajları, CYP2C19'u zayıf metabolize edenlere karşı ilaca direnç göstermemesi, daha düşük etkili doz ve daha hızlı etki başlangıcı nedeniyle doza bağlı toksisitenin azalması olarak kabul edilir .