Potasyum ferrosiyanür - Potassium ferrocyanide

|
|
|
|

|
|
| İsimler | |
|---|---|
|
IUPAC adı
Potasyum hekzasiyanoferrat(II)
|
|
| Diğer isimler
(Sarı)
Potasyum Prusyatı, Potasyum hekzasiyanoferrat (II) trihidrat, Tetrapotasyum ferrosiyanür trihidrat, Ferrat hekzasiyano tetrapotasyum trihidrat |
|
| tanımlayıcılar | |
|
3B model ( JSmol )
|
|
| ECHA Bilgi Kartı |
100.034.279 |
| E numarası | E536 (asitlik düzenleyiciler, ...) |
|
PubChem Müşteri Kimliği
|
|
| ÜNİİ | |
|
CompTox Panosu ( EPA )
|
|
|
|
| Özellikler | |
| K 4 [Fe(CN) 6 ] | |
| Molar kütle | 368.35 g/mol (susuz) 422.388 g/mol (trihidrat) |
| Dış görünüş | Açık sarı, kristal granüller |
| Yoğunluk | 1.85 g / cm ' 3 (trihidrat) |
| Kaynama noktası | (çözünür) |
|
trihidrat 28.9 g/100 mL (20 °C) |
|
| çözünürlük | etanol , eter içinde çözünmez |
| -130,0 · 10 -6 cm 3 / mol | |
| Tehlikeler | |
| R cümleleri (modası geçmiş) | R32 , R52 , R53 |
| S-ifadeleri (modası geçmiş) | S50 (B), S61 |
| NFPA 704 (ateş elmas) | |
| Alevlenme noktası | Yanıcı değil |
| Ölümcül doz veya konsantrasyon (LD, LC): | |
|
LD 50 ( ortalama doz )
|
6400 mg/kg (oral, sıçan) |
| Bağıntılı bileşikler | |
|
Diğer anyonlar
|
potasyum ferrisiyanür |
|
Diğer katyonlar
|
Sodyum ferrosiyanür Prusya mavisi |
|
Aksi belirtilmedikçe, veriler standart durumdaki malzemeler için verilmiştir (25 °C [77 °F], 100 kPa'da). |
|
|
|
|
| Bilgi kutusu referansları | |
Potasyum ferrosiyanür , K 4 [Fe(CN) 6 ]·3H 2 O formülüne sahip inorganik bileşiktir . Koordinasyon kompleksinin [Fe(CN) 6 ] 4− potasyum tuzudur . Bu tuz limon sarısı monoklinik kristaller oluşturur .
sentez
1752'de Fransız kimyager Pierre Joseph Macquer (1718-1784) ilk olarak Prusya mavisini (demir(III) ferrosiyanür) potasyum hidroksit ile reaksiyona sokarak elde ettiği potasyum ferrosiyanürün hazırlanışını bildirdi .
Modern üretim
Potasyum ferrosiyanür endüstriyel olarak hidrojen siyanür , demir klorür ve kalsiyum hidroksitten üretilir , bunların kombinasyonu Ca 2 [Fe(CN) 6 ]·11H 2 O verir. Bu çözelti daha sonra karışık kalsiyum-potasyumun çökeltilmesi için potasyum tuzları ile işlenir. tuzu CaK 2 [Fe (CN) 6 sırayla ile muamele edilir], potasyum karbonat tetrapotasyum tuzu elde edildi.
Tarihsel üretim
Tarihsel olarak, bileşik azot, demir talaşları ve potasyum karbonat içeren organik bileşiklerden üretilmiştir. Yaygın nitrojen ve karbon kaynakları, korna boynuzu, deri hurdası, sakatat veya kurumuş kandı . Ayrıca ticari olarak gazhanelerde harcanan oksitten (şehir gazının hidrojen siyanürden saflaştırılması) elde edildi.
kimyasal reaksiyonlar
Potasyum ferrosiyanür tedavisi nitrik asit , H verir 2 [Fe (NO) (CN) 5 ]. Bu ara maddenin sodyum karbonat ile nötrleştirilmesinden sonra , kırmızı sodyum nitroprussid kristalleri seçici olarak kristalleştirilebilir.
Klor gazı ile işleme tabi tutulduğunda, potasyum ferrosiyanür potasyum ferrisiyanüre dönüşür :
- 2 K 4 [Fe(CN) 6 ] + Cl 2 → 2 K 3 [Fe(CN) 6 ] + 2 KCl
Bu reaksiyon, bir çözeltiden potasyum ferrosiyanürü çıkarmak için kullanılabilir.
Ünlü bir reaksiyon, Prusya mavisi vermek için demir tuzları ile muameleyi içerir . Fe bileşimi ileIII
4[FeII
( CN )
6]
3Bu çözünmez ama derinden renkli malzeme, ozalit baskının mavisidir .
Uygulamalar
Potasyum ferrosiyanür endüstride birçok niş uygulama bulur. O ve ilgili sodyum tuzu , hem yol tuzu hem de sofra tuzu için topaklanma önleyici maddeler olarak yaygın olarak kullanılmaktadır. Potasyum ve sodyum ferrosiyanürler ayrıca kalayın saflaştırılmasında ve bakırın molibden cevherlerinden ayrılmasında da kullanılır. Potasyum ferrosiyanür, şarap ve sitrik asit üretiminde kullanılır.
AB'de, ferrosiyanürler (E 535-538), 2017 itibariyle, tuz ikamesi olarak yalnızca iki gıda kategorisinde yetkilendirilmiştir. Böbrekler, ferrosiyanür toksisitesi için organdır.
Hayvan yemlerinde de kullanılabilir.
Laboratuvarda potasyum ferrosiyanür, redoks reaksiyonlarına dayalı titrasyonlarda sıklıkla kullanılan bir bileşik olan potasyum permanganat konsantrasyonunu belirlemek için kullanılır . Potasyum ferrosiyanür, X-Gal'i parçalamak için kullanılan beta-galaktosidaz için bir tampon sağlamak üzere potasyum ferrisiyanür ve fosfat tamponlu çözelti ile bir karışımda kullanılır ve bir antikorun (veya başka bir molekülün) Beta-'ya konjuge olduğu parlak mavi bir görselleştirme sağlar. gal, hedefine bağlandı. Fe(3) ile reaksiyona girdiğinde Prusya mavisi rengi verir. Bu nedenle laboratuvarlarda demir için tanımlayıcı bir reaktif olarak kullanılır.
Potasyum ferrosiyanür bitkiler için gübre olarak kullanılabilir.
MS 1900'den önce, Castner prosesinin icadından önce , potasyum ferrosiyanür, alkali metal siyanürlerin en önemli kaynağıydı . Bu tarihsel süreçte, potasyum ferrosiyanürün ayrıştırılmasıyla potasyum siyanür üretildi:
K 4 [Fe(CN) 6 ] → 4 KCN + FeC 2 + N 2
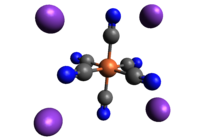
Yapı
Diğer metal siyanürler gibi, hem hidrat hem de susuz tuzlar olarak katı potasyum ferrosiyanür, karmaşık bir polimerik yapıya sahiptir. Polimer , CN ligandlarına bağlı K + iyonlarıyla çapraz bağlanmış oktahedral [Fe(CN) 6 ] 4− merkezlerinden oluşur . Katı suda çözündüğünde K + ---NC bağlantıları kopar.
toksisite
Potasyum ferrosiyanür toksik değildir ve vücutta siyanüre ayrışmaz. Sıçanlarda toksisite ile, düşük ölümcül bir doz (LD 50 6400 mg / kg).
Ayrıca bakınız
Referanslar
Dış bağlantılar
- "Siyanür (inorganik) bileşikleri bilgi formu" . Ulusal Kirletici Envanteri Avustralya.
- "Tuzdaki Potasyum Ferrosiyanür Tüketimi Tamamen Güvenlidir" . rediff.com .

