hidrazoik asit - Hydrazoic acid
|
|

|
|

|
|
| İsimler | |
|---|---|
|
IUPAC adı
hidrojen azid
|
|
| tanımlayıcılar | |
|
3B model ( JSmol )
|
|
| chebi | |
| CHEMBL | |
| Kimyasal Örümcek | |
| ECHA Bilgi Kartı |
100.029.059 |
|
PubChem Müşteri Kimliği
|
|
| ÜNİİ | |
|
CompTox Panosu ( EPA )
|
|
|
|
|
|
| Özellikler | |
| HN 3 | |
| Molar kütle | 43.03 g/mol |
| Dış görünüş | renksiz, çok uçucu sıvı |
| Yoğunluk | 1.09 g / cc 3. |
| Erime noktası | −80 °C (−112 °F; 193 K) |
| Kaynama noktası | 37 °C (99 °F; 310 K) |
| yüksek oranda çözünür | |
| çözünürlük | alkali , alkol , eter içinde çözünür |
| Asit (s K a ) | 4.6 |
| eşlenik taban | azid |
| Yapı | |
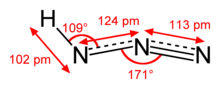
| yaklaşık olarak doğrusal | |
| Tehlikeler | |
| Ana tehlikeler | Son derece toksik, patlayıcı, reaktif |
| R cümleleri (modası geçmiş) | R3 , R27/28 |
| S-ifadeleri (modası geçmiş) | S33 , S36/37 , S38 |
| NFPA 704 (ateş elması) | |
| Bağıntılı bileşikler | |
|
Diğer katyonlar
|
Sodyum azid |
|
Amonyak Hidrazin |
|
|
Aksi belirtilmedikçe, veriler standart durumdaki malzemeler için verilmiştir (25 °C [77 °F], 100 kPa'da). |
|
|
|
|
| Bilgi kutusu referansları | |
Hidrazoik asit olarak da bilinen, hidrojen azid veya azoimide , kimyasal formül HN sahip bir bileşiktir 3 . Oda sıcaklığında ve basıncında renksiz, uçucu ve patlayıcı bir sıvıdır. Bir nitrojen ve hidrojen bileşiğidir ve bu nedenle bir pniktojen hidrittir . İlk olarak 1890'da Theodor Curtius tarafından izole edilmiştir . Asidin birkaç uygulaması vardır, ancak konjuge bazı olan azid iyonu özel işlemlerde faydalıdır.
Hidrazoik asit, diğer mineral asitleri gibi suda çözünür. Seyreltilmemiş hidrazoik asit, standart bir oluşum entalpisi Δ f H o (l, 298K) = +264 kJmol -1 ile tehlikeli bir şekilde patlayıcıdır . Seyreltildiğinde, gaz ve sulu çözeltiler (<%10) güvenle kullanılabilir.
Üretme
Asit genellikle sodyum azid gibi bir azid tuzunun asitleştirilmesiyle oluşturulur . Normalde sudaki sodyum azid çözeltileri, azid tuzu ile dengede olan eser miktarlarda hidrazoik asit içerir, ancak daha güçlü bir asidin eklenmesi, çözelti içindeki birincil türleri hidrazoik aside dönüştürebilir. Saf asit, daha sonra , hoş olmayan bir kokuya sahip, son derece patlayıcı renksiz bir sıvı olarak fraksiyonel damıtma yoluyla elde edilebilir .
- NaN 3 + HCl → HN 3 + NaCl
Sulu solüsyonu ayrıca baryum azid solüsyonunun seyreltik sülfürik asit ile işlenmesi , çözünmeyen baryum sülfatın filtre edilmesiyle de hazırlanabilir .
Başlangıçta sulu hidrazinin nitröz asit ile reaksiyonu ile hazırlanmıştır :
- N 2 H 4 + HNO 2 → HN 3 + 2 H 2 O
İle hidrazinyum katyon ( N
2H+
5) bu reaksiyon şu şekilde yazılır:
-
n
2H+
5+ HNO 2 → HN 3 + H 2 O + H 3 O +
Hidrojen peroksit , nitrosil klorür , trikloramin veya nitrik asit gibi diğer oksitleyici maddeler de hidrazinden hidrazoik asit üretmek için kullanılabilir.
Bertaraf edilmeden önce imha
Hidrazoik asit, nitröz asit ile reaksiyona girer:
- HN 3 + HNO 2 → N 2 O + N 2 + H 2 O
Bu reaksiyon, azotlu bileşikleri dört farklı oksidasyon durumunda içermesi bakımından olağandışıdır.
Azidler ayrıca asitleştirildiğinde sodyum nitrit ile ayrışır . Bu, atılmadan önce artık azidleri yok etme yöntemidir.
- 2 NaN 3 + 2 HNO 2 → 3 N 2 + 2 NO + 2 NaOH
Reaksiyonlar
Özelliklerinde hidrazoik asit, (suda) az çözünür kurşun, gümüş ve cıva(I) tuzları oluşturduğundan halojen asitlere bazı benzerlikler gösterir. Metalik tuzların tümü susuz formda kristalleşir ve ısıtıldığında ayrışır ve saf metal kalıntısı bırakır. Bu zayıf bir asit (p K bir = 4.75). Bu ağır metal tuzları patlayıcı ve kolayca etkileşim ile olan alkil iyodürler . Daha ağır alkali metallerin ( lityum hariç ) veya toprak alkali metallerin azidleri patlayıcı değildir, ancak ısıtıldığında daha kontrollü bir şekilde ayrışır ve spektroskopik olarak saf N açığa çıkarır.
2gaz. Hidrazoik asit solüsyonları (örneğin, bir çok metal çözünmesi çinko , demir denir hidrojen kurtuluşu ve tuzların oluşturulması ile) azidler (eski olarak da adlandırılır azoimides veya hydrazoates).
Hidrazoik asit, aldehitler, ketonlar ve karboksilik asitler dahil olmak üzere karbonil türevleri ile reaksiyona girerek nitrojen çıkışı ile bir amin veya amid verebilir. Buna Schmidt reaksiyonu veya Schmidt yeniden düzenlemesi denir .
En güçlü asitlerde çözünme, H içeren patlayıcı tuzlar üretir.
2N=N=N+
iyon, örneğin:
-
HN=N=N + HSbCl
6→ [H
2N=N=N]+
[SbCl
6]-
iyon H
2N=N=N+
olduğu izoelektronik için diazometanı .
Şok, sürtünme, kıvılcım vb. tarafından tetiklenen hidrazoik asidin ayrışması aşağıdaki gibidir:
- 2 HN
3→ H
2+ 3 N
2
Hidrazoik asit, yeterli enerjide tek moleküllü ayrışmaya uğrar:
-
HN
3→ NH + N
2
En düşük enerji yolu , üçlü halde NH üretir ve bu da onu spin-yasak bir reaksiyon haline getirir. Bu, lazer fotoayrışma çalışmalarıyla zemin elektronik durumundaki belirli miktarlarda titreşim enerjisi için hızı belirlenen birkaç reaksiyondan biridir. Ek olarak, bu tek moleküllü oranlar teorik olarak analiz edilmiştir ve deneysel ve hesaplanan oranlar makul bir uyum içindedir.
toksisite
Hidrazoik asit uçucudur ve oldukça zehirlidir. Keskin bir kokusu vardır ve buharı şiddetli baş ağrılarına neden olabilir . Bileşik, kümülatif olmayan bir zehir görevi görür.
Uygulamalar
2-Furonitrile , bir ilaç ara ve potansiyel yapay tatlandırıcı maddedir muamele edilmesi suretiyle iyi verimde hazırlanmıştır furfuralin bir hidrazoik asit karışımı (HN ile 3 ) ve perklorik asit magnezyum perklorat varlığında benzen 35 çözelti ° C.
Tüm gaz fazı iyot lazer (AGIL) ile gaz hidrazoik asit karışımları klor heyecan üretilmesi için azot klorid daha sonra neden olmak için kullanıldığı, iyot lase için; bu, COIL lazerlerinin sıvı kimyası gerekliliklerini ortadan kaldırır .
Referanslar
Dış bağlantılar
-
 İlgili Medya Hidrojen azid Wikimedia Commons
İlgili Medya Hidrojen azid Wikimedia Commons - OSHA: Hidrazoik Asit



