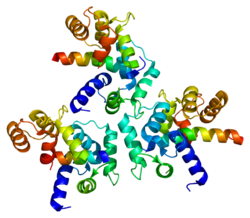
Ca v 1.3 -Cav1.3
Gerilime-bağlı kalsiyum kanalı, L tipi, alfa 1D alt birimi (aynı zamanda , Ca v 1.3 ) a, proteinin insanlarda tarafından kodlandığını CACNA1D geni. Ca v 1.3 kanalları , L tipi kalsiyum akımları oluşturan ve dihidropiridinler (DHP) tarafından seçici inhibisyona duyarlı olan Ca v 1 ailesine aittir .
Yapı ve işlev
Voltaj bağımlı kalsiyum kanalları (VDCC), kalsiyum iyonlarına seçici olarak geçirgendir ve bu iyonların uyarılabilir hücrelerin içine ve dışına hareketine aracılık eder. Dinlenme potansiyelinde bu kanallar kapalıdır, ancak zar potansiyeli depolarize olduğunda bu kanallar açılır. Kalsiyum iyonlarının hücreye akışı, kas kasılması , gen ekspresyonu ve salgılanması dahil olmak üzere sayısız kalsiyum bağımlı süreci başlatabilir . Kalsiyuma bağımlı süreçler, örneğin kalsiyum pompaları tarafından gerçekleştirilebilen hücre içi kalsiyum seviyelerinin düşürülmesiyle durdurulabilir .
Voltaj bağımlı kalsiyum kanalları, α1, β, α2δ ve γ alt birimlerinden oluşan çoklu proteinlerdir. Ana alt birim, VDCC'lerin seçicilik gözenekini, voltaj sensörünü ve geçitleme aparatını oluşturan α1'dir. C v 1.3 kanallarında α1 alt birimi α1D'dir. Bu alt birim, Ca v 1.3 kanallarını , bir α1C alt birimine sahip baskın ve daha iyi çalışılmış Ca v 1.2 gibi Ca v 1 ailesinin diğer üyelerinden ayırır. α1 alt biriminin önemi, aynı zamanda, dihidropiridinler gibi kalsiyum kanal blokerleri için birincil hedef olduğu anlamına gelir . Kalan β, α2δ ve γ alt birimlerinin yardımcı işlevleri vardır.
α1 alt birimi , her biri altı transmembran segmenti olan dört homolog alana sahiptir . Her homolog alan içinde, dördüncü transmembran segmenti (S4), diğer beş hidrofobik segmentin aksine pozitif olarak yüklenir . Bu özellik, S4'ün voltaj sensörü olarak işlev görmesini sağlar. Alfa-1D alt birimleri , L tipi kalsiyum akımları ile karakterize edilen Ca v 1 ailesine aittir . Özellikle, a1D alt birimleri , koklea iç tüy hücrelerinde nörotransmiter salınımı gibi belirli fizyolojik işlevler için ideal olan düşük voltajlı aktivasyon ve yavaş yavaş Ca2 + akımlarını etkisiz hale getiren sağlar .
Ca v 1.3 kanallarının biyofiziksel özellikleri, hem aktivasyonun voltaj bağımlılığını hem de Ca2 +'ya bağlı inaktivasyonu etkileyen bir C-terminal modülatör alanı (CTM) tarafından yakından düzenlenir . Ca v 1.3, DHP için düşük bir afiniteye sahiptir ve eşik altı membran potansiyellerinde aktive olur, bu da onları kalp pili yapımında bir rol için ideal hale getirir .
Düzenleme
alternatif ekleme
C v 1.3'ün transkripsiyon sonrası alternatif eklenmesi , kapsamlı ve hayati bir düzenleyici mekanizmadır. Alternatif ekleme, kanalın geçit özelliklerini önemli ölçüde etkileyebilir. Fonksiyonel özgüllük kazandıran C v 1.2 transkriptlerinin alternatif eklenmesiyle karşılaştırıldığında, özellikle C-terminalinde alternatif eklemenin C v 1.3'ün farmakolojik özelliklerini etkilediği yakın zamanda keşfedilmiştir . Çarpıcı bir şekilde, alternatif olarak eklenmiş izoformlar arasında dihidropiridin duyarlılığında 8 kata kadar farklılıklar bildirilmiştir.
Olumsuz geribildirim
Ca v 1.3 kanalları, Ca2 + homeostazını sağlamak için negatif geri besleme ile düzenlenir . Kalsiyum iyonları, hücre içi sinyal iletimine özgü kritik bir ikinci habercidir . Hücre dışı kalsiyum seviyelerinin, hücre içi seviyelerden 12000 kat daha fazla olduğu tahmin edilmektedir. Kalsiyum bağımlı süreçler sırasında, hücre içi kalsiyum seviyesi 100 kata kadar yükselir. Bu kalsiyum gradyanını düzenlemek hayati derecede önemlidir, çünkü yüksek kalsiyum seviyeleri hücre için toksiktir ve apoptozu indükleyebilir .
Ca2 +'ya bağlı kalmodulin (CaM), kalsiyuma bağlı inaktivasyonu (CDI) indüklemek için Ca v 1.3 ile etkileşime girer . Son zamanlarda, CDI için Ca v 1.3 transkriptlerinin RNA düzenlemesinin gerekli olduğu gösterilmiştir . Beklenenin aksine, RNA düzenlemesi sadece CaM'nin bağlanmasını hafifletmez, ancak Ca2 + içermeyen kalmodulin'in (apoCaM) kanallara ön bağlanmasını zayıflatır . Sonuç olarak, CDI, CaM seviyelerindeki değişikliklerle sürekli olarak ayarlanabilir.
Klinik önemi
İşitme
Ca v 1.3 kanalları insanlarda yaygın olarak ifade edilir. Özellikle, ekspresyonları koklea iç tüy hücrelerinde (IHC'ler) baskındır. Ca v 1.3, normal IHC gelişimi ve sinaptik iletim için gerekli olduğu yama kelepçesi deneyleriyle gösterilmiştir . Bu nedenle, uygun işitme için Ca v 1.3 gereklidir.
kromaffin hücreleri
Ca v 1.3, kromaffin hücrelerinde yoğun olarak eksprese edilir . Bu kanalların düşük voltaj aktivasyonu ve yavaş inaktivasyonu, onları bu hücrelerde uyarılabilirliği kontrol etmek için ideal hale getirir. Kromaffin hücrelerinden katekolamin salgılanması, Ca v 1.3 ile ilişkili L tipi akımlara özellikle duyarlıdır . Katekolaminlerin birden fazla organ üzerinde birçok sistemik etkisi vardır. Ayrıca bu hücrelerde ekzositozdan L tipi kanallar sorumludur.
nörodejenerasyon
Parkinson hastalığı , orta beynin substantia nigra bölgesindeki dopamin üreten hücrelerin ölümünün , belki de en iyi şekilde titreme ile karakterize edilen motor fonksiyon bozukluğuna yol açtığı ikinci en yaygın nörodejeneratif hastalıktır . Son kanıtlar, L-tipi Ca v 1.3 Ca2 + kanallarının Parkinson hastalığı olan hastalarda dopaminerjik nöronların ölümüne katkıda bulunduğunu göstermektedir. Bu nöronların bazal aktivitesi ayrıca Ca v 1.3 gibi L tipi Ca2 + kanallarına da bağlıdır . Sürekli kalp pili aktivitesi, dopaminerjik substantia nigra nöronlarını ölümlerine katkıda bulunan stres faktörlerine karşı savunmasız hale getiren kalıcı hücre içi dendritik ve somatik kalsiyum geçişlerini harekete geçirir . Bu nedenle L-tipi kanalların, özellikle C v 1.3'ün inhibisyonu, bazı hayvan modellerinde Parkinson patogenezine karşı koruyucudur. Erken Parkinson hastalarında bu hipotezi test eden bir klinik faz III denemesi ( STEADY-PD III ), Parkinson'un ilerlemesini yavaşlatmada etkinlik gösteremedi.
Ca v 1.3'ün inhibisyonu , dihidropiridinler (DHP'ler) gibi kalsiyum kanal blokerleri kullanılarak gerçekleştirilebilir . Bu ilaçlar on yıllardır arteriyel hipertansiyon ve anjina tedavisinde kullanılmaktadır. Bunun nedeni , arteriyel düz kastaki Ca v 1.2 L-tipi kalsiyum kanallarının inhibisyonunun aracılık ettiği güçlü vazorelaksan özellikleridir . Bu nedenle, beyinde Ca v 1.3 kanalını inhibe etmek için DHP'ler kullanıldığında hipotansif reaksiyonlar (ve bacak ödemi), doz sınırlayıcı yan etkiler olarak kabul edilir . Bu sorun karşısında, seçici C v 1.3 kanal blokerlerini keşfetmeye yönelik girişimlerde bulunulmuştur . Bir adayın, Ca v 1.3'ün güçlü ve oldukça seçici bir inhibitörü olduğu iddia edilmiştir . Bu bileşik, 1-(3-klorofenetil)-3-siklopentilpirimidin-2,4,6-( 1H , 3H , 5H )-trione bu nedenle Parkinson'un gelecekteki tedavisi için bir aday olarak öne sürülmüştür. Bununla birlikte, seçiciliği ve gücü, diğer iki gruptan iki bağımsız çalışmada doğrulanamadı. Hatta bunlardan biri, bu ilaç tarafından indüklenen ve bloke edici etkilerden ziyade kanal aktivasyonunu gösteren geçiş değişiklikleri bildirdi.
Prostat kanseri
İmmün boyama deneylerinden elde edilen son kanıtlar, CACNA1D'nin iyi huylu prostat dokularına kıyasla prostat kanserlerinde yüksek oranda eksprese edildiğini göstermektedir. L tipi kanallarını bloke edilmesi ya da gen ekspresyonunun aşağı vurma arasında CACNA1D prostat kanseri hücrelerinin anlamlı ölçüde hücre büyümesi. Bu ilişkinin, yüksek α1D protein seviyeleri ile prostat kanseri arasında nedensel bir bağlantıyı temsil etmediğini bilmek önemlidir. CACNA1D geninin aşırı ekspresyonunun prostat kanseri hücre büyümesindeki rolünü araştırmak için daha fazla araştırmaya ihtiyaç vardır .
aldosteronizm
Kanalın gözenek oluşturucu α1-alt biriminin ( CACNA1D) aktivasyon kapısı içindeki korunan bölgelerdeki de novo somatik mutasyonlar , aldosteron üreten adenomlarda (APA) aşırı aldosteron üretimine neden olarak, tedaviye dirençli arteriyel hipertansiyona neden olan birincil aldosteronizm ile sonuçlanır . Bu mutasyonlar , Cav1.3 yoluyla artan Ca2 + girişine izin verir ve bu da Ca2 +'ya bağımlı aldosteron üretimini tetikler . Doğrulanmış APA mutasyonlarının sayısı sürekli artmaktadır. Nadir durumlarda, APA mutasyonları , otizm spektrum bozukluğu dahil olmak üzere farklı şiddette nörogelişimsel bozuklukları olan bireylerde germ hattı mutasyonları olarak da bulunmuştur .
Ayrıca bakınız
Referanslar
daha fazla okuma
- Williams ME, Feldman DH, McCue AF, Brenner R, Velicelebi G, Ellis SB, Harpold MM (Ocak 1992). "Yeni bir insan nöronal kalsiyum kanalı alt tipinin alfa 1, alfa 2 ve beta alt birimlerinin yapısı ve fonksiyonel ifadesi". Nöron . 8 (1): 71–84. doi : 10.1016/0896-6273(92)90109-Q . PMID 1309651 . S2CID 39341712 .
- Seino S, Chen L, Seino M, Blondel O, Takeda J, Johnson JH, Bell GI (Ocak 1992). "Pankreas beta hücrelerinde ifade edilen voltaja bağlı bir kalsiyum kanalının alfa 1 alt biriminin klonlanması" . Amerika Birleşik Devletleri Ulusal Bilimler Akademisi Bildirileri . 89 (2): 584–8. Bibcode : 1992PNAS...89..584S . doi : 10.1073/pnas.89.2.584 . PMC 48283 . PMID 1309948 .
- Seino S, Yamada Y, Espinosa R, Le Beau MM, Bell GI (Ağustos 1992). "Nöroendokrin/beyin tipi kalsiyum kanalının (CACNL1A2) alfa 1 alt birimini kodlayan genin insan kromozomu 3, bant p14.3'e atanması". genomik . 13 (4): 1375–7. doi : 10.1016/0888-7543(92)90078-7 . PMID 1324226 .
- Chin HM, Kozak CA, Kim HL, Mock B, McBride OW (Aralık 1991). "Bir beyin L tipi kalsiyum kanalı alfa 1 alt birim geni (CCHL1A2), fare kromozomu 14 ve insan kromozomu 3'e eşlenir" . Genomik (Gönderilen makale). 11 (4): 914–9. doi : 10.1016/0888-7543(91)90014-6 . PMID 1664412 .
- Mori Y, Friedrich T, Kim MS, Mikami A, Nakai J, Ruth P, Bosse E, Hofmann F, Flockerzi V, Furuichi T (Nisan 1991). "Bir beyin kalsiyum kanalının tamamlayıcı DNA'sından birincil yapı ve fonksiyonel ifade". Doğa . 350 (6317): 398-402. Bibcode : 1991Natur.350..398M . doi : 10.1038/350398a0 . PMID 1849233 . S2CID 4370532 .
- Yamada Y, Masuda K, Li Q, Ihara Y, Kubota A, Miura T, Nakamura K, Fujii Y, Seino S, Seino Y (Mayıs 1995). "İnsan kalsiyum kanalı alfa 1 alt birimi (CACNL1A2) ve beta alt birimi (CACNLB3) genlerinin yapıları". genomik . 27 (2): 312–9. doi : 10.1006/geno.1995.1048 . PMID 7557998 .
- Puro DG, Hwang JJ, Kwon OJ, Chin H (Nisan 1996). "İnsan retina Müller (glial) hücreleri tarafından ifade edilen bir L-tipi kalsiyum kanalının karakterizasyonu" . Beyin Araştırması. Moleküler Beyin Araştırması (Gönderilen makale). 37 (1–2): 41–8. doi : 10.1016/0169-328X(96)80478-5 . PMID 8738134 .
- Yang SN, Larsson O, Bränström R, Bertorello AM, Leibiger B, Leibiger IB, Moede T, Köhler M, Meister B, Berggren PO (Ağustos 1999). "Syntaksin 1, pankreas beta hücrelerinde voltaj kapılı Ca(2+) kanallarının L(D) alt tipi ile etkileşime girer" . Amerika Birleşik Devletleri Ulusal Bilimler Akademisi Bildirileri . 96 (18): 10164–9. doi : 10.1073/pnas.96.18.10164 . PMC 17860 . PMID 10468580 .
- Bell DC, Butcher AJ, Berrow NS, Page KM, Brust PF, Nesterova A, Stauderman KA, Seabrook GR, Nürnberg B, Dolphin AC (Şubat 2001). "Biyofiziksel özellikler, farmakoloji ve insan, nöronal L-tipi (alfa(1D), Ca(V)1.3) voltaja bağlı kalsiyum akımlarının modülasyonu". Nörofizyoloji Dergisi . 85 (2): 816–27. doi : 10.1152/jn.2001.85.2.816 . PMID 11160515 .
- Rosenthal R, Thieme H, Strauss O (Nisan 2001). "Beyin nöronlarında ve retina pigment epitel hücrelerinde fibroblast büyüme faktörü reseptörü 2 (FGFR2), nöroendokrin L-tipi kanalların (Ca(v)1.3) uyarılması yoluyla hareket eder". FASEB Dergisi . 15 (6): 970–7. doi : 10.1096/fj.00-0188com . PMID 11292657 .
- Davare MA, Avdonin V, Hall DD, Peden EM, Burette A, Weinberg RJ, Horne MC, Hoshi T, Hell JW (Temmuz 2001). "Ca2+ kanalı Cav1.2 ile birleştirilmiş bir beta2 adrenerjik reseptör sinyal kompleksi". Bilim . 293 (5527): 98-101. doi : 10.1126/science.293.5527.98 . PMID 11441182 .
- Namkung Y, Skrypnyk N, Jeong MJ, Lee T, Lee MS, Kim HL, Chin H, Suh PG, Kim SS, Shin HS (Ekim 2001). "Doğum sonrası pankreas beta hücre oluşumunda L-tipi Ca(2+) kanal alfa (1D) alt birimi için gereksinim" . Klinik Araştırma Dergisi . 108 (7): 1015–22. doi : 10.1172/JCI13310 . PMC 200955 . PMID 11581302 .
- Stokes L, Gordon J, Grafton G (Mayıs 2004). "İnsan T hücrelerinde voltaj kapılı olmayan L-tipi Ca2+ kanalları: ana alfa gözenek oluşturucu ve yardımcı beta alt birimlerinin farmakolojisi ve moleküler karakterizasyonu" . Biyolojik Kimya Dergisi . 279 (19): 19566-73. doi : 10.1074/jbc.M401481200 . PMID 14981074 .
- Qu Y, Baroudi G, Yue Y, Boutjdir M (Haziran 2005). "Otoimmün ile ilişkili sinüs bradikardisinde alfa1D (Cav1.3) L tipi kalsiyum kanalını içeren yeni moleküler mekanizma" . dolaşım . 111 (23): 3034–41. doi : 10.1161/CIRCULATIONAHA.104.517326 . PMID 15939813 .
- Baroudi G, Qu Y, Ramazan O, Chahine M, Boutjdir M (Ekim 2006). "Protein kinaz C aktivasyonu, NH2-terminal serin 81 fosforilasyon bölgesinde Cav1.3 kalsiyum kanalını inhibe eder". Amerikan Fizyoloji Dergisi. Kalp ve Dolaşım Fizyolojisi . 291 (4): H1614-22. doi : 10.1152/ajpheart.00095.2006 . PMID 16973824 .
- Olsen JV, Blagoev B, Gnad F, Macek B, Kumar C, Mortensen P, Mann M (Kasım 2006). "Sinyal ağlarında küresel, in vivo ve siteye özgü fosforilasyon dinamikleri" . Hücre . 127 (3): 635–48. doi : 10.1016/j.cell.2006.09.026 . PMID 17081983 . S2CID 7827573 .
Dış bağlantılar
- CACNA1D+protein,+insan ABD Ulusal Tıp Kütüphanesinde Tıbbi Konu Başlıkları (MeSH)
- Bulunan tüm yapısal bilgi genel PDB için Uniprot : Q01668 de (Voltaj bağımlı L-tipi kalsiyum kanalı alt-birimi, alfa-1D) PDBe-KB .
Bu makale , kamu malı olan Amerika Birleşik Devletleri Ulusal Tıp Kütüphanesinden alınan metinleri içermektedir .