Barton–McCombie oksijensizleştirme - Barton–McCombie deoxygenation
| Barton-McCombie deoksijenasyonu | |
|---|---|
| Adı üstünde |
Derek Harold Richard Barton Stuart W. McCombie |
| Reaksiyon tipi | Organik redoks reaksiyonu |
| tanımlayıcılar | |
| Organik Kimya Portalı | barton-mccombie-tepki |
| RSC ontoloji kimliği | RXNO:0000134 |
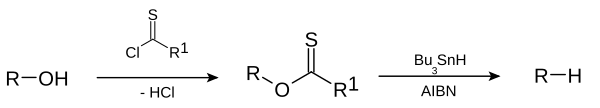
, Barton-McCombie deoksijenasyon bir bir organik reaksiyon , içindeki hidroksi fonksiyonel grup , bir in organik bir bileşiğin , bir ile değiştirildiği , hidrojen , bir vermek üzere bir alkil grubunu . Adını İngiliz kimyagerler Sir Derek Harold Richard Barton ve Stuart W. McCombie'den almıştır.
Bu oksijensizleştirme reaksiyonu bir radikal ikamesidir . İlgili Barton dekarboksilasyonunda reaktant bir karboksilik asittir .
mekanizma
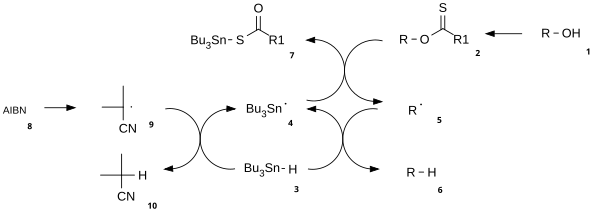
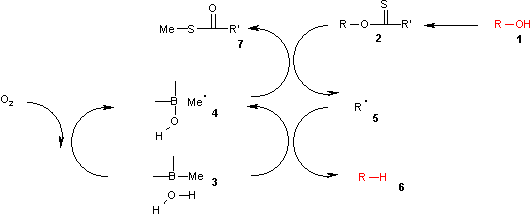
Reaksiyon mekanizması katalitik radikal başlatma adımı ve bir yayılma adım oluşur. Alkol ( 1 ) birinci ara ürün, örneğin bir bir reaktif karbonotiyoil dönüştürülür thionoester veya ksantat 2 . Isıtılmasını AIBN iki 2-siyanoprop-2-il radikalleri üreten onun homolitik yarılması sonuçları 9 her soyut bir proton tribütilstannan 3 tributilstanil oluşturmak için radikalleri 4 ve aktif olmayan 10 . Tribütilkalay radikali, CS π bağının eş zamanlı homolitik bölünmesi ile kükürt atomuna 4 saldırısıyla ksantat grubunu 2'den soyutlar. Bu, RO σ bağının homolitik bölünmesi yoluyla bir CO π bağı oluşturan ve alkil radikali 5 ve tributiltin ksantat 7 veren bir karbon merkezli radikal bırakır . Kükürt kalay , bu bileşikte bağ çok kararlıdır ve içerir itici güç Bu reaksiyon için. Alkil radikali 5 daha sonra istenen oksijeni giderilmiş ürünü ( 6 ) ve yayılmaya hazır yeni bir radikal türünü üreten yeni bir tribütilstanan molekülünden bir hidrojen atomu soyutlar .
Varyasyonlar
Alternatif hidrojen kaynakları
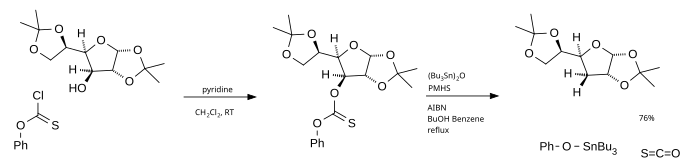
Bu reaksiyonun ana dezavantajı, toksik, pahalı ve reaksiyon karışımından çıkarılması zor olan tributilstannanın kullanılmasıdır. Bir alternatif, radikal kaynağı olarak tributiltin oksit ve hidrojen kaynağı olarak poli(metilhidridiloksan) (PMHS) kullanılmasıdır . Başlangıç materyali olarak kullanılan fenil klorotiyonoformat nihai olarak karbonil sülfür üretir .
trialkil boranlar
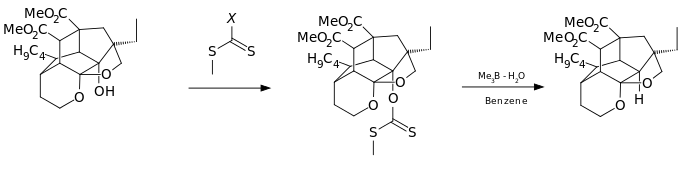
Daha da uygun bir hidrojen donörü, az miktarda su ile kirlenmiş trimetilboran gibi trialkilboran- su kompleksleri ile sağlanır.
Bu katalitik döngüde reaksiyon, trialkilboranın 3 hava ile metil radikaline 4 hava oksidasyonu ile başlatılır . Bu radikal, ksantat 2 ila S-metil-S-metil ditiokarbonat 7 ve radikal ara madde 5 ile reaksiyona girer . (CH 3 ) 3 B.H 2 O karmaşık 3 alkana bu radikal ile rekombine sağlayan bir hidrojen 6 dietil borinik asit ve radikal bir yeni metil geride bırakarak.
Tarafından bulunan teorik hesaplamalar bir OH olduğu homolizi boran-su kompleksi içinde reaksiyon , endotermik tribütilstannan içinde homolizi reaksiyona benzer bir enerji ile, ancak çok daha saf suyun homolizi reaksiyonundan daha düşük.
Kapsam
Bu reaksiyonun bir varyasyonu , azadirachtin'in toplam sentezindeki adımlardan biri olarak kullanıldı :
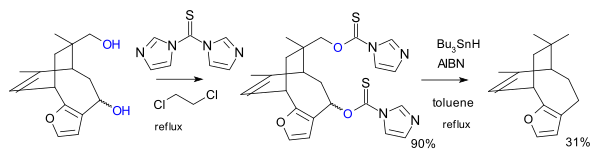
Başka bir varyasyonda reaktif, örneğin pallescensin B'nin toplam sentezinde imidazol 1,1'-tiokarbonildiimidazoldür (TCDI). aromatik altılıda.
Reaksiyon ayrıca S- alkilksantatlar için de geçerlidir . Yeni bir metal içermeyen reaktif olarak trietilboran ile , gerekli hidrojen atomları protik çözücülerden, reaktör duvarından ve hatta (kesinlikle susuz koşullarda) boranın kendisinden soyutlanır.