Genel anestezik etki teorileri - Theories of general anaesthetic action
Bir genel anestezi (ya da anestetik ) a, ilaç bir tersinir kaybına neden olmaktadır bilinç . Bu ilaçlar, ameliyatı kolaylaştırmak için genel anesteziyi indüklemek veya sürdürmek için genellikle bir anestezist/ anestezi uzmanı tarafından uygulanır .
Genel anestezikler, Crawford Long'un bir hastaya ilk kez dietil eter verdiği ve ağrısız bir operasyon gerçekleştirdiği 1842'den beri cerrahide yaygın olarak kullanılmaktadır . Genel anesteziklerin etkilerini (analjezi, amnezi, hareketsizlik) nöronal membrandaki membran proteinlerinin aktivitesini modüle ederek gösterdiğine uzun zamandır inanılmaktadır. Bununla birlikte, bu alanda çok fazla araştırma yapılmış olmasına rağmen, bu eylemin tam yeri ve mekanizması hala büyük ölçüde bilinmemektedir. Anestetik eylemi açıklamaya çalışan hem eski hem de modern bir dizi teori var.
İlk olarak Paul Ehrlich tarafından tanıtılan reseptörler ve ilaçlar arasındaki spesifik etkileşimler kavramı, ilaçların yalnızca hedeflerine (reseptörlere) bağlı olduklarında etki ettiğini belirtir. Bununla birlikte, bu kavram genel anestezikler için geçerli görünmüyor çünkü:
- Yaygın tıpta kullanılan genel anestezikler moleküler yapıları belirgin bir yapı-aktivite ilişkisi (yaygın tıpta kullanılan genel anestezikler yapılarını bkz olduğu çok basit ve farklı şekilde tanımlanır: - 1 etanol , 2 - kloroform , 3 - dietil eter , 4 - fluroksen , 5 - halotan , 6 - metoksifluran , 7 - enfluran , 8 - izofluran , 9 - desfluran , 10 - sevofluran )
- Çoğu genel anestezik, diğer ilaçların çoğundan çok daha yüksek konsantrasyonlarda hareket eden hedeflerine karşı oldukça zayıf afiniteye sahiptir, bu nedenle çeşitli yan etkiler kaçınılmazdır.
Genel anesteziklerin tüm bu ortak özellikleri, ilk araştırmacıların genel anesteziklerin belirli bir şekilde hareket ettiğine inanmalarını zorlaştırdı ve nöronal membran üzerindeki etkilerinin, spesifik bölgelerden ziyade (MSS nöronlarının lipid membranının spesifik olmayan pertürbasyonu yoluyla) küresel olduğu düşünüldü. .
Lipid çözünürlüğü-anestetik potens korelasyonu (Meyer-Overton korelasyonu)
Genel anestezik etkinin spesifik olmayan mekanizması ilk olarak 1847'de Von Bibra ve Harless tarafından önerildi. Genel anesteziklerin beyin hücrelerinin yağlı fraksiyonunda çözünerek ve yağlı bileşenleri onlardan uzaklaştırarak, böylece beyin hücrelerinin aktivitesini değiştirerek ve anesteziyi indükleyerek etki edebileceğini öne sürdüler. . 1899'da Hans Horst Meyer , "Zur Theorie der Alkoholnarkose" başlıklı makalesinde anestezik etkinin lipid çözünürlüğü ile ilişkili olduğu gerçeğinin ilk deneysel kanıtını yayınladı. İki yıl sonra benzer bir teori Overton tarafından bağımsız olarak yayınlandı.
Meyer , iribaşlarda anesteziyi indüklemek için gereken molar konsantrasyonun karşılığı olarak tanımlanan birçok ajanın potensini, zeytinyağı/su bölme katsayısı ile karşılaştırdı . Alkoller , aldehitler , ketonlar , eterler ve esterler gibi birçok anestezik molekül türü için potens ve bölme katsayısı arasında neredeyse doğrusal bir ilişki buldu . Hayvanlar (EC bir popülasyonun% 50'si anestezi indüklemek için gerekli olan anestetik konsantrasyonu 50 ) anestetik, yani, gaz ve sulu fazın teslim sağlayan araçların bağımsızdır.
Meyer ve Overton , genel anestezik moleküllerin fiziksel özellikleri ile güçleri arasındaki çarpıcı ilişkiyi keşfettiler: Bileşiğin zeytinyağındaki lipid çözünürlüğü ne kadar büyükse, anestezik gücü de o kadar büyük olur. Bu korelasyon, yağ fazı olarak zeytinyağı kullanılıyorsa, 4-5 derecenin üzerinde değişen lipit çözünürlüklerine sahip çok çeşitli anestezikler için geçerlidir. Bununla birlikte, bu korelasyon, "yağ" fazı olarak toplu oktanol veya tamamen hidratlanmış sıvı lipid çift tabakası kullanılırsa, hem korelasyonun kalitesi hem de artan anestezik aralığı açısından önemli ölçüde geliştirilebilir. Uçucu anesteziklerin etkilerinde katkı maddesi olduğu da kaydedilmiştir (iki farklı volatil anestetikten oluşan yarım doz bir karışım, her iki ilacın tek başına tam dozu ile aynı anestezik etkiyi vermiştir).
Genel anestezik etkinin modası geçmiş lipid hipotezleri

Lipid çözünürlüğü ve anestezi gücü arasındaki korelasyondan hem Meyer hem de Overton, üniter bir genel anestezi mekanizması tahmin etmişti. Nöronun lipid çift tabakasında lipofilik genel anesteziğin çözünmesinin, kritik anestezik konsantrasyonuna ulaşıldığında arızalanmasına ve anestezik etkisine neden olduğunu varsaydılar. Daha sonra 1973'te Miller ve Smith, lipid çift katmanlı genişleme hipotezi olarak da adlandırılan kritik hacim hipotezini önerdiler. Hacim yer değiştirmesi nedeniyle nöronal lipid membranın hidrofobik (veya lipofilik) bölgeleri içinde hacimli ve hidrofobik anestezik moleküllerin birikerek bozulmasına ve genişlemesine (kalınlaşmasına) neden olduğunu varsaydılar. Kritik miktarda anestezik birikimi, membran iyon kanallarının işlevini tersine çevirmeye yetecek kadar membran kalınlaşmasına neden olarak anestezik etki sağlar. Anestezik maddenin gerçek kimyasal yapısı kendi başına önemli değildir, ancak moleküler hacmi ana rolü oynar: membran içinde anestezik ne kadar fazla yer kaplarsa - anestezik etki o kadar büyük olur. Bu teoriye dayanarak, 1954'te Mullins, anestezik moleküllerin moleküler hacimleri hesaba katılırsa, potens ile Meyer-Overton korelasyonunun geliştirilebileceğini öne sürdü. Bu teori 60 yılı aşkın bir süredir var olmuştur ve atmosferik basınçtaki ters anestetik etkideki ( basıncı tersine çevirme etkisi ) artışların deneysel gerçeğiyle desteklenmiştir .
Daha sonra, genel anesteziklerin çeşitli kimyasal doğasını hesaba katan ve anestezik etkinin lipid çift tabakasının bir miktar bozulması yoluyla uygulandığını öne süren, çoğunlukla 'fizikokimyasal' teoriler ortaya çıktı. Anestezik etkiye neden olmak için birkaç tür çift katmanlı bozulma önerildi (incelemeler):
- faz ayrımındaki değişiklikler
- çift tabaka kalınlığındaki değişiklikler
- sipariş parametrelerindeki değişiklikler
- eğrilik esnekliğindeki değişiklikler
Yanal faz ayırma teorisine göre, anestezikler, sinir zarlarını, kritik lipid bölgelerindeki faz ayrımlarının ortadan kalktığı bir noktaya kadar akışkanlaştırarak hareket ederler. Bu anestezik kaynaklı akışkanlaştırma, zarları, iyon geçişi, sinaptik iletici salımı ve alıcılara iletici bağlanması gibi zar olaylarının temeli olabilecek proteinlerdeki konformasyonel değişiklikleri kolaylaştırma konusunda daha az yetenekli hale getirir.
Tüm bu modası geçmiş lipid teorileri genellikle dört zayıflıktan muzdariptir (tam açıklama aşağıdaki bölümlere bakınız):
- Anestezik bir ilacın stereoizomerleri çok farklı anestezik potansiyele sahipken, petrol/gaz bölme katsayıları benzerdir.
- Lipidlerde yüksek oranda çözünür olan ve bu nedenle anestezik olarak hareket etmesi beklenen bazı ilaçlar, bunun yerine konvülsif etki gösterir (ve bu nedenle hareketsizleştiriciler olarak adlandırılır ).
- Vücut sıcaklığındaki küçük bir artış, genel anestezikler kadar membran yoğunluğunu ve akışkanlığını etkiler, ancak anesteziye neden olmaz.
- Homolog bir düz zincirli alkol veya alkan serisinde zincir uzunluğunun arttırılması, lipid çözünürlüklerini arttırır, ancak anestetik güçleri, belirli bir sınır uzunluğunun ötesinde artmayı durdurur .
Bu nedenle, lipit çözünürlüğü ile genel anesteziklerin gücü arasındaki korelasyon, bir lipit hedef bölgesi çıkarımı için gerekli ancak yeterli olmayan bir koşuldur. Genel anestezikler , beyindeki proteinler üzerindeki hidrofobik hedef bölgelere eşit derecede iyi bağlanabilir . Daha polar genel anesteziklerin daha az etkili olmasının ana nedeni, beyindeki nöronlar üzerinde etkilerini göstermek için kan-beyin bariyerini geçmek zorunda olmalarıdır.
Modası geçmiş lipid hipotezlerine itirazlar
1. Anestezik bir ilacın stereoizomerleri
Birbirlerinin ayna görüntülerini temsil eden stereoizomerler, enantiyomerler veya optik izomerler olarak adlandırılır (örneğin, R-(+)- ve S-(-)-etomidat izomerleri). Enantiyomerlerin fizikokimyasal etkileri, aşiral bir ortamda (örneğin lipid çift tabakasında) her zaman aynıdır. Bununla birlikte, birçok genel anestezik maddenin (örneğin izofluran , tiyopental , etomidat ) in vivo enantiyomerleri , benzer yağ/gaz bölme katsayılarına rağmen anestezik güçleri açısından büyük farklılıklar gösterebilir. Örneğin, etomidatın R-(+) izomeri, S-(-) izomerinden 10 kat daha güçlü anestetiktir. Bu, optik izomerlerin aynı şekilde lipide bölündüğü, ancak iyon kanalları ve sinaptik iletim üzerinde farklı etkilere sahip olduğu anlamına gelir . Bu itiraz, anestezikler için birincil hedefin aşiral lipid çift tabakasının kendisi değil , spesifik anestezik-protein kenetlenme etkileşimleri için kiral bir ortam sağlayan membran proteinleri üzerindeki stereoselektif bağlanma bölgeleri olduğuna dair ikna edici bir kanıt sağlar .
2. Hareketsizleştiriciler
Tüm genel anestezikler, omurilik fonksiyonlarının depresyonu yoluyla immobilizasyona (zararlı uyaranlara yanıt olarak hareket yokluğu) neden olurken, amnezik etkileri beyinde uygulanır. Meyer-Overton korelasyonuna göre, ilacın anestetik gücü, lipid çözünürlüğü ile doğru orantılıdır, ancak bu kuralı karşılamayan birçok bileşik vardır. Bu ilaçlar, güçlü genel anesteziklere çarpıcı bir şekilde benzerdir ve lipid çözünürlüklerine dayalı olarak güçlü anestezikler oldukları tahmin edilmektedir, ancak anestezik etkinin yalnızca bir bileşenini (amnezi) uygularlar ve hareketi baskılamazlar (yani omurilik fonksiyonlarını baskılamazlar). tüm anestezikler yapar. Bu ilaçlara hareketsizleştiriciler denir. Hareketsizleştiricilerin varlığı, anesteziklerin, daha önce inanıldığı gibi sadece tek bir hedefi (nöronal çift katman) değil, farklı moleküler hedefleri etkileyerek anestezik etkinin farklı bileşenlerini (amnezi ve hareketsizlik) indüklediğini düşündürmektedir. Hareketsizleştirici olmayanlara iyi bir örnek, çok hidrofobik olan ancak uygun konsantrasyonlarda zararlı uyarıma yanıt olarak hareketi baskılayamayan halojenli alkanlardır. Ayrıca bakınız: flurothyl .
3. Sıcaklık artışlarının anestezik etkisi yoktur.
Deneysel çalışmalar, etanol dahil genel anesteziklerin, doğal ve yapay membranların güçlü akışkanlaştırıcıları olduğunu göstermiştir. Bununla birlikte, genel anesteziklerin klinik konsantrasyonlarının varlığında membran yoğunluğu ve akışkanlığındaki değişiklikler o kadar küçüktür ki, sıcaklıktaki (~1 °C) nispeten küçük artışlar, anesteziye neden olmadan bunları taklit edebilir. Vücut sıcaklığındaki yaklaşık 1 °C'lik değişiklik fizyolojik aralık içindedir ve açıkça bilinç kaybına neden olmak için yeterli değildir. Böylece membranlar sadece büyük miktarlarda anestezik ile akışkanlaştırılır, ancak anestezik konsantrasyonları küçük ve farmakolojik olarak ilgili ile sınırlı olduğunda membran akışkanlığında herhangi bir değişiklik olmaz.
4. Efekt, belirli bir zincir uzunluğunun ötesinde kaybolur
Meyer-Overton korelasyonuna göre, herhangi bir genel anestetiğin (örneğin n - alkoller veya alkanlar) homolog bir serisinde , zincir uzunluğunun arttırılması lipit çözünürlüğünü arttırır ve dolayısıyla anestetik gücünde karşılık gelen bir artış üretmelidir. Ancak belirli bir zincir uzunluğunun ötesinde anestezik etki ortadan kalkar. İçin , n -alkoller, bu kesim yaklaşık 13 arasında bir karbon zinciri uzunluğuna de ve oluşur , n türlerine bağlı olarak, 6 ve 10 arasında bir zincir uzunluğunda alkanlar.
Genel anestezikler, lipit çift tabakasına bölünerek ve bu tabakayı bozarak iyon kanallarını bozarsa, lipit çift tabakalarındaki çözünürlüklerinin de cutoff etkisini göstermesi beklenir. Ancak lipid iki katmanlı alkollerin ayıran bir uzun zincirli alkoller için cutoff görüntülenmez n - dekanol için n - pentadekanol . Lipid çift tabakası/tampon bölme katsayısı K'nin logaritmasına karşı zincir uzunluğunun bir grafiği doğrusaldır ve her metilen grubunun eklenmesi Gibbs serbest enerjisinde -3.63 kJ/mol'lük bir değişikliğe neden olur .
Cutoff etkisi ilk olarak anesteziklerin etkilerini membran lipidleri üzerinde global olarak hareket ederek değil, proteinlerde iyi tanımlanmış hacimlerin hidrofobik ceplerine doğrudan bağlanarak gösterdiğinin kanıtı olarak yorumlandı. Olarak alkil zinciri , anestetik dolgular daha yüksek afinite ile hidrofobik cebine ve bağlar arasında büyür. Molekül hidrofobik cep tarafından tamamen barındırılamayacak kadar büyük olduğunda, artan zincir uzunluğu ile bağlanma afinitesi artık artmaz. Böylece, kesme uzunluğundaki n-alkanol zincirinin hacmi, bağlanma yeri hacminin bir tahminini sağlar. Bu itiraz, anestezik etkinin protein hipotezinin temelini oluşturdu (aşağıya bakınız).

Ancak cutoff etkisi yine de lipid hipotezi çerçevesinde açıklanabilir. Kısa zincirli alkanollerde (A) zincirin bölümleri oldukça katıdır (yapısal entropi açısından) ve sulu ara yüzey bölgesine ("şamandıra") bağlı hidroksil grubuna çok yakındır. Sonuç olarak, bu segmentler yanal gerilimleri çift katmanlı iç kısımdan arayüze doğru verimli bir şekilde yeniden dağıtır. Uzun zincirli alkanollerde (B) hidrokarbon zincir bölümleri hidroksil grubundan daha uzakta bulunur ve kısa zincirli alkanollere göre daha esnektir. Anestetik etki bir noktada kaybolana kadar hidrokarbon zincirinin uzunluğu arttıkça basıncın yeniden dağıtılmasının etkinliği azalır. İki komşu hidroksil grubu arasındaki zincir uzunluğu kesim değerinden daha küçükse, polialkanollerin (C) kısa zincirli 1-alkanollere benzer anestezik etkiye sahip olacağı öne sürülmüştür. Bu fikir deneysel kanıtlarla desteklenmiştir, çünkü polihidroksialkanlar 1,6,11,16-heksadekantetraol ve 2,7,12,17-oktadekantetraol orijinal olarak önerildiği gibi önemli anestezik etki göstermiştir.
Modern lipid hipotezi
Lipid hipotezinin modern versiyonu, genel anestezik maddenin çift tabakada çözünmesi, membran yanal basınçlarının yeniden dağılımına neden olursa, anestezik etkinin meydana geldiğini belirtir.
Her iki katmanlı membran, yanal basınçların kendi içinde nasıl dağıldığına dair farklı bir profile sahiptir. Çoğu membran proteini (özellikle iyon kanalları) bu yanal basınç dağılım profilindeki değişikliklere duyarlıdır. Bu yanal gerilmeler oldukça büyüktür ve membran içindeki derinliğe göre değişir. Modern lipid hipotezine göre, membran yanal basınç profilindeki bir değişiklik, ligand kapılı iyon kanalları gibi anesteziklerin klinik konsantrasyonlarından etkilendiği bilinen bazı membran proteinlerinin konformasyonel dengesini değiştirir. Bu mekanizma aynı zamanda spesifik değildir, çünkü anestezik maddenin gücü gerçek kimyasal yapısı tarafından değil, ikili katman içindeki segmentlerinin ve bağlarının konumsal ve oryantasyonel dağılımı ile belirlenir. Bununla birlikte, kesin moleküler mekanizmanın ne olduğu hala açık değildir.
1997'de Cantor, kafes istatistiksel termodinamiğine dayanan ayrıntılı bir genel anestezi mekanizması önerdi. Amfifilik ve diğer arayüzeysel olarak aktif çözünen maddelerin (örneğin genel anestezikler) çift tabakaya dahil edilmesinin, çift tabakanın merkezine doğru yanal basınçta bir azalma ile telafi edilen sulu arayüzlerin yakınında yanal basıncı seçici olarak arttırdığı öne sürülmüştür. Hesaplamalar, genel anestezinin, muhtemelen, bir postsinaptik ligand kapılı zar proteininde iyon kanalının açılmasının aşağıdaki mekanizma ile engellenmesini içerdiğini göstermiştir:
- Bir kanal, bir sinir uyarısına yanıt olarak açılmaya çalışır, böylece proteinin enine kesit alanını çift katmanın ortasından daha sulu arayüze yakın bir yerde arttırır;
- Daha sonra, ara yüzey yakınındaki yanal basınçta anestezik kaynaklı artış, protein konformasyonel dengesini kapalı duruma geri kaydırır, çünkü kanal açılması, ara yüzeydeki daha yüksek basınca karşı daha fazla çalışma gerektirecektir. Bu, yalnızca kuvvetin yapısal veya termodinamik özelliklerle korelasyonlarını değil, aynı zamanda ayrıntılı bir mekanik ve termodinamik anestezi anlayışını da sağlayan ilk hipotezdir.
Bu nedenle, modern lipit hipotezine göre, anestezikler doğrudan zar protein hedefleri üzerinde hareket etmezler, bunun yerine protein-lipit arayüzünde aracı olarak hareket eden özel lipit matrislerini bozarlar. Bu, anestezinin (ligand) protein üzerindeki spesifik bölgeye bağlanarak membran proteinlerinin işlevini etkilediği ligand ve reseptörün olağan tuş kilidi etkileşiminden farklı olan yeni bir tür transdüksiyon mekanizmasıdır. Bu nedenle, bazı zar proteinlerinin lipid ortamlarına duyarlı oldukları öne sürülmektedir. Aynı yıl, iki katmanlı bozulmanın iyon kanalını nasıl etkileyebileceğine dair biraz farklı, ayrıntılı bir moleküler mekanizma önerildi. Oleamid (oleik asidin yağ asidi amidi), in vivo (kedinin beyninde) bulunan endojen bir anestetiktir ve boşluk bağlantı kanalı bağlantısını kapatarak uykuyu güçlendirdiği ve vücut sıcaklığını düşürdüğü bilinmektedir. Ayrıntılı mekanizma resimde gösterilmektedir: connexon (macenta) çevresinde bulunan iyi düzenlenmiş lipit (yeşil)/kolesterol (sarı) halkası, anestezik (kırmızı üçgenler) ile tedavi edildiğinde düzensizleşir ve connexon iyon kanalının kapanmasını teşvik eder. Bu beyin aktivitesini azaltır ve uyuşukluğa ve anestezik etkiye neden olur. Son zamanlarda süper çözünürlüklü görüntüleme, tahmin edildiği gibi uçucu anesteziklerin sıralı lipid alanlarını bozduğuna dair doğrudan deneysel kanıtlar gösterdi. Aynı çalışmada, anesteziklerin lipid alanlarından fosfolipaz D (PLD) enzimini saldığı ve enzimin fosfatidik asit üretimi ile TREK-1 kanalına bağlandığı ve aktive ettiği ilgili bir mekanizma ortaya çıktı . Bu sonuçlar deneysel olarak, zarın genel anesteziklerin fizyolojik olarak ilgili bir hedefi olduğunu göstermiştir.
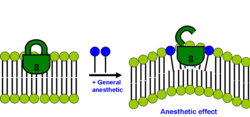
Genel anestezik etkinin zar proteini hipotezi

1980'lerin başında, Franks ve Lieb, Meyer-Overton korelasyonunun çözünür bir protein kullanılarak yeniden üretilebileceğini gösterdi. Lipidlerin toplam yokluğunda klinik anestezik dozları ile iki sınıf proteinin etkisiz hale getirildiğini bulmuşlardır. Bunlar, biyolüminesan hayvanlar ve bakteriler tarafından ışık üretmek için kullanılan lusiferazlar ve yağ asitleri , steroidler ve fenobarbital gibi ksenobiyotikler dahil olmak üzere çeşitli bileşikleri hidroksile eden bir grup hem proteini olan sitokrom P450'dir . Dikkat çekici bir şekilde, bu proteinlerin genel anestezikler tarafından inhibisyonu, anestetik güçleri ile doğrudan ilişkiliydi. Lusiferaz inhibisyonu ayrıca, anestezik bağlayıcı cebin boyutuyla ilgili olan uzun zincirli bir alkol kesmesi sergiler.
Bu gözlemler önemliydi çünkü genel anesteziklerin, aracı olarak lipid çift tabakası ile spesifik olmayan etkileşimler yoluyla dolaylı olarak membran proteinlerini etkilemek yerine, belirli proteinlerin hidrofobik protein bölgeleriyle de etkileşime girebileceğini gösterdiler. Anesteziklerin, protein kinaz C de dahil olmak üzere birçok sitoplazmik sinyal proteininin fonksiyonlarını değiştirdiği gösterilmiştir, ancak anestetiklerin en olası moleküler hedefleri olarak kabul edilen proteinler iyon kanallarıdır. Bu teoriye göre genel anestezikler, lipid hipotezi çerçevesinden çok daha seçicidirler ve CNS'deki sadece az sayıda hedefe doğrudan bağlanırlar, çoğunlukla sinapstaki ligand(nörotransmitter)-kapılı iyon kanalları ve iyon akışını değiştiren G-protein bağlı reseptörler. . Özellikle Cys-loop reseptörleri, alt birimler arasındaki arayüze bağlanan genel anestezikler için makul hedeflerdir. Cys-loop reseptörü üst ailesi, inhibitör reseptörleri (GABA A, GABA C, glisin reseptörleri) ve uyarıcı reseptörleri (asetilkolin reseptörü ve 5-HT3 serotonin reseptörü) içerir. Genel anestezikler sırasıyla uyarıcı reseptörlerin kanal fonksiyonlarını inhibe edebilir veya inhibitör reseptörlerin fonksiyonlarını kuvvetlendirebilir. Anestezikler için protein hedefleri kısmen tanımlanmış olsa da, genel anestezik-protein etkileşimlerinin tam doğası hala bir sır olarak kalmaktadır.
Başlangıçta, genel anesteziklerin hedef iyon kanalına bir kilit mekanizmasıyla bağlandığı ve yapısını açıktan kapalıya veya tam tersine önemli ölçüde değiştirdiği varsayılmıştı. Bununla birlikte, membran proteinlerinin genel anesteziklerle doğrudan tuş kilidi etkileşimine karşı önemli miktarda kanıt vardır.
Çeşitli çalışmalar, inhale genel anestezikler de dahil olmak üzere düşük afiniteli ilaçların, transmembran reseptörlerinin, iyon kanallarının ve globüler proteinlerin moleküler yapılarını değiştirmedikleri için genellikle hedef proteinleri ile spesifik kilit ve anahtar bağlama mekanizması yoluyla etkileşime girmediklerini göstermiştir. Bu deneysel gerçeklere ve bazı bilgisayar simülasyonlarına dayanarak, protein hipotezinin modern versiyonu önerildi. Dört-a-sarmal demeti yapısal motifinin proteinleri, pentamerik Cys-ilmek reseptörünün monomer modelleri olarak hizmet etti, çünkü solunan anesteziklerin bağlayıcı ceplerinin, Cys-ilmek reseptörlerinin transmembran dört-a-sarmal demetleri içinde olduğuna inanılmaktadır. Solunan genel anestezik, membran kanalının yapısını değiştirmez, ancak dinamiklerini, özellikle de α-helisleri bir demet halinde bağlayan ve membran-su arayüzüne maruz kalan esnek halkalardaki dinamiklerini değiştirir. Mikrosaniye-milisaniye zaman ölçeğindeki protein dinamiğinin genellikle proteinin işlevleriyle birleştiği iyi bilinen bir gerçektir. Bu nedenle, solunan genel anesteziklerin protein yapısını değiştirmedikleri için, protein dinamiklerini yavaş mikrosaniye-milisaniye zaman ölçeğinde modüle ederek ve/veya bu proteinin işlevi için gerekli hareket modlarını bozarak proteinler üzerindeki etkilerini gösterebileceklerini önermek mantıklıydı. Protein fonksiyonlarında ve agonist bağlanmasında kritik roller oynayan su-lipid arayüzündeki protein bölgelerindeki (ilmekler) kalıntılar arasındaki normal etkileşimler genel anestezi ile bozulabilir. Aynı ilmek içindeki veya farklı ilmekler arasındaki etkileşimler anestezikler tarafından bozulabilir ve sonuçta Cys-loop reseptörlerinin işlevleri değişebilir.
Anestezik etkinin mikrotübül kuantum titreşim teorisi
Anestezik gazlar nöronal membran proteinlerine bağlanır, ancak bunlar üzerindeki etkileri tutarsız ve paradoksaldır. 2008'de önde gelen araştırmacılar şu sonuca varmışlardır: “…yirmi yıllık odaklanmış araştırma, tek başına hareketsizliğe aracılık etmek için yeterli olan bir ligand veya voltaj kapılı kanal belirlemedi….Ayrıca, hiçbir kombinasyon…yeterli görünmüyor…”. Ancak anestezikler , mikrotübüllerdeki hücre iskeleti aktin ve tübülin dahil olmak üzere nöronların içindeki sitoplazmik proteinlerin işlevlerini de bağlar ve değiştirir . Tübülin polimerleri, mikrotübüller nöronal büyümeyi yönlendirir, sinapsları düzenler ve teorik olarak hafızayı kodlamak ve bilince aracılık etmek için önerilmiştir. Yüksek konsantrasyonlarda (~5 MAC) anestetik gaz halotan, mikrotübüllerin geri dönüşümlü depolimerizasyonuna neden olur. ~1 MAC halotanda, genomik, proteomik, optogenetik ve klinik çalışmalar, anestetik etkinin fonksiyonel bölgesi olarak tübülin/mikrotübüllere işaret etmektedir.
Anestezikler mikrotübüllere bilinç kaybına neden olmak için ne yapabilir? 1990'ların ortalarında Stuart Hameroff ve Sir Roger Penrose ( 'Orch VEYA' olarak da bilinen ' düzenlenmiş nesnel indirgeme ') tarafından ileri sürülen oldukça tartışmalı bir teori , bilincin beyin nöronları içindeki tübül/mikrotübüllerdeki kuantum titreşimlerine dayandığını öne sürüyor. Tubulinin atomik yapısının bilgisayar modellemesi, anestezik gaz moleküllerinin polar olmayan pi elektron rezonans bulutlarının amino asit aromatik halkalarına bitişik olarak bağlandığını ve her bir tubulindeki 86 pi rezonans halkasının tümü arasındaki kolektif kuantum dipol salınımlarının bir kuantum titreşimleri spektrumu gösterdiğini buldu. 613 terahertz'de (613 x 10 12 Hz) ortak mod zirvesi . 8 farklı anestezik gazın ve 2 anestezik olmayan/immobilizer olmayan gazın ('NA'lar - yukarıya bakın) her birinin simüle edilmiş varlığı, 8 anesteziğin tümünün tübülin terahertz salınımlarını (spektrumu daha düşük frekanslara kaydırarak) güçleriyle orantılı olarak azalttığını gösterdi, ve 613 terahertz zirvesini ortadan kaldırdı. NA'lar (TFMB ve F6) terahertz spektrumunu azaltmadı ve 613 terahertz zirvesini etkilemedi. NA'ların anestetik gazlardan önemli ölçüde daha yüksek polarize edilebilirliğe sahip olduğu bulundu, bu da NA elektron bulutu dipollerinin sönümleme olmadan 'sürüşüne devam ettiğini' gösterirken, daha az polarize olabilen anesteziklerle birleştirmenin dipol salınımlarını sönümlemek için yeterli 'sürükleme' uyguladığını ima etti. Orch OR, tübülindeki terahertz salınımlarının, EEG'de görülen daha yavaş frekanslara rezonans müdahalesiyle yukarı doğru uzanan, ölçekle değişmeyen çok seviyeli bir hiyerarşinin küçük, hızlı ucu olduğunu ve anesteziklerin biyolojik kökeninde bilinci, mikrotübüllerdeki terahertz salınımlarını engellediğini öne sürüyor.
Anestezik etkinin 'Mikrotübül kuantum titreşim teorisi', Orch OR'nin öncülündeki birkaç kritik kusur ve teoriyi desteklemek için kullanılan verilerin tahrif edilmesi nedeniyle tartışmalıdır . Bu sorunlara rağmen, savunucuları, yukarıda açıklanan anestezik gazların moleküler etkisinin bilinen birçok kriteri ile tutarlı olduğunu savunuyorlar:
| Meyer-Overton korelasyonu | Farklı potansiyellere sahip stereoizomerler | Anestezisiz/İmmobilizersiz (NA'lar) | Sıcaklık lipid çift katmanlı düzensizlik | Boyut kesme etkisi | Basınç tersine çevirme | |
|---|---|---|---|---|---|---|
| membran lipidleri | Evet | Numara | Numara | Numara | Numara | Evet |
| zar proteinleri | Numara | Evet | Numara | Evet | Evet | Evet |
| Mikrotübül kuantum titreşimi | Evet | Evet | Evet | Evet | Evet | Evet |
Referanslar
daha fazla okuma
- v. Hintzenstern U; Petermann H; Schwarz W (Kasım 2001). "Frühe Erlanger Beiträge zur Theorie und Praxis der äther- und Chloroformnarkose: Die tierexperimentellen Untersuchungen von Ernst von Bibra und Emil Harless". Der Anestezist (Almanca). 50 (11): 869-80. doi : 10.1007/s001010100220 . PMID 11760483 . S2CID 21280594 .