gümüş oksit - Silver oxide
|
|

|
|
| İsimler | |
|---|---|
|
IUPAC adı
Gümüş(I) oksit
|
|
| Diğer isimler
Gümüş pas, Argentous oksit, Gümüş monoksit
|
|
| tanımlayıcılar | |
|
3B model ( JSmol )
|
|
| Kimyasal Örümcek | |
| ECHA Bilgi Kartı |
100.039.946 |
| AT Numarası | |
| ağ | gümüş+oksit |
|
PubChem Müşteri Kimliği
|
|
| RTECS numarası | |
| ÜNİİ | |
|
CompTox Panosu ( EPA )
|
|
|
|
|
|
| Özellikler | |
| Ag 2 O | |
| Molar kütle | 231.735 g·mol -1 |
| Dış görünüş | Siyah/kahverengi kübik kristaller |
| Koku | Kokusuz |
| Yoğunluk | 7.14 g / cc 3. |
| Erime noktası | 300 °C (572 °F; 573 K) ≥200 °C'den ayrışır |
| 0,013 g/L (20 °C) 0,025 g/L (25 °C) 0,053 g/L (80 °C) |
|
|
AgOH'nin çözünürlük ürünü ( K sp )
|
1.52·10 -8 (20 °C) |
| çözünürlük | Çözünür asit , alkali çözünmez etanol |
| -134,0 · 10 -6 cm 3 / mol | |
| Yapı | |
| kübik | |
| Pn 3 m, 224 | |
| Termokimya | |
|
Isı kapasitesi ( C )
|
65,9 J/mol·K |
|
Std molar
entropi ( S |
122 J/mol·K |
|
Std
oluşum entalpisi (Δ f H ⦵ 298 ) |
-31 kJ/mol |
|
Gibbs serbest enerjisi (Δ f G ˚)
|
-11.3 kJ/mol |
| Tehlikeler | |
| GHS piktogramları |
 
|
| GHS Sinyal kelimesi | Tehlike |
| H272 , H315 , H319 , H335 | |
| P220 , P261 , P305+351+338 | |
| NFPA 704 (ateş elması) | |
| Ölümcül doz veya konsantrasyon (LD, LC): | |
|
LD 50 ( ortalama doz )
|
2.82 g/kg (sıçan, oral) |
| Bağıntılı bileşikler | |
|
Bağıntılı bileşikler
|
Gümüş(I,III) oksit |
|
Aksi belirtilmedikçe, veriler standart durumdaki malzemeler için verilmiştir (25 °C [77 °F], 100 kPa'da). |
|
|
|
|
| Bilgi kutusu referansları | |
Gümüş(I) oksit , Ag 2 O formülüne sahip kimyasal bileşiktir. Diğer gümüş bileşiklerini hazırlamak için kullanılan ince siyah veya koyu kahverengi bir tozdur .
Hazırlık

Gümüş oksit, gümüş nitratın sulu çözeltileri ve bir alkali hidroksitin birleştirilmesiyle hazırlanabilir . Bu reaksiyon, aşağıdaki reaksiyon için uygun enerjilerden dolayı kayda değer miktarda gümüş hidroksit sağlamaz:
- 2 AgOH → Ag 2 O + H 2 O ( p K = 2.875)
Uygun şekilde kontrol edilen şartlar ile, bu reaksiyon Ag hazırlamak için kullanılabilecek 2 ince bir iletken macun dolgu taneli olarak dahil olmak üzere çeşitli kullanımlar için uygun olan özelliklere sahip O toz.
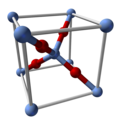
Yapı ve özellikler
Ag 2 O, tetrahedral oksitlerle birbirine bağlanan lineer, iki koordinatlı Ag merkezlerine sahiptir. Bu ise izo- ile Cu 2 O . Onu bozan çözücülerde "çözünür". Ag(OH) iyonunun oluşumu nedeniyle suda az çözünür.-
2ve muhtemelen ilgili hidroliz ürünleri. Amonyak çözeltisinde çözünür , Tollens reaktifinin aktif bileşiğini üretir . Bir Ag 2 O bulamacı asitler tarafından kolayca saldırıya uğrar :
- Ag 2 O + 2 HX → 2 AgX + H 2 O
burada HX = HF , HCl , HBr , HI , ya da CF 3 COOH . Aynı zamanda , gümüş klorürü çökeltmek için alkali klorür çözeltileri ile reaksiyona girerek karşılık gelen alkali hidroksit çözeltisini bırakır.
Birçok gümüş bileşiği gibi, gümüş oksit de ışığa duyarlıdır. Ayrıca 280 °C'nin üzerindeki sıcaklıklarda ayrışır.
Uygulamalar
Bu oksit gümüş oksit pillerde kullanılır . Organik kimyada gümüş oksit, hafif oksitleyici ajan olarak kullanılır . Örneğin, okside aldehitler için karboksilik asitler . Gümüş oksit hazırlanır Bu tür reaksiyonlar, çoğu zaman en iyi sonucu in situ gelen gümüş nitrat ve alkali hidroksit .
Referanslar
Dış bağlantılar
- Gümüş Oksit Tavlama - Gösteri deneyi: Talimat ve video

