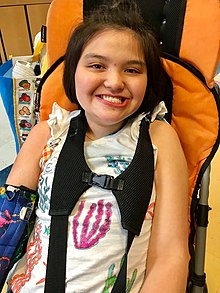
Rett sendromu - Rett syndrome
| Rett sendromu | |
|---|---|
| Diğer isimler | Serebroatrofik hiperamonyemi ( eski ); demans, ataksi ve amaçlı el kullanımı kaybı sendromu |
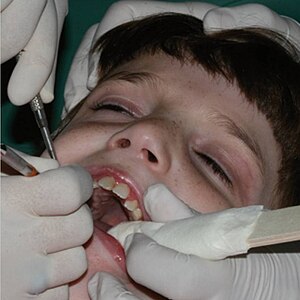 | |
| Diş işi için konumlandırılmış Rett sendromlu kız | |
| uzmanlık | psikiyatri , pediatri |
| Belirtiler | Dil ve koordinasyonda bozulmalar ve tekrarlayan hareketler, daha yavaş büyüme, daha küçük kafa |
| komplikasyonlar | Nöbetler , skolyoz , uyku sorunları |
| Her zamanki başlangıç | 6-18 aylıktan sonra |
| Süre | ömür boyu |
| nedenler | MECP2 genindeki mutasyon |
| teşhis yöntemi | Semptomlara dayalı olarak, genetik test |
| Ayırıcı tanı | Angelman sendromu , otizm , serebral palsi , çeşitli nörodejeneratif bozukluklar . |
| Tedavi | Özel eğitim , fizyoterapi, diş teli |
| İlaç tedavisi | Antikonvülzanlar |
| prognoz | Birçoğu için yaşam beklentisi orta yaştır. |
| Sıklık | 8500 kadından 1'i |
Rett sendromu ( RTT ), kadınlarda tipik olarak 6-18 aylıktan sonra ortaya çıkan genetik bir bozukluktur . Semptomlar dil ve koordinasyondaki bozuklukları ve tekrarlayan hareketleri içerir. Etkilenenler genellikle daha yavaş büyüme, yürüme zorluğu ve daha küçük bir kafa boyutuna sahiptir . Rett sendromunun komplikasyonları arasında nöbetler , skolyoz ve uyku sorunları yer alabilir . Bununla birlikte, durumun ciddiyeti değişkendir.
Rett sendromu, X kromozomu üzerindeki MECP2 genindeki genetik bir mutasyondan kaynaklanır . Neredeyse her zaman yeni bir mutasyon olarak ortaya çıkar ve vakaların yüzde birinden daha azı bir kişinin ebeveynlerinden miras alınır. Neredeyse sadece kızlarda görülür; benzer bir mutasyona sahip erkek çocuklar genellikle doğumdan kısa bir süre sonra ölürler. Tanı semptomlara dayanır ve genetik testlerle doğrulanabilir .
Rett sendromunun bilinen bir tedavisi yoktur. Tedavi semptomları iyileştirmeye yöneliktir. Antikonvülsanlar nöbetlere yardımcı olmak için kullanılabilir. Özel eğitim , fizyoterapi ve diş telleri de faydalı olabilir. Durumu olanların çoğu orta yaşta yaşıyor.
Durum yaklaşık 8.500 kadından 1'ini etkiler. İlk kez 1966'da Avusturyalı çocuk doktoru Andreas Rett tarafından tanımlanmıştır . Yazıları Almanca olduğu için İngilizce konuşulan dünyada yaygın olarak tanınmamıştır. İsveçli çocuk doktoru Bengt Hagberg 1983'te bir İngilizce makale yayınladı ve duruma Rett'in adını verdi. 1999'da Lübnanlı-Amerikalı doktor Huda Zoghbi , duruma neden olan mutasyonu keşfetti.
Belirti ve bulgular
Aşama I
Erken başlangıç olarak adlandırılan Aşama I, tipik olarak 6 ila 18 aylıkken başlar. Bu aşama genellikle gözden kaçar, çünkü bozukluğun semptomları biraz belirsiz olabilir ve ebeveynler ve doktorlar ilk başta gelişimdeki ince yavaşlamayı fark etmeyebilirler. Bebek daha az göz teması kurmaya başlayabilir ve oyuncaklara daha az ilgi duyabilir. Oturma veya emekleme gibi kaba motor becerilerde gecikmeler olabilir. El sıkma ve azalan kafa büyümesi olabilir, ancak dikkat çekmek için yeterli değildir. Bu aşama genellikle birkaç ay sürer ancak bir yıldan fazla devam edebilir.
Aşama II
Aşama II veya hızlı yıkıcı aşama, genellikle 1 ila 4 yaşları arasında başlar ve haftalar veya aylar sürebilir. Çocuk amaçlı el becerilerini ve konuşma dilini kaybettiği için başlangıcı hızlı veya kademeli olabilir. Sıkmak, yıkamak, alkışlamak veya vurmak gibi karakteristik el hareketleri ve elleri tekrar tekrar ağza götürmek genellikle ağızlama olarak adlandırılan bu aşamada başlar. Çocuk, rastgele dokunma, kavrama ve bırakma ile arkadan kenetlenmiş veya yanlardan tutulan elleri tutabilir. Çocuk uyanıkken hareketler devam eder ancak uyku sırasında kaybolur. Uyku sırasında solunum genellikle düzelse de, apne ve hiperventilasyon atakları gibi solunum düzensizlikleri meydana gelebilir. Bazı kızlar ayrıca sosyal etkileşim ve iletişim kaybı gibi otistik belirtiler de gösterirler. Yürüme dengesiz olabilir ve motor hareketleri başlatmak zor olabilir. Yavaşlamış kafa büyümesi genellikle bu aşamada fark edilir.
Aşama III
Aşama III veya plato veya sözde durağan aşama, genellikle 2 ila 10 yaşları arasında başlar ve yıllarca sürebilir. Apraksi , motor problemler ve nöbetler bu aşamada belirgindir. Bununla birlikte, daha az sinirlilik, ağlama ve otistik benzeri özelliklerle davranışta iyileşme olabilir . Aşama III'te çevreye daha fazla ilgi olabilir ve uyanıklık, dikkat süresi ve iletişim becerileri gelişebilir. Birçok kız, hayatlarının çoğu için bu aşamada kalır.
Aşama IV
Evre IV veya geç motor bozulma aşaması, yıllarca veya on yıllarca sürebilir. Belirgin özellikler arasında azalan hareketlilik, omurganın eğriliği ve kas zayıflığı, sertlik, spastisite ve bir kol, bacağın anormal duruşu ile artan kas tonusu bulunur. Daha önce yürüyebilen kızlar yürümeyi bırakabilir. Biliş, iletişim veya el becerileri genellikle IV. evrede azalmaz. Tekrarlayan el hareketleri azalabilir ve bakışlar genellikle düzelir.
Varyantlar
Rett sendromunun tipik formunun belirti ve semptomları iyi tanımlanmıştır. Rett sendromunun klasik formuna ek olarak, yıllar içinde birkaç atipik form tanımlanmıştır; ana gruplar şunlardır:
- Konjenital varyant (Rolando varyantı): Rett sendromunun bu ağır alt tipinde hastaların gelişimi ve baş çevresi doğuştan anormaldir. Rett sendromlu hastaların tipik bakışları genellikle yoktur;
- Rett Sendromunun Zappella varyantı veya korunmuş konuşma varyantı: Rett sendromunun bu alt tipinde hastalar bazı el becerileri kazanırlar ve dil 5 yaş civarında (yani regresyon evresinden sonra) kısmen düzelir. Boy, kilo ve baş çevresi genellikle normal sınırlar içindedir ve iyi bir kaba motor fonksiyon gözlemlenebilir. Zappella varyantı, Rett sendromunun daha hafif bir şeklidir;
- Hanefeld varyantı veya erken epilepsi varyantı. Rett sendromunun bu formunda hastalar 5 aylıktan önce epilepsiden muzdariptir.
Rett sendromunun tanımı yıllar içinde rafine edilmiştir: atipik formlar klasik forma yakın varlığını sürdürdüğü için (Hagberg & Gillgerg, 1993), "Rett Kompleksi" terminolojisi tanıtıldı.
Neden
Genetik olarak, Rett sendromuna (RTT), X kromozomunda (metillenmiş DNA'nın transkripsiyonel susturulması ve epigenetik düzenlenmesinde yer alan) bulunan MECP2 genindeki mutasyonlar neden olur ve sporadik olarak veya germ hattı mutasyonlarından kaynaklanabilir. RTT vakaların% 10'dan daha az ise, genlerindeki mutasyonlar CDKL5 veya FOXG1 da bunu benzer olduğu tespit edilmiştir. Rett sendromu başlangıçta klinik gözlemle teşhis edilir, ancak MECP2 geninde genetik bir kusur olduğunda tanı kesinleşir. Bazı çok nadir durumlarda, bilinen mutasyona uğramış gen bulunamaz; muhtemelen MECP2'deki şu anda kullanılan tekniklerle tanımlanmayan değişiklikler veya klinik benzerliklerle sonuçlanabilecek diğer genlerdeki mutasyonlar nedeniyle.
Rett sendromunun aslında nörodejeneratif bir durumun aksine nörogelişimsel bir durum olduğu iddia edilmiştir. Bunun bir kanıtı, uyarılmış Rett Sendromlu farelerin nöron ölümü göstermemesidir ve bazı araştırmalar, işlevsel MECP2 geninin yetişkin olduklarında geri eklenmesiyle fenotiplerinin kısmen kurtarılabileceğini ileri sürmüştür. Bu bilgi aynı zamanda bozukluğu tedavi etmeyi amaçlayan daha ileri çalışmaların yapılmasına da yardımcı olmuştur.
sporadik mutasyonlar
Rett sendromu vakalarının en az %95'inde neden çocukta de novo mutasyondur . Yani, her iki ebeveynden de miras alınmaz. Ebeveynler genellikle bir MECP2 mutasyonu olmaksızın genotipik olarak normaldir.
RTT'nin sporadik formunun olduğu durumlarda, mutasyona uğramış MECP2'nin neredeyse tamamen X kromozomunun erkek kopyasındaki bir de novo mutasyondan türediği düşünülmektedir. Spermin mutasyona uğramasına neyin sebep olduğu henüz bilinmiyor ve bu tür mutasyonlar nadirdir.
germ hattı mutasyonları
Ayrıca, metil-CpG bağlayıcı protein-2 , MeCP2'yi kodlayan gende bir germ hattı mutasyonuna sahip fenotipik olarak normal annelerden de kalıtsal olabilir . Bu vakalarda kalıtım, X'e bağlı baskın bir model izler ve çoğu erkek uteroda veya doğumdan kısa bir süre sonra öldüğü için neredeyse yalnızca kadınlarda görülür . MECP2, Xq28'de X kromozomunun uzun kolunun ucuna yakın bir yerde bulunur. İnfantil spazmlar veya erken başlangıçlı epilepsi ile karakterize edilen atipik bir RTT formu, sikline bağımlı kinaz benzeri 5'i ( CDKL5 ) kodlayan gendeki bir mutasyondan da kaynaklanabilir . Rett sendromu, 12 yaşına kadar her 12.500 kadın canlı doğumdan birini etkiler.
mekanizma
Pontin noradrenerjik eksiklikleri
Rett sendromlu kişilerde beyin norepinefrin seviyeleri daha düşüktür (incelendi). MECP2'nin genetik kaybı , serebral korteks ve hipokampusun noradrenerjik innervasyonunun tek kaynağı olan locus coeruleus'taki hücrelerin özelliklerini değiştirir . Bu değişiklikler, hipereksitabiliteyi ve noradrenerjik innervasyonunun azalmış işleyişini içerir. Ayrıca, bir azalma tirosin hidroksilaz (Th) mRNA düzeyi, katekolamin sentezinde hız sınırlayıcı bir enzim, bütün tespit edilmiş pons ve MECP2 (-null erkek hem de yetişkin heterozigot MECP2 +/-), dişi farelerin. İmmüno-kantitatif teknikler kullanılarak, semptomatik MeCP2 eksikliği olan farelerde Th protein boyama seviyesinde, locus coeruleus TH eksprese eden nöronların sayısında ve yapıyı çevreleyen dendritik ağaçlandırma yoğunluğunda bir azalma gösterildi . Bununla birlikte, locus coeruleus hücreleri ölmüyor, ancak ponsta hiçbir apoptotik nöron tespit edilmediğinden tamamen olgun fenotiplerini kaybetme olasılıkları daha yüksek.
Araştırmacılar şu sonuca varmışlardır: "Bu nöronlar beyin sapı ve ön beyin boyunca önemli bir norepinefrin kaynağı oldukları ve Rett sendromunda bozulan solunum ve biliş gibi çeşitli işlevlerin düzenlenmesinde yer aldıkları için, locus coeruleus'un kritik bir bölge olduğunu varsayıyoruz. hangi MECP2 kaybı CNS işlev bozukluğuna neden olur." Normal locus coeruleus fonksiyonunun restorasyonu bu nedenle Rett sendromunun tedavisinde potansiyel terapötik değere sahip olabilir.
Orta beyin dopaminerjik bozukluklar
Memeli beynindeki dopaminin çoğunluğu mezensefalonda bulunan çekirdekler tarafından sentezlenir . Substantia nigra pars compacta (SNpc), ventral tegmental alan (VTA) ve retrorubral alan (RRF) (örneğin, katekolamin sentezinde hız sınırlayıcı bir enzim Th) tirosin hidroksilaz eksprese dopaminerjik nöronlar içerir.
Nigro-striatal yol, SNPC'den kaynaklanır ve ana rostral hedefi olan Kaudat-Putamen'i (CPu) medyan ön beyin demeti (MFB) yoluyla ışınlar. Bu bağlantı, bir kortiko-bazal gangliyatalamo-kortikal döngü tarafından hesaplanan motor stratejilerin sıkı modülasyonunda yer alır.
Gerçekten de, bazal gangliyonların kanonik anatomofonksiyonel modeline dayalı olarak, nigrostriatal dopamin, striatal GABAerjik orta dikenli nöronlarda bulunan dopaminerjik reseptörler üzerinde hareket ederek motor döngüyü modüle edebilir.
Nigrostriatal yolun düzensizliği, insanlarda Parkinson hastalığına (PD) neden olur. SNpc nöronlarının toksik ve/veya genetik ablasyonu, farelerde ve primatlarda deneysel parkinsonizm üretir. PD ve PD hayvan modellerinin ortak özellikleri motor bozukluklardır (hipotoni, bradikinezi, hipokinezi).
RTT patolojisi, bazı yönlerden PD hastalarında gözlenen motor fenotiple örtüşmektedir. Postmortem beyin örnekleri üzerinde yapılan birkaç nöropatolojik çalışma, nöromelanin hipopigmentasyonu, yapı alanında azalma ve hatta tartışmalı apoptoz belirtileri ile kanıtlanan bir SNPC değişikliğini savundu. Buna paralel olarak, birkaç katekolamin (dopamin, noradrenalin, adrenalin) ve bunların başlıca metabolik yan ürünlerinin azalmasıyla bir hipometabolizmanın altı çizildi. RTT'nin fare modelleri mevcuttur ve en çok çalışılanlar, Adrian Bird veya Katelyn McCormick laboratuvarları tarafından geliştirilen yapısal olarak silinmiş Mecp2 fareleridir .
RTT fenotipinin motor spektrumuna uygun olarak, Mecp2- null fareler, doğum sonrası 30. günden ölüme kadar kötüleşen motor anormallikler gösterir. Bu modeller, bir MeCP2 eksikliğinin moleküler ve nöroanatomik bağıntılarını aydınlatmak için çok önemli bir substrat sunar . Son zamanlarda (2008), katekolaminerjik nöronlarda Mecp2'nin koşullu olarak silinmesinin ( Th-Cre farelerini loxP ile çevrili Mecp2 olanlarla çaprazlayarak ) bir motor semptomatolojisini özetlediği gösterildi, ayrıca MeCP2'den yoksun farelerde beyin Th seviyelerinin belgelendiği belgelendi. katekolaminerjik nöronlarda sadece motor fenotipe katılarak azalır.
Bununla birlikte, terapötiklerin değerlendirilmesi için en çok çalışılan model Mecp2- null faredir (tamamen MeCP2'den yoksundur ). Bu bağlamda, 5 haftalıktan itibaren Th eksprese eden nöronların sayısında ve soma boyutunda bir azalma mevcuttur ve buna SNpc'den kaynaklanan dopaminerjik nöronların ana hedefi olan kaudat-putamende Th immünoreaktivitesinde bir azalma eşlik eder. Ayrıca, mikrodisseke edilmiş orta beyin ve striatal alanlarda dopaminerjik içeriklerin bir nörokimyasal analizi, beş ve dokuz haftalıkken dopaminde bir azalma olduğunu ortaya çıkardı. Daha sonra (dokuz haftada), morfolojik parametrelerin değişmeye devam etmesi, ancak kötüleşmemesi, buna karşın fenotipin ilerlemesi ve davranışsal eksikliklerin daha şiddetli olması dikkate değerdir. SNpc'de kalan nöronlarda tam olarak aktive edilmiş Th (Serin40-fosforile izoform) miktarı 5 haftada hafif etkilenir, ancak 9 haftada ciddi şekilde bozulur. Son olarak, MeCP2 eksikliği olan fareler üzerinde kronik ve oral bir L-Dopa tedavisi kullanarak, yazarlar daha önce tanımlanan bazı motor eksikliklerin düzeldiğini bildirdiler. Toplamda, bu sonuçlar , nöromotor eksikliklerin bir katkısı olarak MeCP2 eksikliği olan hayvanlarda nigrostriatal dopaminerjik yolun bir değişikliğini tartışmaktadır .
Hastalığın beyin kaynaklı nörotrofik faktör (BDNF) ile bir ilişkisi vardır .
Etkileşimli yol haritası
Bir Rett sendromunun interaktif yolu haritası yayınlanmıştır.
Teşhis
Genetik bir nedenin keşfedilmesinden önce, Rett sendromu , otizm spektrum bozuklukları ile birlikte Ruhsal Bozuklukların Tanısal ve İstatistiksel El Kitabı (DSM) tarafından yaygın bir gelişimsel bozukluk olarak belirlenmişti . Bazıları bu kesin atamaya karşı çıktı çünkü RTT , aynı zamanda otistik özellikler sergileyen frajil X sendromu , tüberoskleroz veya Down sendromu gibi otistik olmayan bozukluklara benziyor . Araştırma moleküler mekanizmayı kanıtladıktan sonra, 2013'te DSM-5 sendromu zihinsel bir bozukluk olarak sınıflandırmadan tamamen çıkardı.
Rett sendromu teşhisi, gelişimsel dönüm noktalarıyla ilgili herhangi bir anormalliği gözlemlemek için çocuğun büyümesinin ve gelişiminin yakından gözlemlenmesini içerir. Baş büyümesinde azalma gözlendiğinde tanı düşünülür. Benzer semptomları olan durumlar öncelikle ekarte edilmelidir.
Teşhis için yerine getirilmesi gereken belirli kriterler vardır. Bir kan testi MECP2 mutasyonunun varlığını ekarte edebilir veya ekarte edebilir, ancak bu mutasyon başka koşullarda da mevcuttur.
Klasik bir teşhis için, bir teşhise karar vermek için dört kriterin yanı sıra bir teşhisi ekarte etmek için iki kriter de karşılanmalıdır. Destekleyici kriterler de mevcut olabilir, ancak tanı için gerekli değildir. Atipik veya değişken bir tanı için, tanıda karar vermek için dört kriterden en az ikisinin yanı sıra on bir destekleyici kriterden beşinin karşılanması gerekir. İyileşme veya semptom stabilizasyonunun izlediği bir semptom gerileme periyodu da gerçekleşmelidir. Çocuklara genellikle otizm, serebral palsi veya başka bir gelişimsel gecikme biçimi olduğu yanlış teşhis edilir. MECP2 mutasyonu için pozitif bir test, tanı koymak için yeterli değildir.
karar vermek
- İnce motor becerilerin kullanımında azalma veya kayıp
- Azalmış veya sözlü konuşma kaybı
- Yürüyüş sırasındaki anormallikler
- Sıkma/sıkma veya alkışlama/dokunma gibi tekrarlayan el hareketleri
karar vermek
- Semptomları daha iyi açıklayabilecek travmatik beyin hasarı, nörometabolik hastalık veya ciddi enfeksiyon
- Yaşamın ilk altı ayında anormal psikomotor gelişim
destekleyici kriterler
- Uyanıkken solunum bozuklukları
- Uyanıkken Bruksizm
- Bozulmuş uyku düzeni
- Anormal kas tonusu
- Periferik vazomotor bozukluklar
- Skolyoz/kifoz
- Büyüme geriliği
- Küçük soğuk eller ve ayaklar
- Uygunsuz gülme/çığlık atma büyüleri
- Ağrıya azalmış tepki
- Yoğun göz iletişimi (gözle işaret etme)
Ayırıcı tanı
Otizme benzer Rett sendromu belirtileri :
- çığlık nöbetleri
- teselli edilemez ağlama
- göz temasından kaçınma
- sosyal/duygusal karşılıklılık eksikliği
- sosyal etkileşimi düzenlemek için sözel olmayan davranışların belirgin şekilde bozulmuş kullanımı
- konuşma kaybı
- duyusal problemler
- uyku gerilemesi
Serebral palside de mevcut olan Rett sendromu belirtileri (Rett sendromunda görülen tipin gerilemesi serebral palside olağandışı olacaktır; bu karışıklık nadiren yapılabilir):
- yürüme güçlüğü veya yutma güçlüğünden kaynaklanan yetersiz beslenme nedeniyle bazen olağandışı vücut oranlarına sahip olası kısa boy
- hipotoni
- Gecikmiş veya yürüme yeteneği yok
- yürüme/hareket zorlukları
- ataksi
- bazılarında mikrosefali - anormal derecede küçük kafa, zayıf kafa büyümesi
- gastrointestinal problemler
- bazı spastisite biçimleri
- kore - el veya yüz kaslarının spazmodik hareketleri
- distoni
- bruksizm - diş gıcırdatma
Tedavi
Şu anda Rett sendromunun tedavisi yoktur. Tedavi, işlevi iyileştirmeye ve semptomları gidermeye yöneliktir. Kişiyi yaşam boyunca tedavi etmek için tipik olarak çok disiplinli bir ekip yaklaşımı kullanılır. Bu ekip, birinci basamak hekimi , fizyoterapist, uğraşı terapisti, konuşma-dil patoloğu, beslenme uzmanı ve akademik ve mesleki ortamlardaki destek hizmetlerini içerebilir . Bazı çocuklar, skolyozu durdurmak için diş telleri, el hareketlerini değiştirmek için ateller ve yeterli kiloyu korumalarına yardımcı olacak beslenme programları gibi özel ekipman ve yardımcılara ihtiyaç duyabilir.
Rett sendromunun tedavisi şunları içerir:
- gastrointestinal (reflü, kabızlık ) ve beslenme (zayıf kilo alımı) sorunlarının yönetimi
- skolyoz gözetimi
- yıllık EKG ile uzun QT sendromunun gözetimi
- özellikle artırıcı iletişim stratejileri ile hastanın iletişim becerilerinin arttırılması
- ebeveyn danışmanlığı
- sosyal ilaçları değiştirmek
- uyku yardımcıları
- seçici serotonin geri alım inhibitörleri (SSRI'lar)
- anti-psikotikler (kendine zarar verme davranışları için)
- uzun QT sendromu için beta blokerler
- mesleki terapi , konuşma terapisi ve fizik tedavi
Ani kardiyak ölüm riskinin artması nedeniyle, yıllık tarama EKG'sinde uzun QT sendromu bulunduğunda, beta bloker gibi bir anti-aritmik ile tedavi edilir . Fenitoinin bir beta blokerden daha etkili olabileceğine dair bazı kanıtlar vardır .
prognoz
Patojenik MECP2 mutasyonlarına sahip erkekler , bir veya daha fazla fazladan X kromozomu veya somatik mozaikliği olmadıkça, genellikle ilk 2 yıl içinde şiddetli ensefalopatiden ölürler .
Bozukluğu olan erkek fetüsler nadiren terme kadar hayatta kalır. Hastalığa neden olan gen X kromozomunda yer aldığından, X kromozomunda bir MECP2 mutasyonu ile doğan bir dişide , aynı genin görünüşte normal bir kopyasına sahip başka bir X kromozomu bulunurken, X kromozomunda mutasyona sahip bir erkekte hiçbir X kromozomu yoktur. diğer X kromozomu, sadece bir Y kromozomu; yani normal bir geni yoktur. Bir MECP2 mutasyonunun neden olduğu anormal proteinlere ek olarak normal proteinler sağlayacak normal bir gen olmadan, XY karyotip erkek fetüsü, hastalığın gelişimini yavaşlatamaz, bu nedenle MECP2 mutasyonuna sahip birçok erkek fetüsün hayatta kalması başarısız olur. .
Ancak MECP2 mutasyonu olan dişiler, onlara daha uzun süre hayatta kalmaları için yeterli normal protein sağlayan mutant olmayan bir kromozoma sahiptir . Araştırmalar, Rett sendromlu erkeklerin , erkeğin XXY karyotipine sahip olduğu Klinefelter sendromundan kaynaklanabileceğini gösteriyor . Bu nedenle, mutant olmayan bir MECP2 geni, başka bir X kromozomu olması gerekir, bir çok durumda hayatta kalmak için Rett's etkilenen embriyo ve embriyo için gerekli olan bir erkek veya kadın.
Bununla birlikte, terme taşınan MECP2 mutasyonu (kadınlarda klasik Rett sendromu ile ilişkili) olan, neonatal ensefalopatiden etkilenen ve 2 yaşından önce ölen 46,XY karyotipli erkeklerin birkaç vakası olmuştur. Kısmen Rett sendromu ile ilişkili MECP2 mutasyonlarına sahip erkek fetüslerin düşük hayatta kalması ve kısmen MECP2 mutasyonlarının neden olduğu belirtiler ile Rett'in neden olduğu belirtiler arasındaki farklılıklar nedeniyle, erkeklerde Rett sendromunun insidansı bilinmemektedir.
Dişiler 40 yıl veya daha fazla yaşayabilir. Rett sendromu ile ilgili laboratuvar çalışmaları aşağıdaki gibi anormallikler gösterebilir:
- 2 yaşından itibaren EEG anormallikleri
- atipik beyin glikolipidleri
- yüksek BOS seviyeleri beta- endorfin ve glutamat
- P maddesinin indirgenmesi
- azalmış BOS sinir büyüme faktörleri seviyeleri
Ölümlerin yüksek bir oranı anidir, ancak çoğunun tanımlanabilir bir nedeni yoktur; bazı durumlarda ölüm, büyük olasılıkla aşağıdakilerin sonucudur:
- spontan beyin sapı disfonksiyonu
- muhtemelen uzun QT sendromu , ventriküler taşikardi veya diğer aritmilere bağlı kalp durması
- nöbetler
- mide delinmesi
Tarih
Viyana'da bir çocuk doktoru olan Andreas Rett , durumu ilk kez 1966'da tanımladı. Yazıları Almanca olduğu için İngilizce konuşulan dünyada yaygın olarak tanınmadı. İsveçli bir çocuk doktoru olan Bengt Hagberg, 1983'te bir İngilizce makale yayınladı ve duruma Rett'in adını verdi. 1999'da Lübnanlı-Amerikalı doktor Huda Zoghbi , duruma neden olan mutasyonu keşfetti.
Araştırma
Normal bir MECP2 geninin düzenlenmiş ekspresyonunu elde etmek için hayvan modellerinde gen tedavisi üzerinde çalışılmaktadır.
Referanslar
Dış bağlantılar
| sınıflandırma | |
|---|---|
| Dış kaynaklar |