Radyum - Radium
 | |||||||||||||||||||||||||||||||
| Radyum | |||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Telaffuz |
/ R eɪ d ı ə m / ( RAY -dee-əm ) |
||||||||||||||||||||||||||||||
| Dış görünüş | gümüşi beyaz metalik | ||||||||||||||||||||||||||||||
| Kütle Numarası | [226] | ||||||||||||||||||||||||||||||
| Periyodik tablodaki radyum | |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
| Atom numarası ( Z ) | 88 | ||||||||||||||||||||||||||||||
| Grup | grup 2 (alkali toprak metalleri) | ||||||||||||||||||||||||||||||
| Dönem | 7. dönem | ||||||||||||||||||||||||||||||
| Engellemek | s bloğu | ||||||||||||||||||||||||||||||
| Elektron konfigürasyonu | [ Rn ] 7s 2 | ||||||||||||||||||||||||||||||
| Kabuk başına elektron | 2, 8, 18, 32, 18, 8, 2 | ||||||||||||||||||||||||||||||
| Fiziki ozellikleri | |||||||||||||||||||||||||||||||
| Faz de STP | sağlam | ||||||||||||||||||||||||||||||
| Erime noktası | 973 K (700 °C, 1292 °F) (tartışmalı) | ||||||||||||||||||||||||||||||
| Kaynama noktası | 2010 K (1737 °C, 3159 °F) | ||||||||||||||||||||||||||||||
| Yoğunluk ( rt yakın ) | 5.5 g / cm ' 3 | ||||||||||||||||||||||||||||||
| Füzyon ısısı | 8.5 kJ/mol | ||||||||||||||||||||||||||||||
| Buharlaşma ısısı | 113 kJ/mol | ||||||||||||||||||||||||||||||
Buhar basıncı
| |||||||||||||||||||||||||||||||
| atomik özellikler | |||||||||||||||||||||||||||||||
| oksidasyon durumları | +2 (kuvvetli bazik oksidesahip olması beklenir) | ||||||||||||||||||||||||||||||
| elektronegatiflik | Pauling ölçeği: 0.9 | ||||||||||||||||||||||||||||||
| iyonlaşma enerjileri | |||||||||||||||||||||||||||||||
| kovalent yarıçap | 221±2 pm | ||||||||||||||||||||||||||||||
| Van der Waals yarıçapı | 283 öğleden sonra | ||||||||||||||||||||||||||||||
| Spektral hatları radyum | |||||||||||||||||||||||||||||||
| Diğer özellikler | |||||||||||||||||||||||||||||||
| Doğal oluşum | çürümeden | ||||||||||||||||||||||||||||||
| Kristal yapı | hacim merkezli kübik (bcc) | ||||||||||||||||||||||||||||||
| Termal iletkenlik | 18,6 W/(m⋅K) | ||||||||||||||||||||||||||||||
| elektrik direnci | 1 µΩ⋅m (20 °C'de) | ||||||||||||||||||||||||||||||
| Manyetik sıralama | manyetik olmayan | ||||||||||||||||||||||||||||||
| CAS numarası | 7440-14-4 | ||||||||||||||||||||||||||||||
| Tarih | |||||||||||||||||||||||||||||||
| keşif | Pierre ve Marie Curie (1898) | ||||||||||||||||||||||||||||||
| İlk izolasyon | Marie Curie (1910) | ||||||||||||||||||||||||||||||
| Radyumun ana izotopları | |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
Radyum a, kimyasal element ile sembolü Ra ve atom numarası Bu altıncı elemandır 88. Grup 2 arasında periyodik tablonun olarak da bilinen, alkalin toprak metalleri . Saf radyum gümüşi beyazdır, ancak havaya maruz kaldığında nitrojenle (oksijen yerine) kolayca reaksiyona girerek siyah bir radyum nitrür (Ra 3 N 2 ) yüzey tabakası oluşturur . Tüm izotoplar radyum yüksek olan radyoaktif en izotop olmak üzere, Radyum-226 , bir sahiptir yarı ömrü 1600 yıllık ve bozunur içine Radon gaz (özellikle izotop Radon-222 ). Radyum bozunduğunda, iyonlaştırıcı radyasyon , floresan kimyasalları uyarabilen ve radyolüminesansa neden olabilen bir yan üründür .
Radyum şeklinde radyum klorid , olduğu keşfedilmiştir ile Marie ve Pierre Curie de çıkarılan cevherden 1898 Jáchymov . Radyum bileşiğini uraninitten çıkardılar ve keşfi beş gün sonra Fransız Bilimler Akademisi'nde yayınladılar . Radyum, 1911'de radyum klorürün elektrolizi yoluyla Marie Curie ve André-Louis Debierne tarafından metalik halde izole edildi .
Doğada radyum, uranyumda ve (daha az ölçüde) toryum cevherlerinde, eser miktarda uraninit tonu başına bir gramın yedide biri kadar küçük miktarlarda bulunur. Radyum canlı organizmalar için gerekli değildir ve radyoaktivitesi ve kimyasal reaktivitesi nedeniyle biyokimyasal süreçlere dahil edildiğinde olumsuz sağlık etkileri olasıdır. Şu anda, nükleer tıpta kullanımı dışında , radyumun ticari bir uygulaması yoktur; eskiden, radyolüminesan cihazlar için radyoaktif bir kaynak olarak ve ayrıca sözde iyileştirici güçleri için radyoaktif şarlatanlıkta kullanılıyordu. Bugün, bu eski uygulamalar artık moda değil çünkü radyumun toksisitesi biliniyor ve radyolüminesan cihazlarda bunun yerine daha az tehlikeli izotoplar kullanılıyor.
Toplu özlellikler
Radyum, bilinen en ağır toprak alkali metaldir ve grubunun tek radyoaktif üyesidir. Fiziksel ve kimyasal özellikleri, daha hafif türdeş baryumuna çok benzer .
Saf radyum, daha hafif türdeşleri olan kalsiyum , stronsiyum ve baryumun hafif sarı bir tonu olmasına rağmen, uçucu gümüşi beyaz bir metaldir . Bu renk tonu havaya maruz kaldığında hızla kaybolur ve siyah bir radyum nitrür tabakası (Ra 3 N 2 ) verir. Bu , erime noktası ya da 700 ° C (1,292 ° F) ya da 960 ° C (1,760 ° F) ve kaynama noktası 1,737 ° C (3,159 ° F) 'dir. Bu değerlerin her ikisi de baryumun değerlerinden biraz daha düşüktür ve grup 2 elementlerindeki periyodik eğilimleri doğrular . Baryum ve alkali metaller gibi , radyum da standart sıcaklık ve basınçta vücut merkezli kübik yapıda kristalleşir : radyum-radyum bağ mesafesi 514.8 pikometredir . Radyum 5.5 bir yoğunluğa sahip g / cm 3 , baryum, yine periyodik eğilimleri teyit daha yüksek; radyum-baryum yoğunluk oranı, iki elementin benzer kristal yapıları nedeniyle, radyum-baryum atomik kütle oranı ile karşılaştırılabilir.
izotoplar
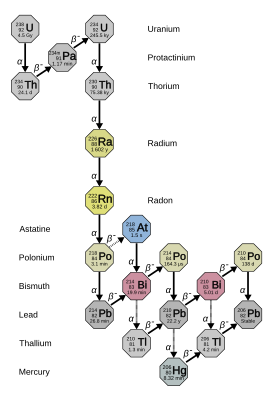
Radyumun bilinen 33 izotopu vardır ve kütle numaraları 202'den 234'e kadardır: hepsi radyoaktiftir . Bunlardan dördü – 223 Ra ( yarı ömür 11.4 gün), 224 Ra (3.64 gün), 226 Ra (1600 yıl) ve 228 Ra (5.75 yıl) – ilkel toryum -232, uranyum- bozunma zincirlerinde doğal olarak meydana gelir. 235 ve uranyum-238 ( 223 Ra uranyum-235'ten, 226 Ra uranyum-238'den ve diğer ikisi toryum-232'den). Yine de bu izotopların yarı ömürleri ilkel radyonüklidler olamayacak kadar kısadır ve doğada yalnızca bu bozunma zincirlerinden bulunur. Doğada yalnızca 237 Np'lik dakika izlerinin bozunma ürünü olarak meydana gelen çoğunlukla yapay 225 Ra (15 d) ile birlikte, bunlar radyumun en kararlı beş izotopudur. Bilinen diğer tüm radyum izotoplarının yarılanma ömrü iki saatin altındadır ve çoğunluğunun yarılanma ömrü bir dakikanın altındadır. En az 12 nükleer izomer rapor edilmiştir; en kararlı olanı radyum-205m olup, yarılanma ömrü 130 ile 230 milisaniye arasındadır; bu hala yirmi dört temel durum radyum izotopundan daha kısadır .
Radyoaktivite çalışmasının erken tarihinde, radyumun farklı doğal izotoplarına farklı isimler verildi. Bu şemada 223 Ra, aktinyum X (AcX), 224 Ra toryum X (ThX), 226 Ra radyum (Ra) ve 228 Ra mezotoryum 1 (MsTh1 ) olarak adlandırıldı. Bunların hepsinin aynı elementin izotopları olduğu anlaşıldığında, bu isimlerin çoğu kullanım dışı kaldı ve "radyum" sadece 226 Ra'yı değil tüm izotopları ifade etmeye başladı . Radyum-226'nın bozunma ürünlerinden bazıları, radyum A'dan radyum G'ye kadar değişen "radyum" da dahil olmak üzere tarihsel adlar aldı ve harf, zincirde yaklaşık olarak 226 Ra'dan ne kadar uzakta olduklarını gösterir . Radyum yayılımı = 222 Rn, RaA = 218 Po, RaB = 214 Pb, RaC = 214 Bi, RaC 1 = 214 Po, RaC 2 = 210 Tl, RaD = 210 Pb, RaE = 210 Bi, RaF = 210 Po ve RaG = 206 Pb.
226 Ra, radyumun en kararlı izotopudur ve yarı ömrü bin yıldan fazla olan uranyum-238'in (4 n + 2) bozunma zincirindeki son izotoptur : neredeyse tüm doğal radyumu oluşturur. Ani bozunma ürünü, çevresel radyum tehlikesinin çoğundan sorumlu olan yoğun radyoaktif soy gaz radonudur (özellikle izotop 222 Rn ). Orantılı olarak daha kısa yarı ömrü nedeniyle , aynı molar miktardaki doğal uranyumdan (çoğunlukla uranyum-238) 2,7 milyon kat daha fazla radyoaktiftir .
Radyum metalinin bir örneği, yaydığı radyasyon ( alfa parçacıkları , beta parçacıkları ve gama ışınları) nedeniyle kendisini çevresinden daha yüksek bir sıcaklıkta tutar . Daha spesifik olarak, doğal radyum (çoğunlukla 226 Ra'dır) çoğunlukla alfa parçacıkları yayar, ancak bozunma zincirindeki diğer adımlar ( uranyum veya radyum serisi ) alfa veya beta parçacıkları yayar ve neredeyse tüm parçacık emisyonlarına gama ışınları eşlik eder.
2013 yılında radyum-224'ün çekirdeğinin armut şeklinde olduğu keşfedildi. Bu, asimetrik bir çekirdeğin ilk keşfiydi.
Kimya
Radyum, baryum gibi, oldukça reaktif bir metaldir ve her zaman +2 grup oksidasyon durumunu sergiler. Renksiz Ra oluşturan 2+ katyon olarak sulu çözelti yüksek olan, bazik ve oluşturmayan kompleksleri kolaylıkla. Bu nedenle çoğu radyum bileşiği basit iyonik bileşiklerdir, ancak göreli etkiler nedeniyle 6s ve 6p elektronlarından (değer 7s elektronlarına ek olarak) katılım beklenir ve Ra F 2 ve Ra At 2 gibi radyum bileşiklerinin kovalent karakterini geliştirir. . Bu nedenle, yarı reaksiyon Ra 2+ (aq) + 2e − → Ra (s) için standart elektrot potansiyeli , baryum için -2,92 V değerinden biraz daha düşük olsa da , -2,916 V'dir , oysa değerler daha önce düzgün bir şekilde vardı. grubu aşağı doğru artırdı (Ca: -2.84 V; Sr: -2.89 V; Ba: -2.92 V). Baryum ve radyum değerleri, daha ağır alkali metaller olan potasyum , rubidyum ve sezyumun değerleriyle hemen hemen aynıdır .
Bileşikler
Katı radyum bileşikleri, radyum iyonları belirli bir renklendirme sağlamadığından beyazdır, ancak radyumun alfa bozunmasından kaynaklanan kendi kendine radyoliz nedeniyle zamanla yavaş yavaş sararır ve daha sonra koyulaşır . Çözünmeyen radyum bileşikleri , tüm baryum, çoğu stronsiyum ve çoğu kurşun bileşikleri ile birlikte çökelir .
Radyum oksit (RaO), oksitlerin diğer alkalin toprak metalleri için yaygın bileşikler olmasına rağmen, varlığından çok iyi bir şekilde karakterize edilmemiştir. Radyum hidroksit (Ra(OH) 2 ), alkalin toprak hidroksitleri arasında en kolay çözünür olandır ve baryum türdeşi baryum hidroksitten daha güçlü bir bazdır . Aynı zamanda aktinyum hidroksit ve toryum hidroksitten daha çözünür : bu üç bitişik hidroksit, amonyak ile çökeltilerek ayrılabilir .
Radyum klorür (RaCl 2 ) renksiz, parlak bir bileşiktir. Radyumun bozunması sırasında yaydığı alfa radyasyonunun kendine verdiği hasar nedeniyle bir süre sonra sarı olur . Az miktarda baryum safsızlıkları bileşiğe gül rengi verir. Baryum klorürden daha az olsa da suda çözünür ve artan hidroklorik asit konsantrasyonu ile çözünürlüğü azalır . Sulu çözeltiden kristalizasyon dihidrat RaCl verir 2 2H · 2 olan baryum analog ile O, izomorf.
Radyum bromür (RaBr 2 ) ayrıca renksiz, parlak bir bileşiktir. Suda radyum klorürden daha fazla çözünür. Radyum klorid gibi, sulu bir çözeltiden kristalizasyon dihidrat RABR verir 2 2H · 2 olan baryum analog ile O, izomorf. Radyum bromür tarafından yayılan iyonlaştırıcı radyasyon , havadaki nitrojen moleküllerini uyararak parlamasını sağlar. Alfa parçacıkları radyum tarafından yayılan hızla nötr olmak üzere iki elektronlar kazanacak helyum içinde birikir ve radyum bromür kristaller zayıflatır. Bu etki bazen kristallerin kırılmasına hatta patlamasına neden olur.
Radyum nitrat (Ra(NO 3 ) 2 ), radyum karbonatın nitrik asit içinde çözülmesiyle elde edilebilen beyaz bir bileşiktir . Nitrik asit konsantrasyonu arttıkça, radyumun kimyasal saflaştırılması için önemli bir özellik olan radyum nitratın çözünürlüğü azalır.
Radyum formları daha hafif türdeş baryum kadar aynı çözünmeyen tuzları çözünmeyen oluşturan sülfat (Raso 4 , en çözünmeyen bilinen sülfat), kromat (RaCrO 4 ), karbonat (RaCO 3 ), iyodat (Ra (IO 3 ) 2 ) , tetrafloroberillat (RaBeF 4 ) ve nitrat (Ra(NO 3 ) 2 ). Karbonat hariç, bunların tümü, karşılık gelen baryum tuzlarından suda daha az çözünür, ancak hepsi baryum karşılıklarına göre yapısaldır. Buna ek olarak, radyum fosfat , oksalat ve sülfit bunlar gibi, aynı zamanda, muhtemelen çözünmezler müşterek tortulandırılması uygun çözünür olmayan bir baryum tuzları ile. Radyum sülfatın büyük çözünmezliği (20 °C'de, 1 kg suda sadece 2.1 mg çözünür ), biyolojik olarak daha az tehlikeli radyum bileşiklerinden biri olduğu anlamına gelir. Ra 2+'nın (148 pm) büyük iyon yarıçapı , yüksek pH'da olmadığında zayıf kompleksleşme ve sulu çözeltilerden radyumun zayıf ekstraksiyonu ile sonuçlanır.
oluşum
Radyumun tüm izotoplarının yarılanma ömrü Dünya'nın yaşından çok daha kısadır , bu nedenle herhangi bir ilkel radyum çok uzun zaman önce bozunur. Radyum gene de ortaya çıkar ortamında izotoplar olarak, 223 Ra, 224 Ra, 226 Ra ve 228 Ra, doğal toryum ve uranyum izotoplarının bozunma zincirinin bir parçasıdır; toryum ve uranyum çok uzun yarı ömre sahip olduğundan, bu yavrular çürümeleriyle sürekli olarak yenilenirler. Bu dört izotoptan en uzun ömürlü olanı , doğal uranyumun bir bozunma ürünü olan 226 Ra'dır (yarı ömür 1600 yıl). Göreceli uzun ömürlülüğü nedeniyle, 226 Ra, elementin en yaygın izotopudur ve yerkabuğunun trilyon başına yaklaşık bir parçasını oluşturur ; aslında tüm doğal radyum 226 Ra'dır. Böylece, radyum, uranyum cevheri uraninit ve diğer çeşitli uranyum minerallerinde çok küçük miktarlarda ve toryum minerallerinde daha da küçük miktarlarda bulunur. Bir ton arasında pitchblende tipik olarak bir yedinci yaklaşık verir gram radyum. Bir kilogram yerkabuğunun 900 hakkında içerdiği pikogram radyumun ve bir litre arasında deniz suyu 89 hakkında içerdiği femtogram radyumun.
Tarih
Radyum edildi keşfedilen tarafından Marie Sklodowska-Curie ve kocası Pierre Curie bir de, 21 Aralık 1898 tarihinde Uraninit dan (pitchblende) numunenin Jáchymov . Minerali daha önce incelerken, Curies ondan uranyumu çıkardı ve kalan malzemenin hala radyoaktif olduğunu buldu. Temmuz 1898'de pitchblend üzerinde çalışırken bizmut benzeri bir elementi izole ettiler ve bu elementin polonyum olduğu ortaya çıktı . Daha sonra, çoğunlukla iki bileşenden oluşan bir radyoaktif karışımı izole ettiler: parlak yeşil alev rengi veren baryum bileşikleri ve daha önce hiç belgelenmemiş karmin spektral çizgileri veren bilinmeyen radyoaktif bileşikler . Curies, radyoaktif bileşiklerin, daha az çözünür olmaları dışında, baryum bileşiklerine çok benzer olduğunu buldu. Bu, Curies'in radyoaktif bileşikleri izole etmesini ve onlarda yeni bir element keşfetmesini mümkün kıldı. Curie'ler keşiflerini 26 Aralık 1898'de Fransız Bilimler Akademisi'ne duyurdular. Radyumun adlandırılması, Modern Latince'de yarıçaptan ( ışın ) türetilen Fransızca radyum kelimesinden yaklaşık 1899'a kadar uzanır : bu, radyumun yayma gücünün tanınmasıydı. ışınlar şeklinde enerji.
Eylül 1910'da Marie buna ve Andre Louis Debierne bir saf olarak izole radyum olduğunu ilan metal aracılığıyla elektroliz saf radyum klorid (RaCl 2 using) çözeltisi cıva katot bir radyum-cıva üreten amalgam . Bu amalgam daha sonra cıvayı çıkarmak için bir hidrojen gazı atmosferinde ısıtıldı ve saf radyum metali kaldı. Aynı yılın ilerleyen saatlerinde, E. Eoler , azidi Ra(N 3 ) 2'nin termal ayrışmasıyla radyumu izole etti . Radyum metali ilk endüstriyel tarafından 20. yüzyılın başlarında üretildi Biraco , bir kuruluşu Birliği Minière du Haut Katanga onun içinde (UMHK) Olen Belçika'da bitki.
Radyoaktivite için ortak tarihsel birim olan curie , 226 Ra'nın radyoaktivitesine dayanmaktadır .
Tarihsel uygulamalar
ışıldayan boya
Radyum eskiden saatler, nükleer paneller, uçak anahtarları, saatler ve gösterge kadranları için kendinden ışıklı boyalarda kullanılıyordu . Radyum boyası kullanan tipik bir kendinden ışıklı saat, yaklaşık 1 mikrogram radyum içerir. 1920'lerin ortalarında, ölmekte olan beş " Radyum Kızı " - saatlerin kadranlarına radyum bazlı parlak boya boyayan kadran ressamları tarafından Birleşik Devletler Radium Şirketi'ne dava açıldı . Kadran ressamlarına, ince bir nokta vermek için fırçalarını yalamaları ve böylece radyum yutmaları talimatı verildi. Radyuma maruz kalmaları, yaralar, anemi ve kemik kanseri gibi ciddi sağlık etkilerine neden oldu . Bunun nedeni, vücudun radyumu kalsiyum olarak işlemesi ve onu , radyoaktivitenin kemik iliğini bozduğu ve kemik hücrelerini mutasyona uğratabileceği kemiklerde biriktirmesidir .
Dava sırasında, şirketin bilim adamları ve yönetiminin kendilerini radyasyonun etkilerinden korumak için önemli önlemler aldığı ancak çalışanlarını korumayı uygun görmediği belirlendi. Ek olarak, birkaç yıl boyunca şirketler, Radium Girls'ün sifilizden muzdarip olduklarında ısrar ederek etkileri örtbas etmeye ve sorumluluktan kaçınmaya çalıştılar . Çalışan refahına yönelik bu tam ihmal, meslek hastalığı iş kanununun formüle edilmesinde önemli bir etkiye sahipti .
Dava sonucunda, radyoaktivitenin olumsuz etkileri yaygın olarak bilinir hale geldi ve radyum kadran boyacılarına uygun güvenlik önlemleri konusunda talimat verildi ve koruyucu giysiler sağlandı. Özellikle, kadran ressamları artık onları şekillendirmek için boya fırçalarını yalamıyordu (bu da bir miktar radyum tuzunun yutulmasına neden oldu). Radyum 1960'lara kadar hala kadranlarda kullanılıyordu, ancak kadran ressamlarında daha fazla yaralanma olmadı. Bu, Radium Girls'e verilen zararın kolayca önlenebileceğini vurguladı.
1960'lardan itibaren radyum boya kullanımı durduruldu. Çoğu durumda, ışıkla uyarılan radyoaktif olmayan floresan malzemelerle ışıklı kadranlar uygulandı; bu tür cihazlar ışığa maruz kaldıktan sonra karanlıkta parlar, ancak parlaklık kaybolur. Karanlıkta uzun süreli kendi kendine parlaklık gerekli olduğunda, daha güvenli radyoaktif promethium -147 (yarı ömür 2,6 yıl) veya trityum (yarı ömür 12 yıl) boya kullanıldı; ikisi de günümüzde kullanılmaya devam etmektedir. Bunlar, radyumdan farklı olarak fosforu zamanla bozmama gibi ek bir avantaja sahipti. Trityum , radyumun nüfuz eden gama radyasyonundan ziyade cilde nüfuz edemeyen ve daha güvenli olarak kabul edilen çok düşük enerjili beta radyasyonu (prometyum tarafından yayılan beta radyasyonundan bile daha düşük enerjili) yayar.
Genellikle askeri uygulamalarda kullanılan 20. yüzyılın ilk yarısından kalma saatler, saatler ve aletler radyoaktif parlak boya ile boyanmış olabilir. Genellikle artık parlak değildirler; bununla birlikte bu, radyumun radyoaktif bozunmasından (yarı ömrü 1600 yıl olan) değil, çinko sülfür floresan ortamının floresansının radyumdan gelen radyasyon tarafından aşınmasından kaynaklanmaktadır. Bu döneme ait cihazlarda genellikle kalın bir yeşil veya sarımsı kahverengi boya tabakasının görünümü, radyoaktif bir tehlikeye işaret eder. Sağlam bir cihazdan gelen radyasyon dozu nispeten düşüktür ve genellikle akut bir risk değildir; ancak boya serbest bırakılırsa ve solunursa veya yutulursa tehlikelidir.
Ticari kullanım
Radyum, sözde iyileştirici güçleri nedeniyle bir zamanlar diş macunu, saç kremleri ve hatta gıda maddeleri gibi ürünlerde katkı maddesiydi. Bu tür ürünler kısa sürede modası geçti ve sağlık üzerinde ciddi olumsuz etkileri olabileceği keşfedildikten sonra birçok ülkede yetkililer tarafından yasaklandı. (Örneğin, "radyum suyu" veya "İçme için Standart Radyum Çözümü" nün Radithor veya Revigator türlerine bakın .) Radyum açısından zengin su içeren kaplıcalar , Misasa, Tottori , Japonya'dakiler gibi hala zaman zaman faydalı olarak lanse ediliyor . ABD'de, 1940'ların sonlarından 1970'lerin başlarına kadar orta kulak problemlerini veya genişlemiş bademcikleri önlemek için çocuklara nazal radyum ışınlaması da uygulandı.
tıbbi kullanım
Radyum (genellikle radyum klorür veya radyum bromür biçiminde ) tıpta radon gazı üretmek için kullanıldı, bu da kanser tedavisi olarak kullanıldı ; örneğin, bu radon kaynaklarının birçoğu 1920'lerde ve 1930'larda Kanada'da kullanıldı. Bununla birlikte, 1900'lerin başında kullanılan birçok tedavi, radyum bromür maruziyetinin neden olduğu zararlı etkiler nedeniyle artık kullanılmamaktadır. Bu etkilerin bazı örnekleri anemi , kanser ve genetik mutasyonlardır . Daha az maliyetli ve daha büyük miktarlarda bulunan 60 Co gibi daha güvenli gama yayıcılar , bu uygulamada geçmişteki radyum kullanımının yerini almak için günümüzde genellikle kullanılmaktadır.
1900'lerin başlarında, biyologlar mutasyonları indüklemek ve genetiği incelemek için radyumu kullandılar . 1904 gibi erken bir tarihte, Daniel MacDougal, ani büyük mutasyonlara neden olup olmayacağını ve büyük evrimsel değişimlere neden olup olmayacağını belirlemek için radyumu kullandı. Thomas Hunt Morgan , beyaz gözlü meyve sinekleriyle sonuçlanan değişiklikleri indüklemek için radyum kullandı. Nobel ödüllü biyolog Hermann Muller , daha uygun fiyatlı röntgen deneylerine geçmeden önce radyumun meyve sineği mutasyonları üzerindeki etkilerini kısaca inceledi.
Johns Hopkins Hastanesi'nin kurucu doktorlarından biri olan Howard Atwood Kelly , kanseri tedavi etmek için radyumun tıbbi kullanımında büyük bir öncüydü. İlk hastası 1904'te ameliyattan kısa bir süre sonra ölen kendi teyzesiydi. Kelly'nin çeşitli kanserleri ve tümörleri tedavi etmek için aşırı miktarda radyum kullandığı biliniyordu. Sonuç olarak, bazı hastaları radyuma maruz kalmaktan öldü. Radyum uygulama yöntemi, etkilenen bölgenin yakınına bir radyum kapsülü yerleştirmek ve ardından radyum "noktalarını" doğrudan tümöre dikmekti . Bu, rahim ağzı kanseri için orijinal HeLa hücrelerinin konakçısı olan Henrietta Lacks'i tedavi etmek için kullanılan yöntemle aynıydı . Şu anda, bunun yerine daha güvenli ve daha erişilebilir radyoizotoplar kullanılmaktadır.
Üretme
Uranyumun 19. yüzyılın sonlarında büyük ölçekli bir uygulaması yoktu ve bu nedenle büyük uranyum madenleri yoktu. Başlangıçta uranyum cevheri için tek büyük kaynak , Avusturya-Macaristan'daki (şimdi Çek Cumhuriyeti ) Jáchymov'daki gümüş madenleriydi . Uranyum cevheri, madencilik faaliyetlerinin yalnızca bir yan ürünüydü .
Curie, radyumun ilk ekstraksiyonunda, pitchblend'den uranyumun ekstraksiyonundan sonraki kalıntıları kullandı. Uranyum, sülfürik asit içinde çözündürülerek, baryum sülfata benzer, ancak kalıntılarda daha az çözünür olan radyum sülfat bırakarak çıkarıldı . Kalıntılar ayrıca oldukça önemli miktarlarda baryum sülfat içerdi ve bu da radyum sülfat için bir taşıyıcı görevi gördü. Radyum ekstraksiyon işleminin ilk adımları, sodyum hidroksit ile kaynatmayı ve ardından diğer bileşiklerin safsızlıklarını en aza indirmek için hidroklorik asit muamelesini içeriyordu . Kalan tortu daha sonra baryum sülfatı baryum karbonata (radyumu taşıyan) dönüştürmek için sodyum karbonat ile işlendi , böylece hidroklorik asit içinde çözünür hale getirildi. Çözünmeden sonra baryum ve radyum sülfatlar olarak yeniden çökeltildi; bu daha sonra karışık sülfatın daha da saflaştırılması için tekrarlandı. Çözünmeyen sülfit oluşturan bazı safsızlıklar, klorür çözeltisinin hidrojen sülfür ile işlenmesi ve ardından filtre edilmesiyle çıkarıldı. Karışık sülfatlar yeterince saf olduğunda, bir kez daha karışık klorürlere dönüştürüldüler; baryum ve radyum daha sonra bir spektroskop (radyum yeşil baryum çizgilerinin aksine karakteristik kırmızı çizgiler verir) ve elektroskop kullanılarak ilerleme izlenirken fraksiyonel kristalizasyon ile ayrıldı .
Marie ve Pierre Curie tarafından Joachimsthal'daki uranyum cevherinden radyumu izole ettikten sonra, birkaç bilim adamı radyumu küçük miktarlarda izole etmeye başladı. Daha sonra küçük şirketler Joachimsthal madenlerinden maden atıkları satın aldı ve radyumu izole etmeye başladı. 1904'te Avusturya hükümeti madenleri kamulaştırdı ve ham cevher ihracatını durdurdu. Bir süredir radyum kullanılabilirliği düşüktü.
Avusturya tekelinin oluşumu ve diğer ülkelerin radyuma erişme konusundaki güçlü dürtüsü, dünya çapında uranyum cevheri arayışına yol açtı. Amerika Birleşik Devletleri 1910'ların başında lider üretici olarak devraldı. Karnotit içinde kumlar Colorado elemanın bazı sağlar, ancak daha zengin cevherler bulunan Kongo ve alanında Büyük Ayı Gölü ve Great Slave Lake Kuzeybatı Kanada. Yatakların hiçbiri radyum için çıkarılmaz, ancak uranyum içeriği madenciliği karlı hale getirir.
Curies'in işlemi 1940'ta endüstriyel radyum ekstraksiyonu için hala kullanılıyordu, ancak daha sonra fraksiyonlama için karışık bromürler kullanıldı. Uranyum cevherinin baryum içeriği yeterince yüksek değilse, radyumu taşımak için biraz eklemek kolaydır. Bu işlemler yüksek dereceli uranyum cevherlerine uygulandı, ancak düşük dereceli cevherlerle iyi çalışmayabilir.
1990'ların sonlarında bu karışık çökeltme ve iyon değişimi yöntemiyle uranyum cevherinden küçük miktarlarda radyum elde ediliyordu, ancak bugün bunlar yalnızca kullanılmış nükleer yakıttan elde ediliyor. 1954'te, dünya çapındaki toplam saflaştırılmış radyum arzı yaklaşık 5 pound (2.3 kg) idi ve bugün hala bu aralıktayken, yıllık saf radyum bileşiklerinin üretimi bugün toplamda sadece 100 g civarındadır. Başlıca radyum üreten ülkeler Belçika, Kanada, Çek Cumhuriyeti, Slovakya , Birleşik Krallık ve Rusya'dır . Üretilen radyum miktarları her zaman nispeten küçüktü; örneğin, 1918'de Amerika Birleşik Devletleri'nde 13.6 g radyum üretildi. Metal, 1200 °C'de bir vakumda alüminyum metal ile radyum oksitin indirgenmesiyle izole edilir.
Modern uygulamalar
Atomik, moleküler ve optik fizik araştırması
Radyum, atomik, moleküler ve optik fizik alanında artan bir kullanım görüyor . Simetri kırma kuvvetleri , radyumu en ağır alkali toprak elementi yapan ile orantılıdır ve yeni fiziği standart modelin ötesinde sınırlamak için çok uygundur. Radyum-225 gibi bazı radyum izotopları, Hg'ye kıyasla iki ila üç büyüklük sırası ile yeni fiziği ihlal eden yük paritesine duyarlılığı artıran sekiz kutuplu deforme parite çiftlerine sahiptir .
Radyum ayrıca tuzaklanmış bir iyon optik saat için umut vericidir . Radyum iyonu, optik bir saatte saat geçişi olarak hizmet edebilecek zemin durumundan iki althertz-hat genişliği geçişine sahiptir . Ek olarak, saat çalışması için gerekli tüm geçişler doğrudan diyot lazerler ile adreslenebildiğinden, radyum taşınabilir bir optik saat için özellikle uygun olabilir.
Radyumun kararlı izotopları olmamasına rağmen, bir King planında yüksek hassasiyetle karşılaştırılabilecek, bir dakikadan uzun yarı ömürleri olan on bir radyum izotopu vardır. İzotop kaymalar temel durum, ya da üzerinde radyum iyon subhertz-çizgi genişliği geçişler ya yüksek hassasiyetle ölçülebilir için nötr radyum olarak intercombination hattı. Böyle bir King planındaki herhangi bir potansiyel doğrusal olmama derecesi, standart modelin ötesinde yeni fiziğe sınırlar koyabilir.
Radyumun birkaç pratik kullanımından bazıları, radyoaktif özelliklerinden türetilmiştir. Kobalt-60 ve sezyum-137 gibi daha yakın zamanda keşfedilen radyoizotoplar , bu sınırlı kullanımlarda bile radyumun yerini almaktadır, çünkü bu izotopların birçoğu daha güçlü yayıcılardır, ele alınması daha güvenlidir ve daha konsantre biçimde mevcuttur.
223 Ra izotopu ( Xofigo ticari adı altında ), tıpta kemik metastazının kanser tedavisi olarak kullanılmak üzere 2013 yılında Amerika Birleşik Devletleri Gıda ve İlaç Dairesi tarafından onaylanmıştır . Xofigo ile tedavinin ana endikasyonu, bu alfa-yayıcı radyofarmasötiğin olumlu özelliklerinden dolayı kastrasyona dirençli prostat kanserinden kemik metastazlarının tedavisidir. 225 Ra, kızlarından biri olarak radon içermeyen, makul derecede uzun ömürlü tek radyum izotopu olduğu için, terapötik ışınlama ile ilgili deneylerde de kullanılmıştır.
Radyum, günümüzde X-ray görüntülemeye benzer şekilde kusurlu metalik parçaları kontrol etmek için bazı endüstriyel radyografi cihazlarında radyasyon kaynağı olarak hala kullanılmaktadır . Berilyum ile karıştırıldığında , radyum bir nötron kaynağı görevi görür . Radyum-berilyum nötron kaynakları bugün bile hala bazen kullanılmaktadır, ancak polonyum gibi diğer malzemeler artık daha yaygındır: Rusya'da yıllık olarak 1.850 Ci (68 TBq) bireysel aktiviteye sahip yaklaşık 1500 polonyum-berilyum nötron kaynağı kullanılmıştır . Bu RaBeF 4 tabanlı (α, n), nötron kaynakları nötronlar yüksek sayıda rağmen kaldırıldı edilmiştir yaydıkları (1.84 x 10 6 lehine saniyede nötron) 241 Am -Hemen kaynağa. Bugün, izotop 226 Ra esas olarak oluşturmak için kullanılan 227 Ac tarafından nötron ışınlaması bir nükleer reaktör içinde.
Tehlikeler
Radyum oldukça radyoaktiftir ve onun en yakın kızı radon gazı da radyoaktiftir. Yutulduğunda, yutulan radyumun %80'i dışkı yoluyla vücudu terk ederken, kalan %20'si ise çoğunlukla kemiklerde birikerek kan dolaşımına girer . Radyuma iç veya dış maruziyet, kansere ve diğer rahatsızlıklara neden olabilir, çünkü radyum ve radon, bozunmaları üzerine hücreleri öldüren ve mutasyona uğratan alfa ve gama ışınları yayar . Zamanında Manhattan Projesi 1944 yılında, işçiler için "tolerans dozu" mideye radyumun 0.1 mikrogram olarak belirlendi.
Radyumun biyolojik etkilerinden bazıları, elementin keşfinden iki yıl sonra 1900'de bildirilen ilk "radyum-dermatit" vakasını içerir. Fransız fizikçi Antoine Becquerel altı saat boyunca yelek cebinde küçük bir radyum ampulü taşıdı ve derisinin ülserleştiğini bildirdi . Pierre ve Marie Curie radyasyondan o kadar etkilendiler ki, onun hakkında daha fazla şey öğrenmek için kendi sağlıklarını feda ettiler. Pierre Curie, on saat boyunca koluna radyumla dolu bir tüp taktı, bu da bir cilt lezyonunun ortaya çıkmasına neden oldu ve radyumun sağlıklı dokuya saldırdığı gibi kanserli dokuya da saldırmak için kullanıldığını düşündürdü. Marie Curie'nin aplastik anemi nedeniyle ölümünden radyum kullanımı sorumlu tutuldu . Önemli miktarda radyum tehlikesi, kızı radonundan gelir: bir gaz olduğundan vücuda ana radyumdan çok daha kolay girebilir.
Bugün 226 Ra, radyoelementlerin en zehirlisi olarak kabul edilir ve 222 Rn'nin çevreye kaçmasını önlemek için önemli miktarda hava akımı sirkülasyonu olan sıkı eldivenli kutularda işlenmelidir . Radyum çözeltileri içeren eski ampuller dikkatli bir şekilde açılmalıdır çünkü suyun radyolitik bozunması hidrojen ve oksijen gazının aşırı basıncına neden olabilir. Dünyanın en büyük 226 Ra konsantrasyonu , Niagara Şelalesi, New York'un yaklaşık 9,6 mil (15,4 km) kuzeyindeki Geçici Atık Muhafaza Yapısında depolanır .
Ayrıca bakınız
Notlar
Referanslar
bibliyografya
- Kirby, HW; Salutsky, Murrell L. (1964). Radyumun Radyokimyası (PDF) . Ulusal Akademiler Basını.
- Greenwood, Norman N. ; Earnshaw, Alan (1997). Elementlerin Kimyası (2. baskı). Butterworth-Heinemann . ISBN'si 978-0-08-037941-8.
daha fazla okuma
- Albert Stwertka (1998). Öğeler Kılavuzu – Gözden Geçirilmiş Baskı . Oxford Üniversitesi Yayınları. ISBN'si 978-0-19-508083-4.
- Denise Grady (6 Ekim 1998). "Karanlıkta Bir Parıltı ve Bilimsel Tehlikede Bir Ders" . New York Times . Erişim tarihi: 25 Aralık 2007 .
- Dadı Fröman (1 Aralık 1996). "Marie ve Pierre Curie ve Polonyum ve Radyumun Keşfi" . Nobel Vakfı . Erişim tarihi: 25 Aralık 2007 .
- Macklis, RM (1993). "Büyük radyum skandalı". Bilimsel Amerikalı . 269 (2): 94–99. Bibcode : 1993SciAm.269b..94M . doi : 10.1038/scientificamerican0893-94 . PMID 8351514 .
- Clark, Claudia (1987). Radyum Kızları: Kadınlar ve Endüstriyel Sağlık Reformu, 1910–1935 . Kuzey Karolina Üniversitesi Yayınları. ISBN'si 978-0-8078-4640-7.
- Marie Curie (1921), Radyumun Keşfi (1. baskı), Poughkeepsie: Vassar College , Wikidata Q22920166
Dış bağlantılar
- "Yanal Bilim: Radyumun Keşfi" . 8 Temmuz 2012'de Arşivlenen orijinal 9 Mart 2016 tarihinde . 13 Mayıs 2017'de alındı .
- Oklahoma'daki Radyum Su Banyosu Fotoğrafları
- NLM Tehlikeli Maddeler Veri Bankası – Radyum, Radyoaktif
- Nükleer Sorunlar için Alsos Dijital Kütüphanesi'nden radyum için kaynakça Açıklamalı Arşivlenen de 25 Haziran 2019 Wayback Machine
- Radyum de video Periyodik Tablo (Nottingham Üniversitesi)













