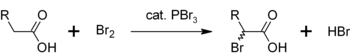Fosfor tribromür - Phosphorus tribromide

|
|

|
|

|
|
| İsimler | |
|---|---|
|
IUPAC adı
fosfor tribromür
|
|
| Diğer isimler
fosfor(III) bromür,
fosfor bromür, tribromofosfin |
|
| tanımlayıcılar | |
|
3B model ( JSmol )
|
|
| Kimyasal Örümcek | |
| ECHA Bilgi Kartı |
100.029.253 |
| AT Numarası | |
|
PubChem Müşteri Kimliği
|
|
| RTECS numarası | |
| ÜNİİ | |
|
CompTox Panosu ( EPA )
|
|
|
|
|
|
| Özellikleri | |
| pBr 3 | |
| Molar kütle | 270.69 g/mol |
| Görünüm | berrak, renksiz sıvı |
| Yoğunluk | 2.852 g / cc 3. |
| Erime noktası | −41,5 °C (−42,7 °F; 231,7 K) |
| Kaynama noktası | 173.2 °C (343.8 °F; 446.3 K) |
| hızlı hidroliz | |
|
Kırılma indisi ( n D )
|
1.697 |
| viskozite | 0,001302 Pas |
| yapı | |
| Köşeli piramit | |
| Tehlikeler | |
| Güvenlik Bilgi Formu | Bakınız: veri sayfası |
|
AB sınıflandırması (DSD) (eski)
|
|
| R cümleleri (modası geçmiş) | R14 , R34 , R37 |
| S-ifadeleri (modası geçmiş) | (S1/2) , S26 , S45 |
| NFPA 704 (ateş elmas) | |
| Bağıntılı bileşikler | |
|
Diğer anyonlar
|
fosfor triflorür fosfor triklorür fosfor triiyodür |
|
Diğer katyonlar
|
azot tribromür arsenik tribromür antimon tribromür |
|
Bağıntılı bileşikler
|
fosfor pentabromid fosfor oksibromid |
| Ek veri sayfası | |
|
Kırılma indisi ( n ), Dielektrik sabiti (ε r ), vb. |
|
|
termodinamik
veriler |
Faz davranışı katı-sıvı-gaz |
| UV , IR , NMR , MS | |
|
Aksi belirtilmedikçe, veriler standart durumdaki malzemeler için verilmiştir (25 °C [77 °F], 100 kPa'da). |
|
|
|
|
| Bilgi kutusu referansları | |
Fosfor tribromür , P Br 3 formülüne sahip renksiz bir sıvıdır . Sıvı, hidroliz nedeniyle nemli havada duman çıkar ve nüfuz edici bir kokuya sahiptir. Bu dönüşüm için laboratuarda kullanılan alkoller için alkil bromürler .
Hazırlık
PBr 3 , kırmızı fosforun brom ile işlenmesiyle hazırlanır . PBr 5 oluşumunu önlemek için fazla fosfor kullanılır :
- 2 P + 3 Br 2 → 2 PBr 3
Reaksiyon yüksek ölçüde ekzotermik olduğu için, genellikle PBR olarak bir seyreltici varlığında gerçekleştirilir 3 .
Reaksiyonlar
Fosfor tribromür gibi PCIs 3 ve PF 3 , bir iki özelliklere sahip Lewis bazı ve bir Lewis asidi . Örneğin, bir Lewis asidi, örn ile bor tribromür bu kararlı 1 olmasıdır: bu Br olarak 1 adüktler 3 B · PBR 3 . Aynı zamanda PBR 3 bir şekilde reaksiyona girebilen bir elektrofil ile, örneğin, kendi reaksiyonların çoğunda ya da Lewis asidi aminler .
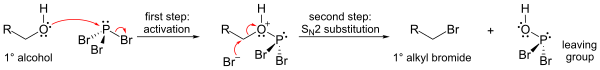
PBR'nin en önemli reaksiyon 3 ile alkollerin bir yerine, OH, bir üretilmesi için bir brom atomu ile bir grup alkil bromür . Üç bromürün tamamı transfer edilebilir.
- PBR 3 + 3 ROH → 3 RBr + HP (O) (OH) 2
(Birincil alkol için gösterilen) mekanizma, bir fosfor ester oluşumunu kapsayan bir takiben, (iyi bir ayrılan grubu oluşturmak için) S , N 2 ikame .
Çünkü S K 2 ikame aşamasında, reaksiyon genellikle iyi çalışır primer ve sekonder alkoller , ancak tersiyer alkoller başarısız olur. Reaksiyona giren karbon merkezi kiral ise, reaksiyon genellikle, bir S N2 reaksiyonunda olduğu gibi, alkol alfa karbonunda konfigürasyonun ters çevrilmesiyle meydana gelir .
Benzer bir reaksiyonda, pBR 3 de dönüştürür karboksilik asitler için asil bromürler .
- PBR 3 + 3 R-COOH → 3 RCOBr + HP (O) (OH) 2
Uygulamalar
Fosfor tribromür ana kullanım birincil ya da ikincil dönüştürülmesi için olan alkoller için alkil bromürler tarif edildiği gibi, yukarıda . PBR 3 genellikle daha yüksek verim veren hidrobromik asit ve sorunlarını önler karbokatyon da örneğin rearrangement- neopentil bromit% 60 verimle alkolden yapılabilir.
PB ^ 'le başka bir kullanımı, 3 ve α-brominasyonu için bir katalizör olarak bir karboksilik asitler . Asil bromürler, açil klorürlere kıyasla nadiren yapılsa da , Hell-Volhard-Zelinsky halojenasyonunda ara ürünler olarak kullanılırlar . Başlangıçta PBR 3 karboksilik asit ile reaksiyona girerek brominasyon karşı daha reaktiftir asil bromür oluşturmak için. Genel süreç şu şekilde temsil edilebilir:
Ticari ölçekte fosfor tribromür, alprazolam , metoheksital ve fenoprofen gibi farmasötiklerin üretiminde kullanılır . Aynı zamanda PhostrEx adı altında pazarlanan güçlü bir yangın söndürme maddesidir .
Önlemler
PBr 3 , toksik olan ve su ve alkollerle şiddetli reaksiyona giren aşındırıcı HBr geliştirir.
- PBr 3 + 3 H 2 O → H 3 PO 3 + 3 HBr
Yan ürün olarak fosfor asidi üreten reaksiyonlarda, damıtma ile çalışırken bunun yaklaşık 160 °C'nin üzerinde ayrışarak hava ile temas halinde patlamalara neden olabilecek fosfin verebileceğini unutmayın .
Referanslar
daha fazla okuma
- Greenwood, Norman N. ; Earnshaw, Alan (1997). Elementlerin Kimyası (2. baskı). Butterworth-Heinemann . ISBN'si 978-0-08-037941-8.
- Lide, DR, ed. (1990). Kimya ve Fizik El Kitabı (71. baskı). Ann Arbor, MI: CRC Press. ISBN'si 978-0849304712.
- Mart, J. (1992). İleri Organik Kimya (4. baskı). New York: Wiley. s. 723 . ISBN'si 978-0471601807.
- Stecher, PG, ed. (1960). Merck İndeksi (7. baskı). Rahway, NJ, ABD: Merck & Co.
- Holmes, RR (1960). "Fosfor, Arsenik ve Antimon Trihalidlerinin Temel Doğasının İncelenmesi". İnorganik ve Nükleer Kimya Dergisi . 12 (3–4): 266–275. doi : 10.1016/0022-1902(60)80372-7 .