periyod - Periodate
 metaperiyodat iyonu
|
|
 ortoperiyodat iyonu
|
|
| İsimler | |
|---|---|
|
Sistematik IUPAC adı
tetraoksoiyodat(1−) heksaoksoiyodat(5−) |
|
| tanımlayıcılar | |
|
3B model ( JSmol )
|
|
| Kimyasal Örümcek | |
|
PubChem Müşteri Kimliği
|
|
| ÜNİİ | |
|
|
|
|
| Özellikler | |
| IO 4 – veya IO 6 5- | |
| Eşlenik asit | periyodik asit |
| Bağıntılı bileşikler | |
|
Diğer anyonlar
|
Perklorat Perbromat Permanganat |
|
Aksi belirtilmedikçe, veriler standart durumdaki malzemeler için verilmiştir (25 °C [77 °F], 100 kPa'da). |
|
| Bilgi kutusu referansları | |
Periodat / p ə r aɪ . ə d eɪ t / iyot ve oksijenden oluşan bir anyondur . İyotun bir dizi oksianyonundan biridir ve +7 oksidasyon durumunda mevcut olan iyot ile serideki en yüksektir. Perklorat gibi diğer perhalojenatların aksine , iki şekilde bulunabilir: metaperiodat IO -
4ve ortoperiyodat IO5−
6. Bu bakımdan komşu gruptan tellurat iyonu ile karşılaştırılabilir . Periyodik asit tuzları olarak da kabul edilebilecek olan periyodatları oluşturmak için bir dizi karşı iyonla birleşebilir .
Periyodatlar Heinrich Gustav Magnus ve CF Ammermüller tarafından keşfedilmiştir ; 1833'te ilk kez periyodik asidi sentezleyen kişi.
sentez
Klasik olarak, periodat en yaygın olarak sodyum hidrojen periodat (Na formunda üretilmiştir 3 H 2 IO 6 ). Bu ticari olarak mevcuttur, ancak iyodatların klor ve sodyum hidroksit ile oksidasyonu ile de üretilebilir . Veya benzer şekilde, brom ve sodyum hidroksit ile oksidasyon yoluyla iyodürlerden :
- NaIO 3 + Cl 2 + 4 NaOH → Na 3 H 2 IO 6 + 2 NaCl + H 2 O
- NaI + 4 Br 2 + 10 NaOH → Na 3 H 2 IO 6 + 8 NaBr + 4 H 2 O
Modern endüstriyel ölçekli üretim, aşağıdaki standart elektrot potansiyeli ile bir PbO 2 anot üzerinde iyodatların elektrokimyasal oksidasyonunu içerir :
Metaperiyodatlar tipik olarak sodyum hidrojen periyodatın nitrik asit ile dehidrasyonu veya ortoperiyodik asidin vakum altında 100 °C'ye ısıtılmasıyla dehidre edilmesiyle hazırlanır.
- Na 3 H 2 IO 6 + 2 HNO 3 → NaIO 4 + 2 NaNO 3 + 2 H 2 O
- H 5 IO 6 → HIO 4 + 2 H 2 O
Ayrıca, hipokloritler gibi diğer güçlü oksitleyici maddelerle işlenerek doğrudan iyodatlardan da üretilebilirler :
Formlar ve dönüşüm
Periyodat, pH'ın bir kontrol faktörü olduğu sulu ortamda çeşitli formlarda bulunabilir . Ortoperiodat, bir dizi asit ayrışma sabitine sahiptir .
H 5 İÇ 6 ⇌ H
4GÇ-
6+ H + p K bir = 3.29 H
4GÇ-
6⇌ H
3GÇ2−
6+ H + p K bir = 8.31 H
3GÇ2−
6⇌ H
2GÇ3−
6+ H + p K bir = 11.60
Orto- ve metaperiyodat formları da dengede bulunur.
-
H
4GÇ-
6⇌ GÇ-
4+ 2 H 2 O, K = 29
Bu nedenle ortoperiyodat bazen metaperiodatın dihidratı olarak anılır , IO şeklinde yazılır.-
4· 2H 2 O ; Bununla birlikte, bu açıklama olarak kesin olarak doğru değildir X-ışını kristalografisi H 5 IO 6 gösterir 5 eşdeğer I-OH grupları.
pH'ın uç noktalarında ek türler oluşabilir. Bazik koşullar altında, diperiyodat (bazen mesoperiodat olarak anılır) oluşturmak için bir dehidrasyon reaksiyonu gerçekleşebilir.
- 2 saat
3GÇ2−
6⇌ H
2ben
2Ö4−
10+ 2 H 2 O, K = 820
Kuvvetli asit koşulları altında periyodik asit, ortoperiyodonyum katyonunu vermek üzere protonlanabilir .
-
H
6GÇ+
6⇌ H 5 IO 6 + H + , p K bir = -0.8
Yapı ve yapıştırma
Hem orto- hem de metaperiyodatta iyot, klasik olarak izin verilenden daha fazla bağ oluşturduğu için hipervalenttir . Bu, bu moleküllerde çift bağın olmadığını doğrulayan datif bağlar açısından açıklanmıştır .
Tam yapıları ortalama orthoperiodates biraz deforme oktahedral geometri ile kabul ancak üzerinde, karşı iyon bağlı olarak değişebilir X-ışını kırınımı 1.89 I-O bağı uzunlukları gösteren Å . Metaperiyodlar, ortalama G-Ç mesafesi 1.78 Å olan çarpık bir tetrahedral geometriyi benimser.
Reaksiyonlar
Bölünme reaksiyonları
Periyodatlar, çeşitli 1,2-difonksiyonelleştirilmiş alkanlar üzerindeki karbon-karbon bağlarını parçalayabilir. Bunun en yaygın örneği , aynı zamanda ilk keşfedilen diol bölünmesidir ( Malaprade reaksiyonu ). Ek olarak dioller , periyodatlar yarabilir 1,2-hidroksi ketonlar , 1,2-diketonlar , α-keto asitler , α-hidroksi asitler , amino asitler , 1,2-amino alkolleri , 1,2-diamin , ve epoksitler için aldehitler, ketonlar ve karboksilik asitler verir.
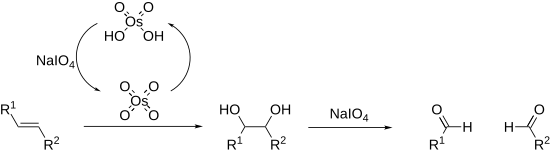
Alkenler ayrıca Lemieux-Johnson oksidasyonunda oksitlenebilir ve parçalanabilir . Bu , periyodat tarafından yerinde yeniden üretilen katalitik bir osmiyum tetroksit yüklemesi kullanır . Genel süreç, ozonolize eşdeğerdir .
Bölünme reaksiyonları, periyodat ester adı verilen siklik bir ara madde aracılığıyla ilerler. Bunun oluşumu pH ve sıcaklıktan etkilenebilir, ancak en çok substratın geometrisinden etkilenir, cis- dioller trans- diollerden önemli ölçüde daha hızlı reaksiyona girer. Reaksiyonlar ekzotermiktir ve tipik olarak 0 °C'de gerçekleştirilir. Periyodat tuzları sadece suda kolayca çözünür olduğundan reaksiyonlar genellikle sulu ortamda gerçekleştirilir. Çözünürlüğün bir sorun olduğu durumlarda, alkollerde çözünür olduğu için periyodik asit kullanılabilir; faz transfer katalizörleri de bifazik reaksiyon karışımlarında etkilidir . Aşırı durumlarda periyodat, benzer bir şekilde reaksiyona giren ve organik çözücülerde çözünen kurşun tetraasetat ile değiştirilebilir ( Criegee oksidasyonu ).
Pek çok beş ve altı üyeli şekerin visinal diolleri olduğu için, periyodat bölünmesi genellikle sakkarit halkalarını modifiye etmek amacıyla moleküler biyokimyada kullanılır . Tarihsel olarak monosakkaritlerin yapısını belirlemek için de kullanılmıştır.
Kağıt üretiminde kullanılan dialdehit nişastasını oluşturmak için periyodat parçalama endüstriyel ölçekte gerçekleştirilebilir .
oksidasyon reaksiyonları
Periyodatlar güçlü oksitleyici ajanlardır . Bu oksidize olabilir katekol için 1,2-benzokinon ve hidrokinon ile 1,4-benzokinon . Sülfitler etkili bir şekilde sülfoksitlere oksitlenebilir . Periyodatlar gibi diğer güçlü inorganik oksitleyicilerden üretmek için yeterince güçlü permanganat , osmium tetroksit ve rutenyum tetroksit .
Niş kullanır
Periyodatlar, belirli rutenyum bazlı oksitler için oldukça seçici dağlayıcılardır .
Mikroskopide kullanılan çeşitli boyama ajanları periyodata dayalıdır (örneğin, periyodik asit-Schiff boyası ve Jones boyası )
Periyodatlar ayrıca piroteknikte kullanım için oksitleyici ajanlar olarak kullanılmıştır . 2013 yılında ABD Ordusu , izleyici mühimmatlarında kullanılmak üzere çevreye zararlı kimyasallar olan baryum nitrat ve potasyum perkloratı sodyum metaperiodat ile değiştireceğini duyurdu .
Diğer oksianyonlar
Periyodat, iyotun -1, +1, +3, +5 veya +7 oksidasyon durumlarını üstlenebildiği bir dizi oksianyonun parçasıdır . Bir dizi nötr iyot oksit de bilinmektedir.
| İyot oksidasyon durumu | -1 | +1 | +3 | +5 | +7 |
|---|---|---|---|---|---|
| İsim | iyodür | hipoiyodit | iyodür | iyodat | periyodat |
| formül | ben - | GÇ - |
GÇ- 2 |
GÇ- 3 |
GÇ- 4veya GÇ5− 6 |
| Yapı |

|
|
|