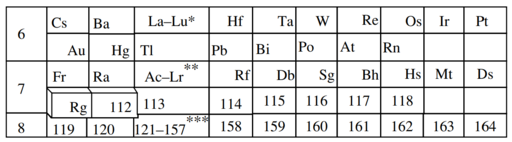
Genişletilmiş periyodik tablo - Extended periodic table
| Bir kısmı bir dizi üzerinde |
| Periyodik tablo |
|---|
Bir genişletilmiş periyodik tablo kurguladığı kimyasal elementlerin şu anda bilinen ötesinde periyodik tablonun kadar ve kanıtlanmış oganesson yedinci tamamlar, dönem içinde (satır) periyodik tablonun en atom numarası ( Z ) 2021 118. As, hiçbir elemanı oganesson'dan daha yüksek bir atom numarası başarıyla sentezlendi; sekizinci periyottaki ve sonrasındaki tüm unsurlar bu nedenle tamamen varsayımsal kalır.
Bundan daha yüksek atom numaralarına sahip başka elementler keşfedilirse, ilgili elementlerin özelliklerinde periyodik olarak tekrarlanan eğilimleri göstermek için (mevcut periyotlarda olduğu gibi) ek periyotlara yerleştirilecektir. Ek periyotların, her periyotta kısmen dolu g- orbitalleri olan en az 18 element içeren g-blok adı verilen ek bir elemente sahip oldukları hesaplandığından, yedinci periyottan daha fazla sayıda element içermesi beklenir . Bir Sekiz-dönem tablo bu bloğu içeren tarafından önerildi Glenn T. Seaborg g bloğun birinci eleman olurdu, böylece atom numarası 121 sahip olabilir ve 1969 yılında sistematik ismi unbiunium . Birçok araştırmaya rağmen, bu bölgede hiçbir element doğada sentezlenmemiş veya keşfedilmemiştir.
Atom yapısının kuantum mekaniksel açıklamalarındaki yörünge yaklaşımına göre , g bloğu kısmen dolu g-orbitalleri olan elementlere karşılık gelir, ancak spin-yörünge birleştirme etkileri, yüksek atom numaralı elementler için yörünge yaklaşımının geçerliliğini büyük ölçüde azaltır. Seaborg'un uzatılmış periyot versiyonu, göreli etkileri hesaba katmadığı için, daha hafif elementler tarafından belirlenen kalıbı takip eden daha ağır elementlere sahipken, göreceli etkileri hesaba katan modeller yoktur. Pekka Pyykkö ve Burkhard Fricke , Z = 172'ye kadar olan elementlerin konumlarını hesaplamak için bilgisayar modellemesini kullandılar ve birkaçının Madelung kuralından çıkarıldığını buldular . 120'nin ötesinde elementlerin kimyasal ve fiziksel özelliklerinin tahminlerindeki belirsizlik ve değişkenliğin bir sonucu olarak, şu anda genişletilmiş periyodik tabloya yerleştirilmeleri konusunda bir fikir birliği yoktur.
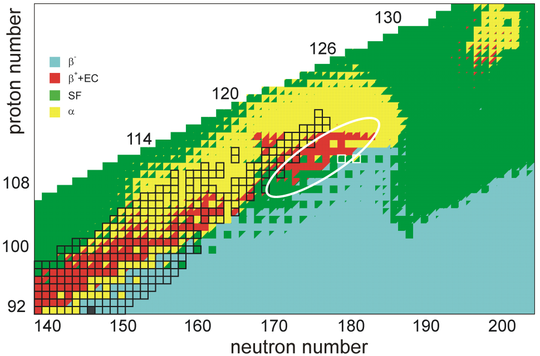
Bu bölgedeki elementlerin radyoaktif bozunma açısından oldukça kararsız olmaları ve alfa bozunmasına veya son derece kısa yarı ömürleri olan kendiliğinden fisyona uğramaları muhtemeldir , ancak element 126'nın fisyona dirençli ancak alfaya dirençli olmayan bir kararlılık adası içinde olduğu varsayılır. çürümek. Kapalı nükleer kabuklardan kaynaklanan stabilize edici etkilerin kapsamı belirsiz olsa da, 164. element etrafında teorize edilenler dahil olmak üzere, bilinen elementlerin ötesinde başka stabilite adaları da mümkün olabilir . Beklenen kararlılık adasının ötesinde kaç elementin fiziksel olarak mümkün olduğu, 8. periyodun tamamlanıp tamamlanmadığı veya bir periyodun olup olmadığı açık değildir. Uluslararası Temel ve Uygulamalı Kimya Birliği (IUPAC), bir elementin ömrü boyunca var olduğunu tanımlar. 10-14 saniyeden (0.01 pikosaniye veya 10 femtosaniye) daha uzundur , bu da çekirdeğin bir elektron bulutu oluşturması için geçen süredir .
1940 gibi erken bir tarihte, göreli Dirac denkleminin basit bir yorumunun , Z > 1/α ≈ 137'deki elektron orbitalleriyle ilgili problemlerle karşılaştığı , bu da nötr atomların element 137'nin ötesinde var olamayacağını ve elementlere dayalı periyodik bir tablonun elektron orbitallerinde bu nedenle bu noktada bozulur. Öte yandan, daha titiz bir analiz , 1s alt kabuğunun Dirac denizine daldığı yerde benzer limiti Z ≈ 173 olarak hesaplar ve bunun yerine, 173. elementin ötesinde varolamayan nötr atomlar değil, çıplak çekirdekler olur, böylece hiçbir şey ortaya çıkmaz. Periyodik sistemin daha da genişletilmesine engel. Bu kritik atom numarasının ötesindeki atomlara süper kritik atomlar denir .
Tarih
Aktinitlerin ötesinde daha ağır elementlerin var olduğu ilk olarak 1895 gibi erken bir tarihte Danimarkalı kimyager Hans Peter Jørgen Julius Thomsen'in toryum ve uranyum'un kimyasal olarak aktif olmayan ve atom ağırlığı 292 olan bir elementte sona erecek olan 32 elementli bir periyodun parçasını oluşturduğunu öngördüğü zaman önerildi. Oganesson'un ilk ve tek keşfedilen izotopu için bugün bilinen 294'ten çok uzak değil ). 1913'te İsveçli fizikçi Johannes Rydberg benzer şekilde radondan sonraki soy gazın 118 atom numarasına sahip olacağını ve tam olarak Aufbau'nun tam olarak Z = 168, 218, 290, 362 ve 460'ta daha ağır radon türdeşlerini türeteceğini öngördü. ilke , onların olacağını tahmin ederdi. Niels Bohr 1922 yılında bu sonrakinin elektronik yapısını tahmin asil gazın en Z = 118, ve onlar da kararsız oldukları için uranyum ötesi element doğada görülmedi nedeni olduğunu ileri sürdü. Alman fizikçi ve mühendis Richard Swinne , 1926'da , bir istikrar adasının modern tahminlerini öngördüğü transuranik elementler hakkında tahminler içeren bir inceleme makalesi yayınladı (terimi o icat etmiş olabilir) : 1914'ten beri yarı ömürlerin olmaması gerektiğini varsaymıştı. atom numarasıyla kesin olarak azalır, ancak bunun yerine Z = 98-102 ve Z = 108-110'da daha uzun ömürlü bazı elementler olabileceğini öne sürdü ve bu tür elementlerin Dünya'nın çekirdeğinde , demir göktaşlarında veya göktaşlarında var olabileceğini öne sürdü . Grönland'ın sözde kozmik kökenlerinden kilitli kaldıkları buzulları . 1955'te bu elementlere süper ağır elementler adı verildi .
Keşfedilmemiş süper ağır elementlerin özellikleriyle ilgili ilk tahminler, nükleer kabuk kavramının ilk kez keşfedildiği ve 126. element etrafında bir kararlılık adasının var olduğu teorileştirildiği 1957'de yapıldı. 1967'de, daha titiz hesaplamalar yapıldı ve kararlılık adası o zamanlar keşfedilmemiş flerovium'da (element 114) merkezlendiği teorileştirildi ; bu ve sonraki çalışmalar, birçok araştırmacıyı doğada süper ağır elementleri aramaya veya hızlandırıcılarda sentezleme girişiminde bulunmaya motive etti. 1970'lerde süper ağır elementler için birçok arama yapıldı ve hepsi olumsuz sonuçlarla sonuçlandı. Aralık 2018 itibariyle, unbitrium ( Z = 123) hariç, unbiseptium ( Z = 127) dahil olmak üzere her element için sentez yapılmaya çalışıldı , en başarılı şekilde sentezlenen element 2002'de oganesson ve en son keşif tennessine'ydi. 2010 yılında.
Bazı süper ağır elementlerin yedi periyotlu periyodik tablonun ötesinde yer aldığı tahmin edildiğinden, bu elementleri içeren ek bir sekizinci periyot ilk olarak 1969'da Glenn T. Seaborg tarafından önerildi . Bu model, yerleşik elementlerdeki modeli sürdürdü ve yeni bir g-bloğunu tanıttı ve 121. elementte başlayan süperaktinid serileri, bilinen periyotlara kıyasla 8. periyotta element sayısını artırıyor. Bununla birlikte, bu erken hesaplamalar, periyodik eğilimleri bozan ve basit ekstrapolasyonu imkansız kılan göreli etkileri göz önünde bulundurmada başarısız oldu. 1971'de Fricke, periyodik tabloyu Z = 172'ye kadar hesapladı ve bazı elementlerin gerçekten de yerleşik düzeni bozan farklı özelliklere sahip olduğunu keşfetti ve Pekka Pyykkö tarafından 2010 yılında yapılan bir hesaplama da birkaç elementin beklenenden farklı davranabileceğini kaydetti. Daha ağır elementlerin giderek daha kararsız olduğu tahmin edildiğinden, periyodik tablonun bilinen 118 elementin ötesine ne kadar uzanabileceği bilinmiyor. Glenn T. Seaborg , pratik olarak, nükleer istikrarsızlık nedeniyle periyodik tablonun sonunun Z = 120 civarında olabileceğini öne sürdü .
Genişletilmiş bir periyodik tablonun tahmin edilen yapıları
Şu anda , periyodik tablodaki atom numarası 120'nin ötesindeki elementlerin yerleştirilmesi konusunda bir fikir birliği yoktur .
Tüm bu varsayımsal keşfedilmemiş elementler , element keşfedilene, onaylanana ve resmi bir isim onaylanana kadar kullanım için genel bir isim oluşturan Uluslararası Temel ve Uygulamalı Kimya Birliği (IUPAC) sistematik element ismi standardı tarafından adlandırılır. Bu isimler genellikle literatürde kullanılmaz ve atom numaralarıyla anılır; bu nedenle, eleman 164 genellikle "unhexquadium" veya "Uhq" (IUPAC sistematik adı ve sembolü) olarak değil, "164", "(164)" veya "E164" sembollü "eleman 164" olarak adlandırılacaktır.
Aufbau prensibi
118 numaralı elemanda, 1s, 2s, 2p, 3s, 3p, 3d, 4s, 4p, 4d, 4f, 5s, 5p, 5d, 5f, 6s, 6p, 6d, 7s ve 7p orbitallerinin aşağıdakilerle doldurulduğu varsayılır: kalan yörüngeler doldurulmamış. Aufbau ilkesinden basit bir ekstrapolasyon , sekizinci sıranın orbitalleri 8s, 5g, 6f, 7d, 8p sırasına göre doldurmasını öngörür; ancak 120. elementten sonra elektron kabuklarının yakınlığı basit bir tabloya yerleştirmeyi sorunlu hale getirir.
| 1 | 1 saat |
2 O |
||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2 | 3 Litre |
4 ol |
5 B |
6 ° C |
7 N |
8 O |
9 F |
10 Ne |
||||||||||||||||||||||||||||||||||||||||||
| 3 | 11 Na |
12 mg |
13 Al |
14 Si |
15 P |
16 S |
17 Cl |
18 Aralık |
||||||||||||||||||||||||||||||||||||||||||
| 4 | 19 bin |
20 Ca |
21 x |
22 Ti |
23 V |
24 Cr |
25 milyon |
26 Fe |
27 Ortak |
28 Ni |
29 Cu |
30 çinko |
31 Ga |
32 Ge |
33 Olarak |
34 Saat |
35 Br |
36 Kr |
||||||||||||||||||||||||||||||||
| 5 | 37 Rb |
38 Sn |
39 Y |
40 Zr |
41 Nb |
42 Ay |
43 Tc |
44 Ru |
45 Rh |
46 Kişi |
47 Ag |
48 Cd |
49 İçinde |
50 sn |
51 Sb |
52 Te |
53 ben |
54 Xe |
||||||||||||||||||||||||||||||||
| 6 | 55 C |
56 Ba |
57 La |
58 Yıl |
59 Pr |
60 Nd |
61 Öğleden sonra |
62 Sm |
63 AB |
64 Gd |
65 yemek kaşığı |
66 Yıl |
67 Ho |
68 Er |
69 Tm |
70 Yb |
71 Lu |
72 Hf |
73 Ta |
74 B |
75 Yeniden |
76 İşletim Sistemi |
77 Ir |
78 Pt |
79 Au |
80 Hg |
81 TL |
82 Pb |
83 Bi |
84 Po |
85 Saat |
86 Mil |
||||||||||||||||||
| 7 | 87 Fr |
88 Ra |
89 Ac |
90 Bin |
91 Pa |
92 U |
93 Np |
94 Pu |
95 am |
96 cm |
97 milyar |
98 Cf |
99 Es |
100 Fm |
101 Md |
102 Hayır |
103 litre |
104 Rf |
105 Db |
106 Sg |
107 Bh |
108 Hs |
109 Mt |
110 D |
111 Rg |
112 Cn |
113 Nh |
114 Fl |
115 Mc |
116 Sv |
117 Ts |
118 Og |
||||||||||||||||||
| 8 | 119 Uue |
120 ubn |
121 Übü |
122 Ubb |
123 Ubt |
124 Ubq |
125 Ubp |
126 Ubh |
127 Ub |
128 Ubo |
129 Ube |
130 Un |
131 Utu |
132 Utb |
133 Ut |
134 Utq |
135 ÜÇ |
136 Uth |
137 Uts |
138 Uto |
139 Ute |
140 Uqn |
141 uq |
142 Uqb |
143 Uqt |
144 Uqq |
145 Uqp |
146 Uqh |
147 Uq |
148 Uqo |
149 Uqe |
150 Upn |
151 Yukarı |
152 Yukarı |
153 Yukarı |
154 Yukarı |
155 Yukarı |
156 Yukarı |
157 Ups |
158 Yukarı |
159 Yukarı |
160 Ahh |
161 Uhu |
162 Uhb |
163 Uht |
164 Uhq |
165 Uhp |
166 ahh |
167 Ahs |
168 uho |
Pyykkö
Tüm modeller, daha hafif öğeler tarafından oluşturulan deseni takip eden daha yüksek öğeleri göstermez. Pekka Pyykkö , örneğin, kullanılan bilgisayar modelleme kadar elementlerin konumlarını hesaplamak için Z = 172 ve 2011 yılında yayınlanan bir makalede bunların olası kimyasal özellikleri O birkaç elemanları yerinden edildi bulundu Madelung enerji sipariş kuralları sonucunda örtüşen yörüngeler; bu, ağır elementlerde rölativistik etkilerin artan rolünden kaynaklanmaktadır .
frikik
1971'de yayınladığı bir makalede 184. elemente kadar hesaplamalar yapan Burkhard Fricke ve diğerleri de göreli etkiler sonucunda bazı unsurların Aufbau ilkesinden uzaklaştığını bulmuştur.
| H | o | |||||||||||||||||||||||||||||||
| Li | olmak | B | C | n | Ö | F | Ne | |||||||||||||||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| K | CA | sc | Ti | V | cr | Mn | Fe | ortak | Ni | Cu | çinko | ga | Ge | Olarak | Gör | Br | Kr | |||||||||||||||
| Rb | Bay | Y | Zr | not | ay | Tc | Ru | Rh | PD | Ag | CD | İçinde | Sn | Sb | Te | ben | Xe | |||||||||||||||
| C'ler | Ba | La | CE | Halkla İlişkiler | Nd | Öğleden sonra | Sm | AB | gd | yemek | dy | Ho | Er | Tm | yb | lu | hf | Ta | W | Tekrar | İşletim sistemi | ir | nokta | Au | Hg | TL | Pb | Bi | po | NS | Rn | |
| Cum | Ra | AC | NS | baba | sen | np | Pu | NS | Santimetre | bk | bkz. | Es | FM | md | Numara | lr | Rf | db | Çavuş | bh | hs | dağ | Ds | Rg | Müşteri | Nh | fl | Mc | Sv. | Ts | og | |
| 119 | 120 | 121 | 122–141 | 142 | 143 | 144 | 145 | 146 | 147 | 148 | 149 | 150 | 151 | 152 | 153 | 154 | 155 | 156 | 157 | 158 | 159 | 160 | 161 | 162 | 163 | 164 | ||||||
| 165 | 166 | 167 | 168 | 169 | 170 | 171 | 172 |
Nefedov
Nefedov , Trzhaskovskaya ve Yarzhemskii 164'e kadar hesaplamalar yaptılar (sonuçlar 2006'da yayınlandı). Pyykkö'nün yanı sıra Fricke ve arkadaşlarının aksine, 158 ila 164 arasındaki elementleri 4 ila 10 arasındaki grupların homologları olarak kabul ettiler ve 6 ila 12 arasındaki değil, elektron konfigürasyonlarının 5. periyot geçiş metalleriyle benzerliklerine dikkat çektiler. Öğeler 111 ve 112, Au ve Hg'den farklı konfigürasyonları yansıtmak için düzlemden yer değiştirir.
kulşa
Hesaplamalı kimyager Andrey Kulsha, genişletilmiş periyodik tablonun iki biçimini önerdi. Muhtemel kimyasal özelliklerine dayanarak, 157-172 elementleri, beşinci periyotta itriyum yoluyla ksenon yoluyla sekizinci periyot türdeşleri olarak yerleştirilir; bu, Nefedov ve diğerlerinin 2006 hesaplamalarıyla uyumludur. Kulsha'nın ilk önerisinde (2011, Pyykkö'nün makalesi yayınlandıktan sonra), 121-138 ve 139-156 öğeleri , çekirdeğe 5g 18 alt kabuğunun eklenmesiyle ilişkili iki ayrı satır (birlikte "geçiş öğeleri" olarak adlandırılır) olarak yerleştirilir , sırasıyla lantanitleri ve aktinitleri taklit ettikleri için. İkinci önerisinde (2016), 121–142 elementleri bir g bloğu oluştururken (5g aktivitesine sahip oldukları için), 143–156 elementler nobelium aracılığıyla aktinyumun altına yerleştirilmiş bir f bloğu oluşturur.
Keşfedilmemiş elementleri arar
sentez denemeleri
Unbitrium hariç, unbiseptiuma kadar olan periyot 8 elementini sentezlemek için başarısız girişimlerde bulunulmuştur. İlk periyot 8 elementi olan ununenniumu sentezleme girişimleri 2021 yılı itibariyle devam etmektedir.
Ununenyum
Ununenyum sentezi ilk olarak 1985 yılında Berkeley, California'daki superHILAC hızlandırıcısında einsteinium-254 hedefini kalsiyum -48 iyonlarıyla bombalayarak denendi:
-
254
99Es
+ 48
20CA
→ 302
119Uue
* → atom yok
300 nb'lik bir sınırlayıcı kesite yol açan hiçbir atom tanımlanmadı . Daha sonraki hesaplamalar, 3n reaksiyonunun ( 299 Uue ve ürün olarak üç nötron ile sonuçlanacak olan) enine kesitinin, 0,5 pb'de bu üst sınırdan altı yüz bin kat daha düşük olacağını göstermektedir.
Ununenyum keşfedilmemiş en hafif element olduğu için son yıllarda hem Alman hem de Rus ekiplerinin sentez deneylerinin hedefi olmuştur. Rus deneyleri 2011'de yapıldı ve hiçbir sonuç açıklanmadı, bu da güçlü bir şekilde hiçbir ununenyum atomunun tanımlanmadığını ima etti. Nisan-Eylül 2012 arasında, Darmstadt , Almanya'daki GSI Helmholtz Ağır İyon Araştırma Merkezi'nde berkelyum -249 hedefini titanyum -50 ile bombalayarak 295 Uue ve 296 Uue izotoplarını sentezleme girişimi yapıldı . Teorik olarak öngörülen enine kesite dayanarak, deneyin başlamasından sonraki beş ay içinde bir ununenyum atomunun sentezlenmesi bekleniyordu.
-
249
97bk
+ 50
22Ti
→ 299
119Uue
* → 296
119Uue
+ 3 1
0
n
-
249
97bk
+ 50
22Ti
→ 299
119Uue
* → 295
119Uue
+ 4 1
0
n
Deneyin başlangıçta Kasım 2012'ye kadar devam etmesi planlandı, ancak tennessin sentezini doğrulamak için 249 Bk hedefini kullanmak için erken durduruldu (böylece mermiler 48 Ca'ya değiştirildi ). 249 Bk ve 50 Ti arasındaki bu reaksiyonun ununenyum oluşumu için en uygun pratik reaksiyon olduğu tahmin edilmiştir, çünkü oldukça asimetriktir, ancak aynı zamanda biraz soğuktur. (Arasındaki reaksiyon 254 Es ve 48 Ca üstün olduğu, ancak miligram miktarları hazırlanması olur 254 bir hedef Es zordur.) Bununla birlikte, "gümüş mermi" gerekli değişim 48 Ca için 50 Ti ununennium beklenen verim böler yaklaşık yirmi, çünkü verim, füzyon reaksiyonunun asimetrisine güçlü bir şekilde bağlıdır.
Öngörülen kısa yarı ömürler nedeniyle, GSI ekibi, bozunma olaylarını mikrosaniyeler içinde kaydedebilen yeni "hızlı" elektronikler kullandı. 70 fb'lik bir sınırlayıcı kesit anlamına gelen hiçbir ununenyum atomu tanımlanmadı. Öngörülen gerçek kesit, mevcut teknolojinin sınırlarında olan 40 fb civarındadır.
Ekibi Nükleer Araştırma Ortak Enstitüsü içinde Dubna'da planlı, Rusya, kullanarak ununennium ve unbinilium sentezi üzerinde deneyler başlayacak 249 Bk + 50 Ti ve 249 Cf + 50 yeni bir deneysel kompleks kullanılarak 2019 yılında Ti reaksiyonları. Japonya'daki RIKEN ekibi de 2018'den başlayarak 248 Cm+ 51 V ve 248 Cm+ 54 Cr reaksiyonlarını kullanarak 248 Cm hedeflerle bu elementler üzerinde denemeler yapmayı planladı . İlki Haziran 2018'den beri devam ediyor.
unbinilyum
Elde onların başarısının ardından oganesson arasındaki reaksiyonla 249 Cf ve 48 Ca 2006 yılında ekibi Nükleer Araştırma Ortak Enstitüsü içinde (JINR) Dubna'da yaratma umuduyla, Mart-Nisan 2007'de benzer deneyler başladı unbinilium (eleman 120) 58 Fe ve 244 Pu çekirdeklerinden . Unbinilium izotopları sırasına alfa bozunma yarılanma ömrüne sahip olduğu tahmin edilir mikrosaniye . Başlangıç analizi unbinilium herhangi bir atomuna 400 bir sınır temin üretildi ortaya fb için enine kesiti incelenmiştir enerjisinde gerçekleşmiştir.
-
244
94Pu
+ 58
26Fe
→ 302
120übn
* → atom yok
Rus ekibi, reaksiyonu tekrar denemeden önce tesislerini yükseltmeyi planladı.
Nisan 2007'de, ekibi Ağır İyon Araştırma GSI Helmholtz Centre içinde Darmstadt , Almanya kullanarak unbinilium oluşturmaya teşebbüs uranyum -238 ve nikel -64:
-
238
92sen
+ 64
28Ni
→ 302
120übn
* → atom yok
Verilen enerjide kesit için 1,6 pb'lik bir sınır sağlayan hiçbir atom tespit edilmedi . GSI, deneyi daha yüksek hassasiyetle Nisan-Mayıs 2007, Ocak-Mart 2008 ve Eylül-Ekim 2008'de üç ayrı çalışmada tekrarladı, tümü olumsuz sonuçlarla 90 fb'lik bir kesit sınırına ulaştı.
Haziran-Temmuz 2010'da ve yine 2011'de, ekipmanlarını daha radyoaktif hedeflerin kullanımına izin verecek şekilde yükselttikten sonra, GSI'deki bilim adamları daha asimetrik füzyon reaksiyonunu denediler:
-
248
96Santimetre
+ 54
24cr
→ 302
120übn
* → atom yok
Reaksiyondaki değişikliğin, bu tür reaksiyonların verimi asimetrilerine büyük ölçüde bağlı olduğundan, unbinilium sentezleme olasılığını beş katına çıkarması bekleniyordu. 299 Ubn ve kızı 295 Og'nin tahmin edilen alfa bozunma enerjileriyle ve ayrıca torununun 291 Lv deneysel olarak bilinen bozunma enerjisiyle eşleşen üç bağlantılı sinyal gözlendi . Ancak bu olası bozulmaların ömürleri beklenenden çok daha uzundu ve sonuçlar doğrulanamadı.
Ağustos-Ekim 2011'de, GSI'de TASCA tesisini kullanan farklı bir ekip, yeni, daha da asimetrik bir reaksiyon denedi:
-
249
98bkz.
+ 50
22Ti
→ 299
120übn
* → atom yok
Asimetrisi nedeniyle, 249 Cf ve 50 Ti arasındaki reaksiyonun, aynı zamanda biraz soğuk olmasına rağmen, unbinilyumu sentezlemek için en uygun pratik reaksiyon olduğu tahmin edildi. 200 fb'lik bir sınırlayıcı kesit anlamına gelen hiçbir unbinilium atomu tanımlanmadı. Jens Volker Kratz, bu reaksiyonlardan herhangi biri ile unbinilium üretmek için gerçek maksimum kesitin 0.1 fb civarında olduğunu tahmin etti; buna karşılık, başarılı bir reaksiyonun en küçük kesiti için dünya rekoru, 209 Bi( 70 Zn,n) 278 Nh reaksiyonu için 30 fb idi ve Kratz, komşu ununenyumu üretmek için maksimum 20 fb'lik bir kesit öngördü. Bu tahminler doğruysa, o zaman ununenyum sentezlemek mevcut teknolojinin sınırlarında olacak ve unbinilyumu sentezlemek yeni yöntemler gerektirecektir.
unbiunyum
Sentezi unbiunium ilk hedef bombardıman tarafından 1977 yılında denendi uranyum-238 ile bakır -65 iyonları Schwerionenforschung für Gesellschaft içinde Darmstadt , Almanya:
-
238
92sen
+ 65
29Cu
→ 303
121Ubu
* → atom yok
Hiçbir atom tanımlanmadı.
unbibiyum
Unbibiumu sentezlemek için ilk denemeler 1972'de Flerov ve diğerleri tarafından yapıldı . en Nükleer Araştırma Ortak Enstitüsü (JINR), sıcak füzyon reaksiyonları neden olduğu ağır iyonu ile:
-
238
92sen
+ 66,68
30çinko
→ 304, 306
122ubb
* → atom yok
Bu deneyler , N = 184 ve Z > 120'de bir kararlılık adasının varlığına ilişkin erken tahminlerle motive edildi. Hiçbir atom saptanmadı ve 5 nb'lik (5.000 pb ) bir verim sınırı ölçüldü. Mevcut sonuçlar (bkz. flerovium ), bu deneylerin hassasiyetinin en az 3 büyüklük sırası ile çok düşük olduğunu göstermiştir.
2000 yılında, Gesellschaft für Schwerionenforschung (GSI) Helmholtz Ağır İyon Araştırma Merkezi, çok daha yüksek hassasiyetle çok benzer bir deney gerçekleştirdi:
-
238
92sen
+ 70
30çinko
→ 308
122ubb
* → atom yok
Bu sonuçlar, bu tür daha ağır elementlerin sentezinin önemli bir zorluk olmaya devam ettiğini ve ışın yoğunluğunun ve deneysel verimliliğin daha da geliştirilmesi gerektiğini göstermektedir. Daha kaliteli sonuçlar için gelecekte hassasiyet 1 fb'ye yükseltilmelidir .
Unbibiumu sentezlemek için başka bir başarısız girişim, 1978'de, doğal bir erbiyum hedefinin ksenon-136 iyonları ile bombalandığı GSI Helmholtz Merkezi'nde gerçekleştirildi :
-
nat
68Er
+ 136
54Xe
→ 298, 300, 302, 303, 304, 306
ubb
* → atom yok
Özellikle, 170 Er ve 136 Xe arasındaki reaksiyonun , yarı ömürleri mikrosaniye olan alfa-yayıcıları vermesi bekleniyordu; bu, flerovyumun izotoplarına bozunacak ve yarı ömürleri belki birkaç saate kadar uzayacak, çünkü flerovyumun yakınlarda olduğu tahmin edildiğinden, birkaç saate kadar uzayabilir. istikrar adasının merkezi . On iki saatlik ışınlamadan sonra bu reaksiyonda hiçbir şey bulunamadı. 238 U ve 65 Cu'dan unbiunyum sentezlemek için benzer bir başarısız girişimin ardından , süper ağır çekirdeklerin yarı ömürlerinin bir mikrosaniyeden az olması gerektiği veya kesitlerin çok küçük olduğu sonucuna varıldı. Süper ağır elementlerin sentezine ilişkin daha yeni araştırmalar, her iki sonucun da doğru olduğunu gösteriyor. 1970'lerde unbibiumu sentezlemeye yönelik iki girişimin her ikisi de, süper ağır elementlerin potansiyel olarak doğal olarak meydana gelip gelemeyeceğini araştıran araştırmalar tarafından desteklendi.
306 Ubb gibi çeşitli süper ağır bileşik çekirdeklerin fisyon özelliklerini inceleyen birkaç deney, 2000 ve 2004 yılları arasında Flerov Nükleer Reaksiyon Laboratuvarı'nda yapıldı . 248 Cm + 58 Fe ve 242 Pu + 64 Ni olmak üzere iki nükleer reaksiyon kullanıldı . Sonuçlar, süper ağır çekirdeklerin ağırlıklı olarak 132 Sn (Z=50, N=82) gibi kapalı kabuklu çekirdekleri dışarı atarak nasıl bölündüğünü ortaya koymaktadır . Ayrıca, füzyon-fisyon yolunun veriminin, 48 Ca ve 58 Fe mermileri arasında benzer olduğu ve süper ağır element oluşumunda gelecekte 58 Fe merminin olası bir kullanımını önerdiği bulundu .
unbiquadyum
GANIL'deki (Grand Accélérateur National d'Ions Lourds) bilim adamları, bu bölgedeki kabuk etkilerini araştırmak ve bir sonraki küresel protonu belirlemek için Z = 114, 120 ve 124 olan elementlerin bileşik çekirdeklerinin doğrudan ve gecikmeli fisyonunu ölçmeye çalıştılar. kabuk. Tamamen çekirdekte kovanlara sahip (ya da eşdeğer bir olan Bunun nedeni, büyülü numarayı bir proton ya nötron ) bu tür süper ağır elemanların çekirdekleri üzerinde daha fazla stabilite kazandırabilir olur, böylece daha yakın hareket stabilite ada . 2006'da, 2008'de yayınlanan tam sonuçlarla, ekip, doğal bir germanyum hedefinin uranyum iyonları ile bombardımanını içeren bir reaksiyondan elde edilen sonuçları sağladı :
-
238
92sen
+ doğal
32Ge
→ 308, 310, 311, 312, 314
Ubq
* → fisyon
Ekip, yarı ömürleri > 10 -18 s olan bileşik çekirdek fisyonlarını tanımlayabildiklerini bildirdi . Bu sonuç, güçlü bir stabilize edici etki göstermektedir Z sonraki proton kabuk = 124 noktaları Z değil,> 120 Z , daha önce düşünüldüğü gibi = 114. Bileşik çekirdek, henüz kendilerini nükleer kabuklara yerleştirmemiş olan nükleonların gevşek bir bileşimidir . İç yapısı yoktur ve yalnızca hedef ve mermi çekirdeği arasındaki çarpışma kuvvetleri tarafından bir arada tutulur. Nükleonların kendilerini nükleer kabuklar halinde düzenlemeleri için yaklaşık 10-14 s gerektiği tahmin edilmektedir, bu noktada bileşik çekirdek bir nüklide dönüşür ve bu sayı IUPAC tarafından iddia edilen bir izotopun sahip olması gereken minimum yarı ömür olarak kullanılır . potansiyel olarak keşfedilmiş olarak kabul edilebilir. Bu nedenle, GANIL deneyleri, 124 elementinin keşfi olarak sayılmaz .
Bileşik çekirdek 312 124'ün fisyonu da 2006'da İtalya'daki Laboratori Nazionali di Legnaro'daki (Legnaro Ulusal Laboratuvarları) tandem ALPI ağır iyon hızlandırıcısında incelenmiştir :
-
232
90NS
+ 80
34Gör
→ 312
Ubq
* → fisyon
JINR'de ( Joint Institute for Nuclear Research ) gerçekleştirilen önceki deneylere benzer şekilde , fisyon fragmanları 132 Sn ( Z = 50, N = 82) gibi çift sihirli çekirdekler etrafında kümelenmiş ve süper ağır çekirdeklerin bu tür çift sihirli çekirdekleri dışarı atma eğilimini ortaya çıkarmıştır. fisyon. 312 124 bileşik çekirdeğinden (daha hafif sistemlere göre) fisyon başına ortalama nötron sayısının da arttığı bulundu, bu da fisyon sırasında daha fazla nötron yayan daha ağır çekirdeklerin eğiliminin süper ağır kütle bölgesinde devam ettiğini doğruladı.
unbipentium
Unbipentium'u sentezlemek için ilk ve tek girişim 1970-1971'de Dubna'da çinko iyonları ve bir amerikyum - 243 hedefi kullanılarak gerçekleştirildi:
-
243
95NS
+ 66, 68
30çinko
→ 309, 311
UBP
* → atom yok
Hiçbir atom tespit edilmedi ve 5 nb'lik bir kesit sınırı belirlendi. Bu deney, Z ~ 126 ve N ~ 184 civarındaki çekirdekler için daha fazla kararlılık olasılığı tarafından motive edildi , ancak daha yeni araştırmalar, kararlılık adasının bunun yerine daha düşük bir atom numarasında (örneğin, kopernikyum , Z = 112) olabileceğini öne sürüyor . unbipentium gibi daha ağır elementlerin sentezi daha hassas deneyler gerektirecektir.
unbihexium
Başarısız olan ilk ve tek unbihexium sentezleme girişimi , 1971 yılında CERN'de (European Organisation for Nuclear Research) René Bimbot ve John M. Alexander tarafından sıcak füzyon reaksiyonu kullanılarak gerçekleştirildi:
-
232
90NS
+ 84
36Kr
→ 316
126uhh
* → atom yok
Yüksek enerjili (13-15 MeV ) alfa parçacıkları gözlemlendi ve unbihexium sentezi için olası kanıt olarak alındı. Daha yüksek duyarlılığa sahip sonraki başarısız deneyler , bu deneyin 10 mb duyarlılığının çok düşük olduğunu göstermektedir; bu nedenle, bu reaksiyonda unbihexium çekirdeklerin oluşumu pek olası değildir.
unbiseptium
Başarısız olan ilk ve tek unbiseptium sentezleme girişimi, 1978'de, doğal bir tantal hedefinin ksenon -136 iyonları ile bombalandığı GSI Helmholtz Center'daki UNILAC hızlandırıcısında gerçekleştirildi :
-
doğal
73Ta
+ 136
54Xe
→ 316, 317
Ub'ler
* → atom yok
Doğada aramalar
1976'da çeşitli üniversitelerden bir grup Amerikalı araştırmacı tarafından yapılan bir araştırma , esas olarak karaciğermoryum , unbiquadium, unbihexium ve unbiseptium gibi ilkel süper ağır elementlerin minerallerde açıklanamayan radyasyon hasarına (özellikle radyohalos ) neden olabileceğini öne sürdü . Bu, birçok araştırmacıyı 1976'dan 1983'e kadar doğada aramaya yöneltti . Davis'teki California Üniversitesi'nde profesör olan Tom Cahill liderliğindeki bir grup , 1976'da alfa parçacıklarını ve doğru enerjilere sahip X-ışınlarını tespit ettiklerini iddia etti. bu unsurların varlığını destekleyerek gözlenen hasara neden olur. Özellikle, (10 mertebesinde uzun ömürlü varlığı 9 10 bir bolluk kendi bozunma ürünleri ile birlikte yılda) unbiquadium ve unbihexium çekirdekler, -11 olası nisbetle aynı gen uranyum ve plütonyum , varsayılmı¸tır. Diğerleri hiçbirinin tespit edilmediğini iddia etti ve ilkel süper ağır çekirdeklerin önerilen özelliklerini sorguladı. Özellikle, bu tür herhangi bir süper ağır çekirdeğin N = 184 veya N = 228'de kapalı bir nötron kabuğuna sahip olması gerektiğini ve gelişmiş stabilite için bu gerekli koşulun yalnızca, karaciğer morumunun nötron eksikliği olan izotoplarında veya diğer elementlerin nötron bakımından zengin izotoplarında mevcut olduğunu belirttiler. doğal olarak oluşan izotopların çoğundan farklı olarak beta kararlı değildir . Bu aktivitenin aynı zamanda doğal seryumdaki nükleer dönüşümlerden kaynaklandığı ve süper ağır elementlerin bu iddia edilen gözlemi üzerine daha fazla belirsizliği artırdığı öne sürüldü.
24 Nisan 2008'de liderliğindeki grubun Amnon Marinov de Kudüs İbrani Üniversitesi'nde tek atomları bulduk iddia unbibium doğal olarak oluşan içinde -292 toryum 10 arasında bir zenginliği de mevduat -11 ve 10 -12 toryum için akrabası. Marinov ve ark. bilim camiasının bir bölümü tarafından eleştirildi. Marinov, makaleyi Nature ve Nature Physics dergilerine gönderdiğini iddia etti, ancak her ikisi de makaleyi hakem değerlendirmesine göndermeden reddetti. Unbibium-292 atomlarının , en az 100 milyon yıllık bir yarı ömre sahip, süper deforme veya aşırı deforme olmuş izomerler olduğu iddia edildi .
Daha önce ileri sürülen çakmak tanımlamada kullanılan teknikle, bir eleştiri toryum ile izotopları kütle spektrometresi , yayınlanan Physical Review C Marinov grup tarafından 2008'de bir çürütme içinde yayımlandı Physical Review C yayınlanan yorum sonra.
Hızlandırıcı Kütle Spektrometrisinin (AMS) üstün yöntemini kullanan toryum deneyinin tekrarı, 100 kat daha iyi duyarlılığa rağmen sonuçları doğrulamadı. Bu sonuç, toryum , roentgenium ve unbibium'un uzun ömürlü izotoplarına ilişkin iddialarıyla ilgili olarak Marinov'un işbirliğinin sonuçları hakkında büyük şüphe uyandırıyor . Bu pek olası olmasa da, unbibiyum izlerinin yalnızca bazı toryum örneklerinde mevcut olması hala mümkündür.
Bugün Dünya'daki ilkel süper ağır elementlerin olası kapsamı belirsizdir. Radyasyon hasarına uzun zaman önce neden oldukları doğrulansa bile, şimdi sadece izlere dönüşmüş, hatta tamamen gitmiş olabilirler. Bu tür süper ağır çekirdekleri tüm doğal olarak üretilebilir, sanki de kesin değildir kendiliğinden fisyon sonlandırmak için beklenen r işlemi daha ağır iyi elemanları önce, kütle numarası 270 ve 290 arasında ağır element oluşumundan sorumlu unbinilium oluşturulabilir.
Güncel bir hipotez spektrumunu açıklamaya çalışan Przybylski Yıldızı doğal olarak oluşan yoluyla flerovyum , unbinilium ve unbihexium .
Sekizinci periyot elementlerinin tahmin edilen özellikleri
Element 118, oganesson , sentezlenmiş en ağır elementtir. Sonraki iki element, elementler 119 ve 120 , bir 8s serisi oluşturmalı ve sırasıyla bir alkali ve alkalin toprak metali olmalıdır . 120 nolu elementin ötesinde , 8s elektronları ve 8p 1/2 , 7d 3/2 , 6f ve 5g alt kabuklarının doldurulması bu elementlerin kimyasını belirlediğinde süperaktinit serisinin başlaması bekleniyor . Durumun aşırı karmaşıklığı nedeniyle 122'nin ötesindeki elementler için tam ve doğru CCSD hesaplamaları mevcut değildir: 5g, 6f ve 7d orbitalleri yaklaşık olarak aynı enerji seviyesine sahip olmalıdır ve 160 element bölgesinde, 9s, 8p 3 /2 ve 9p 1/2 orbitalleri de enerji bakımından yaklaşık olarak eşit olmalıdır. Bu, elektron kabuklarının karışmasını ve böylece blok kavramının artık çok iyi uygulanmamasını sağlayacak ve ayrıca bu elementlerin bazılarının periyodik bir tabloda konumlandırılmasını çok zorlaştıracak yeni kimyasal özelliklerle sonuçlanacaktır.

Kimyasal ve fiziksel özellikler
Öğeler 119 ve 120
119 ve 120 numaralı elementlerin bazı tahmin edilen özellikleri Mülk 119 120 Standart atom ağırlığı [322] [325] Grup 1 2 Değerlik elektron konfigürasyonu 8s 1 8s 2 Kararlı oksidasyon durumları 1 , 3 2 , 4 İlk iyonlaşma enerjisi 463.1 kJ/mol 563.3 kJ/mol metalik yarıçap 260 öğleden sonra saat 200 Yoğunluk G / cm3 3. 7 g / cm 3 Erime noktası 0–30 °C (32–86 °F) 680 °C (1.300 °F) Kaynama noktası 630 °C (1.200 °F) 1.700 °C (3.100 °F)
8. periyodun ilk iki elementi ununenyum ve unbinilium, elementler 119 ve 120 olacaktır. Elektron konfigürasyonları 8s orbitalinin doldurulmasına sahip olmalıdır. Bu yörünge göreceli olarak stabilize ve büzülmüştür; Bu şekilde, elemanlar 119 ve 120 gibi daha fazla olmalıdır rubidyum ve stronsiyum , yukarıda yakın komşuları daha fransiyum ve radyum . 8s yörüngesinin göreli daralmasının bir başka etkisi, bu iki elementin atom yarıçaplarının , fransiyum ve radyumunkilerle yaklaşık olarak aynı olması gerektiğidir. Normal alkali ve toprak alkali metaller gibi davranmalıdırlar (en yakın dikey komşularından daha az reaktif olsalar da), normalde sırasıyla +1 ve +2 oksidasyon durumları oluştururlar , ancak 7p 3/2 alt kabuğunun göreli kararsızlaşması ve nispeten düşük iyonlaşma enerjileri . 7p 3/2 elektronları, +3 ve +4 (sırasıyla) gibi daha yüksek oksidasyon durumlarını da mümkün kılmalıdır.
süperaktinitler
Süperaktinidlerin, ilk 7d elementi ile birlikte sekizinci periyodun 5g ve 6f elementleri olarak sınıflandırılabilen 121 ila 157 elementleri arasında olduğu düşünülebilir. Superactinide serisinde, 7d 3/2 , 8p 1/2 , 6f 5/2 ve 5g 7/2 kabuklarının tümü aynı anda doldurulmalıdır. Bu, çok karmaşık durumlar yaratır, öyle ki, sadece 121 ve 122 elementleri için tam ve doğru CCSD hesaplamaları yapılmıştır. İlk süperaktinit, unbiunyum (element 121), lantan ve aktinyuma benzer olmalıdır : ana oksidasyon durumu + olmalıdır. 3, değerlik alt kabuklarının enerji seviyelerinin yakınlığı, element 119 ve 120'de olduğu gibi daha yüksek oksidasyon durumlarına izin verebilse de. 8p alt kabuğunun göreli stabilizasyonu, element 121 için temel durum 8s 2 8p 1 değerlik elektron konfigürasyonu ile sonuçlanmalıdır , lantan ve aktinyumun ds 2 konfigürasyonlarının aksine ; yine de, bu anormal konfigürasyon, aktinyumunkine benzer kalan hesaplanmış kimyasını etkilemiyor gibi görünüyor. İlk iyonlaşma enerjisinin 429.4 kJ/mol olduğu tahmin edilmektedir, bu da alkali metaller potasyum , rubidyum , sezyum ve fransiyum hariç tüm bilinen elementlerinkinden daha düşük olacaktır : bu değer 8 alkali metal periyodundan bile daha düşüktür. ununenyum (463.1 kJ/mol). Benzer şekilde, bir sonraki süperaktinid, unbibium (element 122), +4 ana oksidasyon durumu ile seryum ve toryuma benzer olabilir , ancak temel durum 7d 1 8s 2 8p 1 veya 8s 2 8p 2 değerlik elektron konfigürasyonuna sahip olacaktır. , toryumun 6d 2 7s 2 konfigürasyonunun aksine . Bu nedenle, unbibiyumun 8p 1/2 elektronunu toryumun 6d elektronundan daha kolay iyonize etme kolaylığı nedeniyle , ilk iyonlaşma enerjisi toryumunkinden (Th: 6,3 eV ; Ubb: 5,6 eV) daha küçük olacaktır. 5g yörüngesinin kendisinin çökmesi, 125 numaralı elementin çevresine kadar ertelenir; 119 elektronlu izoelektronik serinin elektron konfigürasyonlarının, 119'dan 122'ye kadar olan elementler için [Og]8s 1 , 123 ve 124 elementler için [Og]6f 1 ve 125'ten sonraki elementler için [Og]5g 1 olması beklenir .
İlk birkaç süperaktinidde, eklenen elektronların bağlanma enerjilerinin, tüm değerlik elektronlarını kaybedebilecekleri kadar küçük olduğu tahmin edilmektedir; örneğin, unbihexium (element 126) kolayca +8 oksidasyon durumu oluşturabilir ve sonraki birkaç element için daha da yüksek oksidasyon durumları mümkün olabilir. Unbihexium diğer çeşitli görüntülemek için tahmin edilen oksidasyon durumları : Son hesaplamalar stabil sürmüşlerdir monoflorür 5 g arasında bir bağlama etkileşiminden kaynaklanan UbhF mümkün olabilir yörünge unbihexium ve 2 , p orbital flor . Diğer tahmin edilen oksidasyon durumları arasında +2, +4 ve +6; +4 unbihexium'un en olağan oksidasyon durumu olması beklenir. Unbiennium (element 129) için unbipentium (element 125) gelen superactinides bir +6 oksidasyon durumu ve form için öngörülen edilir heksaflorürler UbpF da, 6 ve UbhF 6 nispeten zayıf bir şekilde bağlanmış olduğu tahmin edilmektedir. Bağ ayrışma enerjileri büyük ölçüde element 127 artması ve daha çok elemanı 129 de bu elemanın 129. florür olarak, 8p yörünge içeren eleman 125 daha kovalent karakteri florürler güçlü iyonik karakter bir kayma göstermektedir beklenmektedir Uranyumun uranyum heksaflorürde bağlanma için 5f ve 6d orbitallerini nasıl kullandığından farklı olarak, bu süperaktinit heksaflorürlerde bağlanma, çoğunlukla süperaktinidin en yüksek 8p alt kabuğu ile florin 2p alt kabuğu arasındadır .
Erken süperaktinitlerin yüksek oksidasyon durumlarına ulaşma yeteneklerine rağmen, 5g elektronlarının iyonize edilmesinin en zor olacağı hesaplanmıştır; Ubp 6+ ve Ubh 7+ iyonlarının , Np 6+ iyonunun 5f 1 konfigürasyonuna benzer bir 5g 1 konfigürasyonu taşıması beklenir . Lantanidlerdeki 4f elektronlarının düşük kimyasal aktivitesinde de benzer davranış gözlenir ; bu, 5g orbitallerinin küçük ve elektron bulutunda derinlere gömülü olmasının bir sonucudur. Halihazırda bilinen herhangi bir elementin temel durum elektron konfigürasyonunda mevcut olmayan g-orbitallerindeki elektronların varlığı , g elektronlarının olmamasına rağmen, halihazırda bilinmeyen hibrit orbitallerin süperaktinitlerin kimyasını yeni yollarla oluşturmasına ve etkilemesine izin vermelidir. bilinen elementlerde süperaktinid kimyasını tahmin etmeyi zorlaştırır.
Süperaktinidlerin tahmin edilen bazı bileşikleri (X = bir halojen ) 121 122 123 124 125 126 127 128 129 132 142 143 144 145 146 148 153 154 155 156 157 Birleştirmek UbuX 3 UbbX 4 UbtX 5 UbqX 6 UbpF
UbpF 6
UbpO2+
2UbhF
UbhF 6
UbhO 4UbsF 6 UboF 6 UbeF
UbeF 6UqbX 4
UqbX 6UqtF 6 UqqX 6
UqqO2+
2
UqqF 8
UqqO 4UqpF 6 UqoO 6 analoglar La X 3
Ac X 3Ce X 4
Bin X 4Np O2+
2THF 4 UF 6
UO2+
2
Pu F 8
PuO 4UO 6 oksidasyon durumları 3 4 5 6 1, 6, 7 1, 2, 4, 6, 8 6 6 1, 6 6 4, 6 6, 8 3, 4, 5, 6, 8 6 8 12 3 0, 2 3, 5 2 3
Daha sonraki süperaktinidlerde oksidasyon durumları daha düşük olmalıdır. 132 elementi ile baskın en kararlı oksidasyon durumu sadece +6 olacaktır; bu, eleman 144 tarafından daha da +3 ve +4'e düşürülür ve süperaktinid serisinin sonunda sadece +2 (ve muhtemelen 0) olacaktır, çünkü o noktada doldurulmakta olan 6f kabuğu derinlerdedir. elektron bulutu ve 8s ve 8p 1/2 elektronları kimyasal olarak aktif olamayacak kadar güçlü bir şekilde bağlıdır. 5g kabuğu element 144'te ve 6f kabuğu element 154 civarında doldurulmalıdır ve süperaktinitlerin bu bölgesinde 8p 1/2 elektronları o kadar güçlü bir şekilde bağlanırlar ki artık kimyasal olarak aktif olmazlar, böylece sadece birkaç elektron olabilir. kimyasal reaksiyonlara katılır. Fricke ve diğerleri tarafından yapılan hesaplamalar. 154 elementinde 6f kabuğunun dolu olduğunu ve kimyasal olarak aktif olmayan 8s ve 8p 1/2 kabuklarının dışında d- veya başka elektron dalgası fonksiyonlarının olmadığını tahmin edin . Bu oldukça olmak elemanı 154 neden olabilir reaktif ile soygaz benzeri özellikler. Upp: Pyykkö göre Hesaplamalar yine elemanı 155, 6R kabuk halen kimyasal olarak iyonize olduğu beklemek 3+ tam 6f kabuk sahip olmalıdır, ve dördüncü iyonizasyon potansiyel kişilerce arasında olmalıdır terbiyum ve disprosyum + bilinmektedir, her ikisi de, 4 durum.
Lantanid ve aktinit kasılmalarına benzer şekilde , süperaktinidlerin iyonik yarıçaplarının beklenenden daha küçük olduğu süperaktinid serilerinde bir süperaktinid daralması olmalıdır . Gelen lantanitler , daralma elemanı başına 4.4 pm ile ilgilidir; içinde Aktinitler , bu elemanın başına 3 pm hakkındadır. 4f dalga fonksiyonunun 5f dalga fonksiyonuna kıyasla daha büyük lokalizasyonundan dolayı lantanitlerde kasılma aktinitlerden daha büyüktür. Lantanitlerin, aktinitlerin ve süperaktinitlerin dış elektronlarının dalga fonksiyonlarıyla yapılan karşılaştırmalar, süperaktinitlerde element başına yaklaşık 2 pm'lik bir daralmanın öngörülmesine yol açar; Bu, lantanitler ve aktinitlerdeki kasılmalardan daha küçük olmasına rağmen, 4f ve 5f kabuklarına sadece 14 elektronun doldurulması yerine, derin gömülü 5g ve 6f kabuklarına 32 elektronun doldurulması gerçeğinden dolayı toplam etkisi daha büyüktür. sırasıyla lantanitler ve aktinitler.
Pekka Pyykkö bu süperaktinitleri üç seriye ayırır: 5g serisi (121 ila 138 elementler), 8p 1/2 serisi (139 ila 140 elementler) ve 6f serisi (141 ila 155 elementler), ayrıca bir enerji seviyeleri arasında büyük bir örtüşme ve 6f, 7d veya 8p 1/2 orbitallerinin de erken süperaktinid atomları veya iyonlarında iyi bir şekilde işgal edilebileceği. Ayrıca , her bir lantanitte sadece bir veya iki 4f elektronun kimyasal bileşiklerde nasıl iyonize edildiğine benzer şekilde, 5g elektronlarının çoğunlukla kimyasal olarak aktif olmaması anlamında, bunların daha çok "süper lantanitler " gibi davranmasını bekliyor . Ayrıca süperaktinitlerin olası oksidasyon durumlarının 6f serisinde çok yüksek, element 148'de +12 gibi değerlere yükselebileceğini tahmin etti.
Andrey Kulsha, 121'den 156'ya kadar olan otuz altı elementi "geçiş" elementi olarak adlandırdı ve onları, biri 121'den 138'e ve diğeri 139'dan 156'ya kadar olan elementler olmak üzere, her biri on sekizlik iki diziye ayırmayı önerdi. 5g kabuğunun dolgusu baskın olduğundan ve komşu elementler birbirine çok benzer olduğundan, oksidasyon durumları esas olarak +4 ila +6 arasında değişen lantanitler, uranyum , neptunyum ve plütonyum ile bir benzerlik oluşturur . İkincisi, aktinitlere benzer olacaktır: başlangıçta (140'lardaki elementlerin çevresinde), 6f kabuğu 7d'nin üzerine çıktığında çok yüksek oksidasyon durumları beklenir, ancak bundan sonra tipik oksidasyon durumları düşer ve elementlerdeki elementlerde azalır. 150'li yıllardan itibaren 8p 1/2 elektronlar kimyasal olarak aktif olmayı bırakacaktır. İki sıra, tam bir 5g 18 alt kabuğun eklenmesiyle ayrıldığından , birbirlerinin analogları olarak da kabul edilebilirler.
Geç süperaktinidlerden bir örnek olarak, element 156'nın, kararlı bir [Og]5g 18 6f 14 8s 2 8p üzerinde kolayca çıkarılabilen 7d 2 elektronlu elektron konfigürasyonu nedeniyle, esas olarak +2 oksidasyon durumunu sergilemesi beklenir.2
1/2çekirdek. Bu nedenle , aynı şekilde kararlı bir [Rn]5f 14 çekirdek üzerinde bir çift kolayca çıkarılabilen 7s 2 elektrona sahip olan ve genellikle +2 durumunda olan nobeliumun daha ağır bir türdeşi olarak kabul edilebilir ( nobelium elde etmek için güçlü oksitleyiciler gereklidir). +3 durumu). İlk iyonlaşma enerjisi yaklaşık 400 kJ/mol ve metalik yarıçapı yaklaşık 170 pikometre olmalıdır. Yaklaşık 445 u bir nispi atom kütlesi ile, g / cm 26 civarında bir yoğunluğa sahip çok ağır metal olmalıdır 3 .
157'den 166'ya kadar olan elementler
8. periyotta 7d geçiş metallerinin 157 ila 166 arası elementler olması beklenir. 8s ve 8p 1/2 elektronları bu elementlerde o kadar güçlü bir şekilde bağlı olsalar da herhangi bir kimyasal reaksiyonda yer alamamaları gerekir, 9s ve 9p 1/2 seviyelerin hibridizasyon için hazır olması bekleniyor. Bu 7d elementler, itriyum ile kadmiyum arasındaki 4d elementlere benzer olmalıdır . Özellikle, 7d 10 9s 0 elektron konfigürasyonuna sahip element 164 , 4d 10 5s 0 elektron konfigürasyonu ile paladyum ile açık benzerlikler gösterir .
Geçiş metallerinin bu serinin soy metaller nedeniyle bir dış bulunmadığı için, bunların hafif homologları gibi soylu olması beklenmemektedir s koruma için ve aynı zamanda 7d kabuk güçlü iki altkabuklarda bölüme bölündüğü için nedeniyle göreli etkilere kabuk. Bu, 7d geçiş metallerinin ilk iyonlaşma enerjilerinin, daha hafif türdeşlerinden daha küçük olmasına neden olur.
Unhexquadium kimyasında teorik ilgi büyük ölçüde teorik tahminler motive olması olan, özellikle izotopları 472 UHQ ve 482 UHQ (164 proton ve 308 ya da 318 nötron , varsayımsal bir ikinci merkezinde olacaktır) stabilite ada (ilk copernicium , özellikle de yarı ömürleri yüzyıllar veya binyıllar olması beklenen 291 Cn, 293 Cn ve 296 Cn izotopları üzerinde odaklanmıştır ).
Hesaplamalar, element 164'ün (hexquadium olmayan) 7d elektronlarının kimyasal reaksiyonlara çok kolay bir şekilde katılması gerektiğini tahmin eder, böylece unhexquadium , güçlü ligandlara sahip sulu çözeltilerde normal +2 durumuna ek olarak stabil +6 ve +4 oksidasyon durumları gösterebilmelidir. . Unhexquadium bu nedenle Uhq( CO ) 4 , Uhq( PF 3 ) 4 (her ikisi de karşılık gelen paladyum bileşikleri gibi dört yüzlü ) ve Uhq( CN ) gibi bileşikler oluşturabilmelidir.2−
2( lineer ) kurşundan çok farklı bir davranıştır, ki bu unhexquadium göreli etkiler için olmasa bile daha ağır bir homologu olacaktır . Bununla birlikte, iki değerlikli durum sulu çözeltideki ana durum olacaktır (her ne kadar +4 ve +6 durumları daha güçlü ligandlarla mümkün olsa da) ve unhexquadium(II) kurşuna unhexquadium(IV) ve unhexquadium(VI)'dan daha benzer davranmalıdır. ).
Unhexquadium yumuşak olması beklenmektedir Lewis asidi ve 4 Ahrlands yumuşaklık parametresi yakın olması eV . Unhexquadium en fazla orta derecede reaktif olmalı ve molibdeninkiyle karşılaştırılabilir yaklaşık 685 kJ/mol olması gereken bir ilk iyonizasyon enerjisine sahip olmalıdır . Nedeniyle lantanit, aktinit ve superactinide kasılmaları , unhexquadium sadece 158 bir metalik yarıçapı olmalıdır pm çok yakın daha hafif o kadar magnezyum 474 civarında getirirken beklenen atom ağırlığına rağmen, u 19.5 kat atom ağırlığı yaklaşık olan magnezyum. Bu küçük yarıçap ve yüksek ağırlık , 22.61 g·cm- 3 ile şu anda bilinen en yoğun element olan osmiyumun iki katından fazla , yaklaşık 46 g·cm -3 gibi son derece yüksek bir yoğunluğa sahip olmasının beklenmesine neden olur ; unhexquadium sadece komşu unhextrium (öğe 163) olmak üzere, periyodik tablodaki ilk 172 elemanlarında daha yoğun ikinci en yoğun bir unsuru olmalıdır (47 g-cm -3 ). Metalik unhexquadium , kovalent bağları nedeniyle çok büyük bir kohezyon enerjisine ( kristalizasyon entalpisi ) sahip olmalıdır , bu da büyük olasılıkla yüksek bir erime noktasına neden olur. Metalik durumda, unhexquadium oldukça asil ve paladyum ve platine benzer olmalıdır . Frick ve ark. Her iki elementin de kapalı kabuk konfigürasyonları ve benzer iyonlaşma enerjileri olduğundan, oganesson ile bazı biçimsel benzerlikler önerdiler , ancak oganesson çok kötü bir soy gaz olsa da, hexquadium'un iyi bir soy metal olacağını belirtiyorlar.
Son iki 7d metali olan 165 (unhexpentium) ve 166 (unhexhexium) elementleri, sırasıyla +1 ve +2 oksidasyon durumlarındayken alkali ve toprak alkali metallere benzer şekilde davranmalıdır . 9s elektronlarının , göreli olmayan hesaplamaların öngördüğünden çok daha güçlü bir şekilde bağlanmasına neden olan göreli etkilerden dolayı, 9s elektronları, sodyum ve magnezyumun 3s elektronlarınınkiyle karşılaştırılabilir iyonizasyon enerjilerine sahip olmalıdır . 7d elektronlarının iyonizasyon enerjileri, element 165 için +3 gibi daha yüksek oksidasyon durumlarına izin verecek kadar düşük olmasına rağmen, element 165 ve 166 normalde sırasıyla +1 ve +2 oksidasyon durumlarını sergilemelidir. Element 166 için oksidasyon durumu +4 daha azdır. muhtemelen, 11. ve 12. gruplardaki (özellikle altın ve cıva ) daha hafif elementlere benzer bir durum yaratıyor . Copernicium cıva ile değil, olduğu gibi, Ahh elemanın 166 iyonizasyon 2+ bir 7d ile sonuçlanması beklenmektedir 10 daha benzer hafif "daha az göreli hale s-elektron kaybı, ancak D-elektron tekabül eden konfigürasyon 12. grup elementler çinko, kadmiyum ve esasen geçiş metali karakterine sahip olmayan cıvadır.
Elementlerin tahmin edilen bazı özellikleri 156-166
Metalik yarıçaplar ve yoğunluklar ilk yaklaşımlardır.
Çoğu benzer grup önce verilir, ardından diğer benzer gruplar gelir.Mülk 156 157 158 159 160 161 162 163 164 165 166 Standart atom ağırlığı [445] [448] [452] [456] [459] [463] [466] [470] [474] [477] [481] Grup Yb grubu
(4)3
(5)4
(6)5
(7)6
(8)7
(9)8
(10)9
(11)10
(12, 14, 18)11
(1, 13)12
(2, 14)Değerlik elektron konfigürasyonu 7d 2 7d 3 7d 4 7d 5 7d 6 7 gün 7 7 gün 8 7 gün 9 7 gün 10 7d 10 9s 1 7d 10 9s 2 Kararlı oksidasyon durumları 2 3 4 1 , 5 2 , 6 3 , 7 4 , 8 5 0 , 2 , 4 , 6 1 , 3 2 İlk iyonlaşma enerjisi 400 kJ/mol 450 kJ/mol 520 kJ/mol 340 kJ/mol 420 kJ/mol 470 kJ/mol 560 kJ/mol 620 kJ/mol 690 kJ/mol 520 kJ/mol 630 kJ/mol metalik yarıçap 170 pm 163 pm 157 öğleden sonra 152 öğleden sonra 148 öğleden sonra 148 öğleden sonra 149 öğleden sonra 152 öğleden sonra 158 öğleden sonra 250 öğleden sonra saat 200 Yoğunluk 26 g / cm 3 28 g / cm 3 30 g / cm 3 33 g / cm 3 36 g / cm 3 40 g / cm 3 45 g / cm 3 47 g / cm 3 46 g / cm 3 7 g / cm 3 11 g / cm 3
167 ila 172 arasındaki elementler
Periyodik tabloda önümüzdeki altı elemanları kendi döneminde geçen ana grup elemanları olması bekleniyor, ve büyük olasılıkla 5p elemanları benzer olması olan olan indiyum yoluyla xenon . 167 ila 172 numaralı elemanlarda 9p 1/2 ve 8p 3/2 mermiler doldurulacaktır. Enerji öz değerleri birbirine o kadar yakındır ki, göreceli olmayan 2p ve 3p alt kabuklarına benzer şekilde birleşik bir p-alt kabuk gibi davranırlar. Böylece, eylemsiz çift etkisi oluşmaz ve 167 ila 170 arasındaki elementlerin en yaygın oksidasyon durumlarının sırasıyla +3, +4, +5 ve +6 olması beklenir. Element 171'in (unseptunium) halojenlerle bazı benzerlikler göstermesi , -1 ile +7 arasında değişen çeşitli oksidasyon durumları göstermesi beklenir, ancak fiziksel özelliklerinin bir metalinkine daha yakın olması beklenir. Elektron afinitesinin 3.0 eV olması beklenir , bu da bir hidrojen halojenür benzeri HUsu oluşturmasına izin verir . Usu - iyonunun iyodür (I - ) ile karşılaştırılabilir yumuşak bir baz olması beklenir . Element 172'nin (unseptbium), iyonizasyon enerjilerinin çok benzer olması gerektiğinden (Xe, 1170.4 kJ/mol; Usb, 1090 kJ/mol) ksenonunkine benzer kimyasal davranışa sahip bir soy gaz olması beklenir . Aralarında sadece temel fark xenon farklı olarak, bir olması beklenmektedir, bu elemanın 172 olan sıvı ya da katı olarak , standart sıcaklık ve basınç nedeniyle çok daha yüksek bir atom ağırlığına. Unseptbiyumun, daha hafif türdeş ksenonuna benzer şekilde florürler ve oksitler oluşturan güçlü bir Lewis asidi olması beklenir . 165-172 numaralı elementlerin 2. ve 3. periyotlarla benzerliğinden dolayı, Fricke ve ark. onları periyodik tablonun dokuzuncu periyodunu oluştururken, sekizinci periyodu asil metal elementinde sona erdirmek için aldılar 164. Bu dokuzuncu periyot, hiçbir geçiş olmaması beklendiği için ikinci ve üçüncü periyotla benzer olacaktır. metaller.
Elementlerin tahmin edilen bazı özellikleri 167-172
Metalik veya kovalent yarıçaplar ve yoğunluklar ilk yaklaşımlardır.Mülk 167 168 169 170 171 172 Standart atom ağırlığı [485] [489] [493] [496] [500] [504] Grup 13 14 15 16 17 18 Değerlik elektron konfigürasyonu 9s 2 9p 1 9s 2 9p 2 9s 2 9p 2 8p 1 9s 2 9p 2 8p 2 9s 2 9p 2 8p 3 9s 2 9p 2 8p 4 Kararlı oksidasyon durumları 3 4 5 6 -1 , 3 , 7 0 , 4 , 6 , 8 İlk iyonlaşma enerjisi 620 kJ/mol 720 kJ/mol 800 kJ/mol 890 kJ/mol 984 kJ/mol 1090 kJ/mol Metalik veya kovalent yarıçap akşam 190 180 öğleden sonra 175 öğleden sonra 170 pm 165 öğleden sonra 220 öğleden sonra Yoğunluk 17 g / cm 3 19 g / cm 3 18 g / cm 3 17 g / cm 3 16 g / cm 3 9 g / cm 3
172 öğesinin ötesinde
Son periyot 8 element olan 172 elementinin, oganesson'dan (son periyot 7 element) sonraki ilk soy gaz olması beklenmektedir . Bunun ötesinde, süperaktinitler gibi başka bir uzun geçiş serisi başlamalı, en azından 6g, 7f ve 8d kabuklarını doldurmalıdır (10s, 10p 1/2 ve 6h 11/2 , serinin başlarında katkıda bulunmak için çok yüksek enerjiyle). Bu elektronlar çok gevşek bir şekilde bağlanacak ve potansiyel olarak son derece yüksek oksidasyon durumlarını ulaşılabilir kılacak, ancak iyonik yük arttıkça elektronlar daha sıkı bağlanacaktır.
173 numaralı elementte (unsepttrium), en dıştaki elektron 6g 7/2 alt kabuğuna girer . Spin-yörünge etkileşimleri, 8p 3/2 ve 6g 7/2 alt kabukları arasında çok büyük bir enerji boşluğu yaratacağından , bu en dıştaki elektronun çok gevşek bir şekilde bağlanması ve bir Ust + katyonu oluşturmak için çok kolay bir şekilde kaybolması beklenir . Bunun bir sonucu olarak, eleman 173, bir alkali metal gibi kimyasal olarak davranması beklenir, ve hatta çok daha fazla reaktif ile bir sezyum (fransiyum ve eleman 119 sezyum daha az reaktif olması nedeniyle göreli etkilerine bağlı olarak).
Element 184 (unoctquadium) erken tahminlerde önemli ölçüde hedeflendi, çünkü başlangıçta 184'ün sihirli bir proton sayısı olacağı tahmin edildi: en az 7f ile [Usb] 6g 5 7f 4 8d 3 elektron konfigürasyonuna sahip olduğu tahmin ediliyor. ve 8d elektronları kimyasal olarak aktiftir. Kimyasal davranışının uranyum ve neptünyuma benzer olması beklenir , çünkü +6 durumunu geçen iyonlaşma (6g elektronların çıkarılmasına karşılık gelir) muhtemelen kârsız olacaktır; +4 durumu, katı bileşiklerde +5 ve +6 erişilebilirliği ile sulu çözeltide en yaygın olmalıdır.
Periyodik tablonun sonu
Fiziksel olarak mümkün olan elementlerin sayısı bilinmemektedir. Düşük bir tahmin, periyodik ve nüklid tablolarının uzantısı proton ve nötron damlama hatları ve alfaya karşı kararlılık ile sınırlandırıldığından , Z = 126 üzerinde merkezlenmesi beklenen kararlılık adasından hemen sonra periyodik tablonun sona erebileceğidir. çürüme ve kendiliğinden fisyon. Y. Gambhir ve diğerleri tarafından yapılan bir hesaplama . , nükleer bağlanma enerjisini ve çeşitli bozunma kanallarındaki kararlılığı analiz ederek , Z = 146'da bağlı çekirdeklerin mevcudiyeti için bir sınır önerir . Walter Greiner gibi bazıları, periyodik tablonun bir sonu olmayabileceğini öngördü. Periyodik tablonun sonunun diğer tahminleri arasında Z = 128 ( John Emsley ) ve Z = 155 (Albert Khazan) bulunur.
Atom numarası 137'nin üzerindeki elementler
Richard Feynman'ın , göreli Dirac denkleminin böyle bir durumda en içteki elektronun temel-durum enerjisinin öngördüğü gerekçesiyle, Z = 137'den büyük atom numaraları için nötr atomların var olamayacağını öne sürmesi fizikçiler arasında bir "halk efsanesidir". atom hayali bir sayı olurdu . Burada 137 sayısı, ince yapı sabitinin tersi olarak ortaya çıkar . Bu argümanla, nötr atomlar untriseptium'un ötesinde var olamaz ve bu nedenle elektron orbitallerine dayalı periyodik bir element tablosu bu noktada bozulur. Ancak bu argüman, atom çekirdeğinin noktasal olduğunu varsayar. Daha doğru bir hesaplama, sınırı Z ≈ 173'e daha da iteceği tahmin edilen çekirdeğin küçük ama sıfır olmayan boyutunu hesaba katmalıdır .
Bohr modeli
Bohr modeli bir bir elektronun hızı için 137 den atom numarası daha sonra ile atomlar için sergiler zorluk, yörünge elektron 1s , v , ile verilmektedir
burada Z, bir atom numarası ve α olan ince yapı sabiti , elektromanyetik etkileşim kuvvetinin bir ölçüsüdür. Bu yaklaşımda altında, daha büyük 137 bir atom ağırlığına sahip olan herhangi bir eleman 1s elektronların daha hızlı seyahat için gerektirecek c , ışığın hızı . Bu nedenle, göreli olmayan Bohr modeli, böyle bir öğeye uygulandığında hatalıdır.
Göreli Dirac denklemi

Relativistik Dirac denklemi temel hal enerji olarak verir
burada m elektronun kalan kütlesidir. İçin Z > 137 Dirac temel durum dalga fonksiyonu bağlı yerine, titreşimli ve pozitif ve negatif enerji spektrumları arasındaki bir aralık olarak, orada Klein paradoksu . Çekirdeğin sonlu boyutunun etkilerini hesaba katan daha doğru hesaplamalar , Z > Z cr ≈ 173 için bağlanma enerjisinin önce 2 mc 2'yi aştığını gösterir. Z > Z cr için , en içteki yörünge (1s) dolu değilse, çekirdeğin elektrik alanı bir elektronu vakumdan çekerek bir pozitronun kendiliğinden emisyonuna neden olur . 1s alt kabuğunun negatif sürekliliğe bu dalışı, daha ayrıntılı tedaviler daha az kasvetli bir sonuç önerse de, genellikle periyodik tablonun bir "sonunu" teşkil ettiği düşünülmüştür.
Atom numaraları Z cr ≈ 173'ün üzerinde olan atomlara süper kritik atomlar denir . Süperkritik atomlar tamamen iyonize edilemezler çünkü 1s alt kabukları, elektronun bağlı olduğu ve pozitronun kaçtığı negatif süreklilikten bir elektron-pozitron çiftinin yaratıldığı kendiliğinden çift oluşumu ile doldurulacaktır. Bununla birlikte, atom çekirdeğinin etrafındaki güçlü alan, uzayın çok küçük bir bölgesiyle sınırlıdır, bu nedenle Pauli dışlama ilkesi , negatif sürekliliğe dalmış olan alt kabuklar bir kez doldurulduktan sonra kendiliğinden çift oluşumunu yasaklar. Elementler 173-184, onlar için sadece 1s kabuğu negatif sürekliliğe daldığı için zayıf süper kritik atomlar olarak adlandırılmıştır ; 2p 1/2 kabuğunun, element 185'in etrafında ve 2s kabuğunun element 245'in etrafında birleşmesi bekleniyor. Deneyler, şimdiye kadar, ağır çekirdeklerin çarpışması yoluyla süper kritik yüklerin bir araya getirilmesinden kendiliğinden çift oluşumunu tespit etmeyi başaramadı (örn. 174'lük bir etkin Z'yi verir; uranyumlu uranyum, etkin Z = 184'ü verir ve kaliforniyumlu uranyum, etkin Z = 190'ı verir ). Süper kritik atomların elektronik yapılarında herhangi bir zorluk oluşturmaması beklendiğinden, periyodik tablonun sonu elektron kabuğu kararsızlıklarından ziyade nükleer kararsızlık tarafından belirlenebilir.
kuark maddesi
Ayrıca ötesinde bölgede ileri sürmüşlerdir edilmiş A > 300, tüm bir " denge kıtası " kararlı bir hipotetik fazdan oluşan kuark madde serbest içeren, akıcı yukarı ve aşağı kuark yerine kuark , proton ve nötronlara bağlanmış, mevcut olabilir. Maddenin bu tür bir şekilde bir taban durumuna olduğu varsayımı ileri sürülmüştür Baryonik madde daha büyük bir ortalama bağlanma enerjisi ile baryon'ait daha nükleer madde zerre madde içine, bu kütle eşiğinin ötesinde nükleer maddenin çürüme lehine. Eğer maddenin bu hali mevcutsa, normal süper ağır çekirdeklere yol açan aynı füzyon reaksiyonlarında sentezlenebilir ve Coulomb itmesini yenmek için yeterli olan daha güçlü bağlanmasının bir sonucu olarak fisyona karşı stabilize edilebilir.
Son hesaplamalar ötesinde konvansiyonel çekirdeklerin karşı yukarı-aşağı kuark madde (udQM) külçelerin kararlılığını göstermektedir A ~ 266 ve ayrıca udQM külçeleri (süperkritik önceki haline göstermektedir Z'nin cr ~ 163 A ~ 609) çekirdeklerinin konvansiyonel daha ( Z cr ~ 177 A ~480).
nükleer özellikler
Sihirli sayılar ve istikrar adası
Çekirdeklerin kararlılığı sonra atom sayısının artması ile büyük ölçüde azalır küriyum , elemanın 96 bu yüzden üzerinde bir atom numarası olan tüm izotopları 101 radyoaktif bozunma bir ile yarı-ömrü arasında bir haricinde bir günden daha kısa bir, dubnium -268. İle hiçbir elementler atom numaralarına 82 (sonra yukarıdaki kurşun ) kararlı izotopları var. Bununla birlikte, henüz çok iyi anlaşılmayan nedenlerden dolayı , 110 – 114 atom numaraları etrafında hafif bir artan nükleer kararlılık vardır ve bu, nükleer fizikte " kararlılık adası " olarak bilinen şeyin ortaya çıkmasına neden olur . California Üniversitesi profesörü Glenn Seaborg tarafından önerilen bu kavram, süper ağır elementlerin neden tahmin edilenden daha uzun sürdüğünü açıklıyor .
Göreli olmayan Skyrme etkileşimini kullanan Hartree–Fock–Bogoliubov yöntemine göre hesaplamalar, kapalı bir proton kabuğu olarak Z = 126'yı önerdi . Periyodik tablonun bu bölgesinde, N = 184, N = 196 ve N = 228, kapalı nötron kabukları olarak önerilmiştir. Bu nedenle, en çok ilgi duyulan izotoplar 310 126, 322 126 ve 354 126'dır, çünkü bunlar diğer izotoplardan çok daha uzun ömürlü olabilir. Eleman 126, bir olan büyülü numarayı bir proton , bu bölgede diğer elemanlar daha stabil olduğu tahmin edilmektedir ve sahip olabilir nükleer izomerleri , çok uzun yarılanma ömürleri . Ayrıca istikrar adasının 306 122'de merkezlenmiş olması da mümkündür , ki bu küresel olabilir ve çifte büyü olabilir .
Nükleer deformasyon ve göreli etkiler hesaba katıldığında, tek parçacık seviyelerinin bir analizi, süper ağır çekirdekler için Z = 126, 138, 154 ve 164 ve N = 228, 308 ve 318'de yeni sihirli sayılar öngörür . 291 Cn, 293 Cn ve 298 Fl merkezli stabilite adası , double magic 354 126 ve 472 164 veya 482 164 çevresinde başka stabilite adaları bulunabilir. Bu çekirdeklerin beta kararlı olduğu ve alfa emisyonu ile bozunduğu tahmin edilmektedir. veya nispeten uzun yarı ömürleri olan spontan fisyon ve sırasıyla komşu N = 228 izotonlara ve 152-168 elementlerine ek stabilite sağlar . Öte yandan, aynı analiz, 354 126 gibi bazı durumlarda proton kabuğu kapanmalarının nispeten zayıf olabileceğini veya hatta mevcut olmadığını , yani bu tür çekirdeklerin çifte sihirli olmayabileceği ve bunun yerine stabilitenin öncelikle güçlü nötron kabuğu kapanışları tarafından belirleneceği anlamına gelir. Ek olarak, ikinci adadaki ( Z = 164) güçlü kuvvet tarafından üstesinden gelinmesi gereken çok büyük elektromanyetik itme kuvvetleri nedeniyle , bu bölgenin etrafındaki çekirdeklerin yalnızca rezonans olarak var olması ve anlamlı bir miktar için bir arada kalamaması mümkündür. zaman. Bu seriler arasındaki bazı süperaktinidlerin her iki adadan da çok uzakta oldukları için gerçekte var olmamaları da mümkündür, bu durumda periyodik tablo Z = 130 civarında bitebilir.
Eleman 164 ötesinde, Dilinme kendiliğinden fisyon göre stabilite sınırı tayin eden çizgisi ile birleşebilirler nötron damla hattı ağır elementler varlığı için bir sınır poz. Bununla birlikte, Z = 210, 274 ve 354 ve N = 308, 406, 524, 644 ve 772'de başka sihirli sayılar da tahmin edilmiştir ; 616 210 ve 798 274'te bulunan iki beta-kararlı çift sihirli çekirdek ; aynı hesaplama yöntemi 298 Fl ve 472 164 için tahminleri yeniden üretti. ( Z = 354 için tahmin edilen çift sihirli çekirdekler beta-kararsız, 998 354 nötron-eksik ve 1126 354 nötron açısından zengin.) Her ne kadar alfaya karşı ek stabilite bozunma ve fisyon için tahmin edilen 616 210 ve 798 , 274 için yüzlerce mikro kadar yarı ömürleri ile 616 210, tahmin edilen gibi anlamlı stabilite adaları orada mevcut olmayacaktır Z süper ağır elementlerin varlığı olarak = 114 ve 164. kapalı kabuklardan kaynaklanan stabilize edici etkilere çok güçlü bir şekilde bağlıdır, nükleer istikrarsızlık ve fisyon, muhtemelen bu kararlılık adalarının ötesinde periyodik tablonun sonunu belirleyecektir.
Keşfedilmemiş elementlerin tahmin edilen bozunma özellikleri
Ana kararlılık adasının 291 Cn ve 293 Cn civarında olduğu düşünüldüğünden , oganessonun ötesinde keşfedilmemiş elementler çok kararsız olabilir ve mikrosaniye veya daha kısa sürede alfa bozunumuna veya kendiliğinden fisyona uğrayabilir . Yarı ömürlerin bir mikrosaniyeyi aştığı kesin bölge bilinmemekle birlikte, çeşitli modeller , mevcut hedefler ve mermilerle füzyon reaksiyonlarında üretilebilecek unbinilium'dan daha ağır elementlerin izotoplarının bir mikrosaniyenin altında yarı ömürlere sahip olacağını ve bu nedenle, olamayacaklarını öne sürmektedir. saptanmış. N = 184 ve N = 228'de ve muhtemelen ayrıca Z ~ 124 ve N ~ 198'de de kararlılık bölgelerinin bulunacağı tutarlı bir şekilde tahmin edilmektedir . Bu çekirdeklerin yarılanma ömrü birkaç saniye olabilir ve ağırlıklı olarak alfa bozunumuna uğrayabilir ve spontane olabilir. fisyon, küçük beta artı bozunma (veya elektron yakalama ) dalları da mevcut olabilir. Geliştirilmiş stabilite, bu bölgelerin dışında, fizyon engeller altında fisyon yarı ömür ile sonuçlanan bu sabitleme etkileri kaybı önemli ölçüde düşmesi beklenmektedir 10 -18 , özellikle de saniye çift çift çekirdeğin engelleme da nedeniyle daha düşük olduğu için nucleon eşleştirme . Genel olarak, alfa bozunma yarı ömürlerinin, nötron sayısıyla birlikte, en nötron eksikliği olan izotoplardaki nanosaniyelerden beta-kararlılık çizgisine daha yakın saniyelere kadar artması beklenir . Sihirli bir sayıdan yalnızca birkaç nötronu fazla olan çekirdekler için, bağlanma enerjisi önemli ölçüde düşer, bu da trendde bir kırılmaya ve daha kısa yarı ömürlere neden olur. Bu elementlerin en nötron eksikliği olan izotopları da bağlanmamış olabilir ve proton emisyonuna uğrayabilir . Küme bozunması (ağır parçacık emisyonu), bazı izotoplar için alternatif bir bozunma modu olarak önerilmiştir ve bu elementlerin tanımlanmasına bir başka engel teşkil etmektedir.
Elektron konfigürasyonları
Aşağıdakiler, 119-173 ve 184 numaralı elementlerin beklenen elektron konfigürasyonlarıdır. [Og] sembolü, şu anda bilinen son element olan oganessonun (Z = 118) olası elektron konfigürasyonunu gösterir. Bu tablodaki elemanların konfigürasyonları [Og] ile başlayarak yazılmıştır, çünkü oganesson'un kapalı kabuklu (inert gaz) konfigürasyonlu son önceki eleman olması beklenir, 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 4d 10 4f 14 5s 2 5p 6 5d 10 5f 14 6s 2 6p 6 6d 10 7s 2 7p 6 .
Öğe 123'ün ötesinde tam hesaplamalar mevcut değildir ve bu nedenle bu tablodaki veriler geçici olarak alınmalıdır . 123 nolu element ve belki de daha ağır elementler söz konusu olduğunda, birkaç olası elektron konfigürasyonunun çok benzer enerji seviyelerine sahip olduğu tahmin edilmektedir, öyle ki temel durumu tahmin etmek çok zordur . Önerilen tüm konfigürasyonlar (Madelung kuralının muhtemelen burada çalışmayı bıraktığı anlaşıldığından) dahil edilmiştir.
172'ye kadar tahmin edilen blok atamaları, beklenen mevcut değerlik orbitallerini izleyen Kulsha'lardır. Bununla birlikte, literatürde, eleman 138'den sonra blokların nasıl çalışması gerektiği konusunda bir fikir birliği yoktur.
Kimyasal element Engellemek Öngörülen elektron konfigürasyonları 119 Uue Ununenyum s bloğu [Og] 8s 1 120 übn unbinilyum s bloğu [Og] 8s 2 121 Ubu unbiunyum g bloğu [Og] 8s 2 8p1
1/2122 ubb unbibiyum g bloğu [Og] 8s 2 8p2
1/2
[Og] 7d 1 8s 2 8p1
1/2123 ubt unbitrium g bloğu [Og] 6f 1 8s 2 8p2
1/2
[Og] 6f 1 7d 1 8s 2 8p1
1/2
[Og] 6f 2 8s 2 8p1
1/2
[Og] 8s 2 8p2
1/2 8p1
3/2124 Ubq unbiquadyum g bloğu [Og] 6f 2 8s 2 8p2
1/2
[Og] 6f 3 8s 2 8p1
1/2125 UBP unbipentium g bloğu [Og] 6f 4 8s 2 8p1
1/2
[Og] 5g 1 6f 2 8s 2 8p2
1/2
[Og] 5g 1 6f 3 8s 2 8p1
1/2
[Og] 8s 2 0.81(5g 1 6f 2 8p2
1/2) + 0.17(5g 1 6f 1 7d 2 8p1
1/2) + 0.02(6f 3 7d 1 8p1
1/2)126 uhh unbihexium g bloğu [Og] 5g 1 6f 4 8s 2 8p1
1/2
[Og] 5g 2 6f 2 8s 2 8p2
1/2
[Og] 5g 2 6f 3 8s 2 8p1
1/2
[Og] 8s 2 0.998(5g 2 6f 3 8p1
1/2) + 0.002(5g 2 6f 2 8p2
1/2)127 Ub'ler unbiseptium g bloğu [Og] 5g 2 6f 3 8s 2 8p2
1/2
[Og] 5g 3 6f 2 8s 2 8p2
1/2
[Og] 8s 2 0.88(5g 3 6f 2 8p2
1/2) + 0.12(5g 3 6f 1 7d 2 8p1
1/2)128 Ubo biyolojik olmayan g bloğu [Og] 5g 3 6f 3 8s 2 8p2
1/2
[Og] 5g 4 6f 2 8s 2 8p2
1/2
[Og] 8s 2 0.88(5g 4 6f 2 8p2
1/2) + 0.12(5g 4 6f 1 7d 2 8p1
1/2)129 übe iki yıllık g bloğu [Og] 5g 4 6f 3 7d 1 8s 2 8p1
1/2
[Og] 5g 4 6f 3 8s 2 8p2
1/2
[Og] 5g 5 6f 2 8s 2 8p2
1/2
[Og] 5g 4 6f 3 7d 1 8s 2 8p1
1/2130 Utn untrinilium g bloğu [Og] 5g 5 6f 3 7d 1 8s 2 8p1
1/2
[Og] 5g 5 6f 3 8s 2 8p2
1/2
[Og] 5g 6 6f 2 8s 2 8p2
1/2
[Og] 5g 5 6f 3 7d 1 8s 2 8p1
1/2131 Utu untriunyum g bloğu [Og] 5g 6 6f 3 8s 2 8p2
1/2
[Og] 5g 7 6f 2 8s 2 8p2
1/2
[Og] 8s 2 0.86(5g 6 6f 3 8p2
1/2) + 0.14(5g 6 6f 2 7d 2 8p1
1/2)132 utb untribiyum g bloğu [Og] 5g 7 6f 3 8s 2 8p2
1/2
[Og] 5g 8 6f 2 8s 2 8p2
1/2133 utt tritriyum g bloğu [Og] 5g 8 6f 3 8s 2 8p2
1/2134 Utq üç dörtlük olmayan g bloğu [Og] 5g 8 6f 4 8s 2 8p2
1/2135 Utp untripentium g bloğu [Og] 5g 9 6f 4 8s 2 8p2
1/2136 Uh untrihexium g bloğu [Og] 5g 10 6f 4 8s 2 8p2
1/2137 uts untriseptium g bloğu [Og] 5g 11 6f 4 8s 2 8p2
1/2138 Sende untrioktiyum g bloğu [Og] 5g 12 6f 4 8s 2 8p2
1/2
[Og] 5g 12 6f 3 7d 1 8s 2 8p2
1/2139 Ute untrienyum g bloğu [Og] 5g 13 6f 3 7d 1 8s 2 8p2
1/2
[Og] 5g 13 6f 2 7d 2 8s 2 8p2
1/2140 Uqn unquadnilyum g bloğu [Og] 5g 14 6f 3 7d 1 8s 2 8p2
1/2
[Og] 5g 15 6f 1 8s 2 8p2
1/2 8p2
3/2141 Uqu unquadunium g bloğu [Og] 5g 15 6f 2 7d 2 8s 2 8p2
1/2142 Uqb unquadbium g bloğu [Og] 5g 16 6f 2 7d 2 8s 2 8p2
1/2143 Uqt dörtlü olmayan f bloğu [Og] 5g 17 6f 2 7d 2 8s 2 8p2
1/2144 Uqq dörtlü olmayan f bloğu [Og] 5g 18 6f 2 7d 2 8s 2 8p2
1/2
[Og] 5g 18 6f 1 7d 3 8s 2 8p2
1/2
[Og] 5g 17 6f 2 7d 3 8s 2 8p2
1/2
[Og] 8s 2 0,95(5g 17 6f 2 7d 3 8p2
1/2) + 0.05(5g 17 6f 4 7d 1 8p2
1/2)145 Uqp dörtgen olmayan f bloğu [Og] 5g 18 6f 3 7d 2 8s 2 8p2
1/2146 uqh unquadhexium f bloğu [Og] 5g 18 6f 4 7d 2 8s 2 8p2
1/2147 Uq'lar unquadseptium f bloğu [Og] 5g 18 6f 5 7d 2 8s 2 8p2
1/2148 Uqo unquadoctium f bloğu [Og] 5g 18 6f 6 7d 2 8s 2 8p2
1/2149 Uqe unquadenium f bloğu [Og] 5g 18 6f 6 7d 3 8s 2 8p2
1/2150 yukarı unpentilyum f bloğu [Og] 5g 18 6f 6 7d 4 8s 2 8p2
1/2
[Og] 5g 18 6f 7 7d 3 8s 2 8p2
1/2151 Upu unpentunyum f bloğu [Og] 5g 18 6f 8 7d 3 8s 2 8p2
1/2152 yukarı Pentbiyum f bloğu [Og] 5g 18 6f 9 7d 3 8s 2 8p2
1/2153 yukarı penttriyum f bloğu [Og] 5g 18 6f 10 7d 3 8s 2 8p2
1/2
[Og] 5g 18 6f 11 7d 2 8s 2 8p2
1/2154 Upq pentquadium f bloğu [Og] 5g 18 6f 11 7d 3 8s 2 8p2
1/2
[Og] 5g 18 6f 12 7d 2 8s 2 8p2
1/2155 upp Penpentium f bloğu [Og] 5g 18 6f 12 7d 3 8s 2 8p2
1/2
[Og] 5g 18 6f 13 7d 2 8s 2 8p2
1/2156 yukarı unpentexium f bloğu [Og] 5g 18 6f 13 7d 3 8s 2 8p2
1/2
[Og] 5g 18 6f 14 7d 2 8s 2 8p2
1/2157 Güç kaynağı pentseptyum d-blok [Og] 5g 18 6f 14 7d 3 8s 2 8p2
1/2158 Upo pentoktiyum d-blok [Og] 5g 18 6f 14 7d 4 8s 2 8p2
1/2159 yukarı Pentenyum d-blok [Og] 5g 18 6f 14 7d 5 8s 2 8p2
1/2
[Og] 5g 18 6f 14 7d 4 8s 2 8p2
1/29s 1160 Ahh altıgen olmayan d-blok [Og] 5g 18 6f 14 7d 6 8s 2 8p2
1/2
[Og] 5g 18 6f 14 7d 5 8s 2 8p2
1/29s 1161 uhu altıgen olmayan d-blok [Og] 5g 18 6f 14 7d 7 8s 2 8p2
1/2
[Og] 5g 18 6f 14 7d 6 8s 2 8p2
1/29s 1162 uhb unheksbiyum d-blok [Og] 5g 18 6f 14 7d 8 8s 2 8p2
1/2
[Og] 5g 18 6f 14 7d 7 8s 2 8p2
1/29s 1163 ahh altıgen olmayan d-blok [Og] 5g 18 6f 14 7d 9 8s 2 8p2
1/2
[Og] 5g 18 6f 14 7d 8 8s 2 8p2
1/29s 1164 uhq altı köşeli olmayan d-blok [Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/2165 uhp altıgen olmayan d-blok [Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/29s 1166 Ahh unhexhexium d-blok [Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/29s 2167 Ahs altıgen olmayan p-blok [Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/29s 2 9p1
1/2
[Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/2 8p1
3/29s 2168 uho heksoktiyum olmayan p-blok [Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/29s 2 9p2
1/2
[Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/2 8p2
3/29s 2169 uhe altıgen olmayan p-blok [Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/2 8p1
3/29s 2 9p2
1/2
[Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/2 8p3
3/29s 2170 usn unseptilyum p-blok [Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/2 8p2
3/29s 2 9p2
1/2
[Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/2 8p4
3/29s 2171 Usu unseptunyum p-blok [Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/2 8p3
3/29s 2 9p2
1/2
[Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/2 8p4
3/29s 2 9p1
1/2172 USB unseptbiyum p-blok [Og] 5g 18 6f 14 7d 10 8s 2 8p2
1/2 8p4
3/29s 2 9p2
1/2173 Ust septtriyum ? [Usb] 6g 1
[Usb] 9p1
3/2... ... ... ... ... 184 Uoq Unoctquadium ? [Usb] 6g 5 7f 4 8d 3
Ayrıca bakınız
Referanslar
daha fazla okuma
- Kaldor, U. (2005). "Süper Ağır Elementler-Kimya ve Spektroskopi". Hesaplamalı Kimya Ansiklopedisi . doi : 10.1002/0470845015.cu0044 . ISBN'si 978-0470845011.
- Seaborg, GT (1968). "100'ün Ötesindeki Unsurlar, Mevcut Durum ve Gelecek Beklentileri" . Nükleer Bilimin Yıllık İncelemesi . 18 : 53–152. Bibcode : 1968ARNPS..18...53S . doi : 10.1146/annurev.ns.18.120168.000413 .
- Scerri, Eric. (2011). Periyodik Tabloya Çok Kısa Bir Giriş, Oxford University Press, Oxford . ISBN'si 978-0-19-958249-5.
Dış bağlantılar
- Holler, Jim. "G-orbitallerinin görüntüleri" . Kentucky Üniversitesi.
- Rihani, Jeries A. " Elementlerin genişletilmiş periyodik tablosu" .
- Scerri, Eric. "Elementler ve periyodik tablo için Eric Scerri'nin web sitesi" .