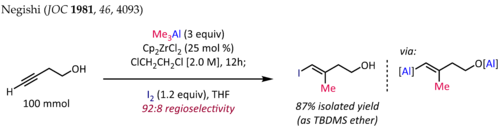Organoalüminyum kimyası - Organoaluminium chemistry
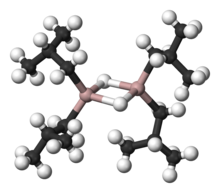
Organoalüminyum kimyası , karbon ve alüminyum arasındaki bağları içeren bileşiklerin incelenmesidir . Organometalik kimyadaki ana temalardan biridir . Örnek organoalüminyum bileşikleri, dimer trimetilalüminyum , monomer triizobütilalüminyum ve Tebbe reaktifi olarak adlandırılan titanyum-alüminyum bileşiğidir . Organoalüminyum bileşiklerinin davranışı, C-Al bağının polaritesi ve üç koordineli türün yüksek Lewis asitliği açısından anlaşılabilir . Endüstriyel olarak, bu bileşikler esas olarak poliolefinlerin üretimi için kullanılır .
Tarih
İlk organoalüminyum bileşiği (C 2 H 5 ) 3 , Al 2 I 3 1859. Organoalüminyum bileşikler keşfedilmiştir, ancak çok az 1950 yılına kadar bilinen edildi Karl Ziegler ve arkadaşları trialkil alüminyum bileşiklerinin doğrudan sentezini bulmuştur ve katalitik bu bileşikleri uygulanan olefin polimerizasyon . Bu araştırma dizisi nihayetinde Ziegler'e Nobel Ödülü ile sonuçlandı.
Yapı ve yapıştırma
Alüminyum(III) bileşikleri
Organoalüminyum bileşikleri genellikle üç ve dört koordinatlı Al merkezlerine sahiptir, ancak florür gibi inorganik ligandlarda daha yüksek koordinasyon sayıları gözlemlenir . Alışılmış eğilimlere uygun olarak, dört koordinatlı Al, tetrahedral olmayı tercih ediyor. Borun aksine, alüminyum daha büyük bir atomdur ve dört karbon ligandını kolayca barındırır. Triorganoaluminium bileşikler bu nedenle, bir çift genellikle dimerik köprü alkil ligandları, örneğin, Al 2 (Cı- 2 , H 5 ) 4 (μ-Cı- 2 , H 5 ) 2 . Böylece, trietilalüminyum ortak adına rağmen, bu bileşik iki alüminyum merkez ve altı etil grubu içerir . Organoalüminyum bileşiği hidrit veya halojenür içerdiğinde , bu daha küçük ligandlar köprüleme bölgelerini işgal etme eğilimindedir. Zaman üç koordinasyon meydana R grupları , örneğin, Al kütlelidir (MES) 3 (Mes = 2,4,6-Me 3 C 6 , H 2 ve mesitil ) ya da izobutildir.

trialkilalüminyum bileşiklerinde ligand değişimi
Trialkilalüminyum dimerleri genellikle dinamik dengeye katılır, bu da dimerler arasındaki ligand değişiminin yanı sıra köprüleme ve terminal ligandların değişimi ile sonuçlanır. Koordine olmayan çözücülerde bile Al-Me değişimi, proton NMR spektroskopisi ile teyit edildiği gibi hızlıdır . Örneğin, -25 ° C'de 1 Me H NMR spektrumu 6 Al 2 içeren istem 1 içinde iki sinyal: 2 oranında, katı hal yapısından beklendiği gibi. 20 °C'de, terminal ve köprü metil gruplarının değişimi NMR tarafından çözülemeyecek kadar hızlı olduğu için sadece bir sinyal gözlemlenir. Monomerik türlerin yüksek Lewis asitliği, Al(III) merkezinin boyutu ve bir oktet konfigürasyonu elde etme eğilimi ile ilgilidir .
Düşük oksidasyon durumlu organoalüminyum bileşikleri
Al-Al bağına sahip ilk organoalüminyum bileşiği 1988'de (((Me 3 Si) 2 CH) 2 Al) 2 (bir dialan) olarak rapor edildi. Tipik olarak dialkilalüminyum klorürlerin metalik potasyum ile indirgenmesiyle hazırlanırlar:
- (R 2 AlCl) 2 + 2 K → R 2 Al-AlR 2 + 2 KCl
Bir diğer dikkate değer alan grubu, dört Al(I) merkezi içeren tetraalanlardır. Bu bileşikler, bir kabul tetrahedrane (gösterildiği gibi, göbek Cp * Al) 4 ve ((Me 3 Si 3 ° C), Al) 4 . [Al 12 ( i-Bu ) 12 ] 2− kümesi , organoalüminyum bileşiklerinin indirgenmesiyle ilgili araştırmalardan elde edilmiştir. Bu dianyon, dodecaboratı ([B 12 H 12 ] 2− ) andıran ikosahedral bir yapıya sahiptir . Resmi oksidasyon durumu birden azdır.
Hazırlık
Alkil halojenürler ve alüminyumdan
Endüstriyel olarak, Al tipi basit alüminyum alkiller 2 R, 6 (R = Me, Et) ile başlayan bir iki-aşamalı yöntemde hazırlanmış olan alkilasyon alüminyum tozu:
- 2, Al + 3, CH 3 CH 2 Cı → (CH 3 CH 2 ) 3 , Al 2 Cı 3
Reaksiyon, Grignard reaktiflerinin sentezine benzer . Ürün, (CH 3 CH 2 ) 3 , Al 2 Cı 3 olarak adlandırılır etilaluminyum seskiklorür . Seskiklorür terimi, ortalama olarak Cl:Al oranının 1.5 olduğu gerçeğini ifade eder. Bu seskiklorürler, indirgeme yoluyla triorganoalüminyum türevlerine dönüştürülebilir:
- 2 (CH 3 CH 2 ) 3 Al 2 Cl 3 + 6 Na → (CH 3 CH 2 ) 6 Al 2 + 2 Al + 6 NaCl
Bu yöntem, trimetilalüminyum ve trietilalüminyum üretimi için kullanılır .
hidroalüminasyon
Alüminyum tozu, hidrojen varlığında belirli terminal alkenlerle doğrudan reaksiyona girer. İşlem, ilki dialkilalüminyum hidrit üreten iki adımdan oluşur. Bu tür reaksiyonlar tipik olarak yüksek sıcaklıklarda yürütülür ve trialkilalüminyum reaktifleri ile aktivasyon gerektirir:
- 6 Al + 3 H 2 + 12 CH 2 =CHR → 2 [HAl(CH 2 CHR) 2 ] 3
Hacimli olmayan R grupları için organoalüminyum hidritler tipik olarak trimeriktir. Bir sonraki adımda, bu hidritler, hidroalüminasyonun gerçekleştirilmesi için daha fazla alken ile işlenir:
- 2 [HAl(CH 2 CHR) 2 ] 3 + 3 CH 2 =CHR → 3 [Al 2 (CH 2 CHR) 3
Dimerik olan diizobutilalüminyum hidrit , triizobütilalüminyumdan hidrit eliminasyonu ile hazırlanır:
- 2 i -Bu 3 Al → ( i -Bu 2 AlH) 2 + 2 (CH 3 ) 2 , C = CH 2
karboalüminasyon
Organoalüminyum bileşikleri, alkenler ve alkinlerle reaksiyona girerek, çoklu bağ boyunca bir organil grubu ve metal parçasının net eklenmesiyle (karboalüminasyon) sonuçlanabilir. Bu işlem, tamamen termal bir şekilde veya bir geçiş metali katalizörü varlığında ilerleyebilir. Katalizlenmemiş işlem için, mono ilave sadece alken ikame edildiğinde mümkündür. Etilen için, karboalüminasyon , daha yüksek alkilalüminyum türlerinin Poisson dağılımına yol açar . Reaksiyon 1-alkenler için bölgesel seçicidir. İlk olarak Ei-ichi Negishi tarafından bildirilen ZACA reaksiyonu olarak adlandırılan reaksiyon , bir kiral zirkonosen katalizörü tarafından katalize edilen alkenlerin asimetrik karboalüminasyonunun bir örneğidir.
Cp varlığında alkinlerin methylalumination 2 ZrCl 2 stereodefined tri-ikame edilmiş olefin fragmanların sentezine, terpenin ortak bir alt için kullanılan ve doğal ürünler poliketid olan. Aşağıda gösterilen ( E )-4-iyodo-3-metilbut-3-en-1-ol sentezi , bu reaksiyonun tipik bir uygulamasıdır:
Terminal alkinler için reaksiyon , propargilik veya homopropargilik heteroatom ikame edicilerinin varlığında bile, genellikle iyi bir bölgesel seçicilik (>90:10 rr) ve tam eş seçicilik ile ilerler. Ne yazık ki, zirkonosen katalizli metilalüminasyonun daha yüksek alkillerle alkilalüminasyona uzatılması, daha düşük verimler ve zayıf bölgesel seçiciliklerle sonuçlanır.
Laboratuvar hazırlıkları
Basit elemanlar ticari olarak düşük maliyetle temin edilebilmesine rağmen, metatez veya transmetalasyon dahil olmak üzere laboratuvarda sentezleri için birçok yöntem geliştirilmiştir . Alüminyum triklorürün RLi veya RMgX ile metatezi trialkili verir:
- AlCl 3 + 3 BuLi → Bu 3 Al + 3 LiCl
- Transmetalasyon
- 2 Al + 3 HgPh 2 → 2 AlPh 3 + 3 Hg
Reaksiyonlar
Organoalüminyum bileşiklerinin elektrofillere karşı yüksek reaktivitesi, alüminyum ve karbon atomu arasındaki yük ayrımına atfedilir .
Lewis asitliği
Organoalüminyum bileşikleri sert asitlerdir ve piridin , THF ve üçüncül aminler gibi bazlarla kolaylıkla katkı maddeleri oluştururlar . Bu eklentiler Al'de tetrahedraldir.
elektrofiller
Al-C bağı, karbon oldukça bazik olacak şekilde polarize edilmiştir. Asitler reaksiyona girerek alkanlar verir. Örneğin, alkoller alkoksitler verir :
- AlR' 3 + ROH → 1/n (R' 2 Al-OR) n + R'H
Basit mineral asitlerin ötesinde çok çeşitli asitler kullanılabilir. Aminler amido türevleri verir. İle , karbon dioksit , trialkil alüminyum bileşikleri vermek dialkylaluminium karboksilat ve daha sonra alkil alüminyum dikarboksilatlar:
- HAVA 3 + CO 2 → R, 2 AIO 2 CR
- R 2 AlO 2 CR + CO 2 → RAL(O 2 CR) 2
Dönüşüm, Grignard reaktiflerinin karbonatlaşmasını andırıyor .
Benzer şekilde, trialkilalüminyum bileşikleri ve karbon dioksit arasındaki reaksiyon, alkolleri, olefinleri veya ketonları sentezlemek için kullanılmıştır.
Oksijen ile alkollere hidrolize edilebilen ilgili alkoksitler elde edilir:
- AlR 3 + 3/2 O 2 → Al(OR) 3
Yapısal olarak, özelliği organo alüminyum peroksit olan [{HC [C (Me) N 6 H 5 ] 2 } AI (R) -OO- CMe 3 ] [R = CH (SiMe 3 ) 2 ].
Saf trialalkilalüminyum bileşikleri ile su , alkoller , fenoller , aminler , karbon dioksit , kükürt oksitler , nitrojen oksitler , halojenler ve halojenli hidrokarbonlar arasındaki reaksiyon şiddetli olabilir.
alken polimerizasyonu
Endüstriyel olarak, organoalüminyum bileşikleri, örneğin metilalüminoksan katalizörü gibi poliolefinlere alken polimerizasyonu için katalizörler olarak kullanılır .