Oddo-Harkins kuralı - Oddo–Harkins rule
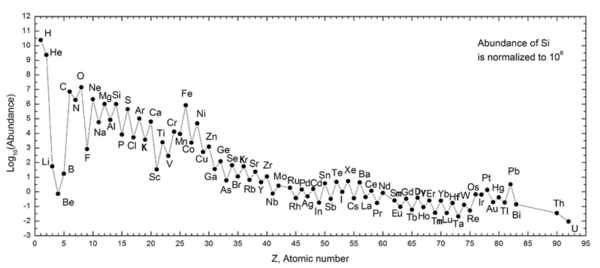
Oddo-Harkins kuralı , bir o tutan eleman (örneğin, bir çift atom numarası ile karbon : elemanı gibi bitişik daha büyük ve daha küçük tek atom numaraları ile her iki eleman (daha bol olan 6) bor elemanı 5 ve: azot , elemanı 7: sırasıyla karbon için ). Kimyasal elementlerin bolluğunun bu eğilimi ilk olarak 1914'te Giuseppe Oddo ve 1917'de William Draper Harkins tarafından rapor edildi .
Tanım
Hidrojenden daha büyük tüm atomlar , yerçekimi , sıcaklık ve basınç protonları ve nötronları birbirine kaynaştıracak kadar yüksek seviyelere ulaştığında nükleosentez yoluyla yıldızlarda veya süpernovalarda oluşur . Protonlar ve nötronlar, atomları oluşturmak için elektronları biriktiren atom çekirdeğini oluşturur. Çekirdekteki atom numarası olarak adlandırılan proton sayısı, bir kimyasal elementi benzersiz şekilde tanımlar.
Oddo-Harkins kuralı, tek atom numaralı elementlerin eşleşmemiş bir protona sahip olduğunu ve başka bir protonu yakalama olasılığının daha yüksek olduğunu ve dolayısıyla atom numaralarını arttırdığını iddia eder. Çift atom numarasına sahip elementlerde, protonların , çiftin her bir üyesinin diğerinin dönüşünü dengeleyecek şekilde eşleştirilmesi mümkündür; eşit eşitlik böylece nükleon stabilitesini arttırır.
Kuralın istisnaları
Bununla birlikte, bu varsayım, evrenin en bol bulunan ve elementlerin periyodik tablosundaki en basit elementi için geçerli değildir : atom numarası 1 olan hidrojen . Bunun nedeni, iyonize formunda bir hidrojen atomunun tek bir proton haline gelmesi olabilir. Büyük Patlama'nın ardından, Evren'in enflasyon döneminin ilk saniyesinde kuarkların ilk büyük kümelerinden biri olduğu teorisine göre . Evrenin şişmesinin onu sonsuz küçük bir noktadan yaklaşık modern bir galaksinin büyüklüğüne getirdiği bu dönemde, parçacık çorbasındaki sıcaklıklar bir trilyon dereceden birkaç milyon dereceye düştü.
Bu süre , tekli protonların ve döteryum çekirdeklerinin füzyonunun helyum ve lityum çekirdekleri oluşturmasına izin verdi, ancak her H + iyonunun daha ağır elementlere dönüştürülmesi için çok kısaydı . Bu durumda, atom numarası 2 olan helyum, hidrojenin çift sayılı karşılığı olarak kalır. Böylece, nötr hidrojen - veya bir elektronla eşleştirilmiş hidrojen , tek kararlı lepton - şişmenin sona ermesinin ardından maddenin geriye kalan imha edilmemiş kısımlarının büyük çoğunluğunu oluşturuyordu .
Kuralın diğer bir istisnası , çift atom numarasıyla (4) bile, her iki tarafındaki tek sayılı elementlerden ( lityum ve bor ) daha nadir görülen berilyumdur . Bunun nedeni, evrenin lityum, berilyum ve borunun çoğunun , sıradan yıldız nükleosentezi değil, kozmik ışın spallasyonu ile oluşması ve berilyumun yalnızca bir kararlı izotopu olması ve her ikisinin de iki kararlı izotoplar.
Füzyon ilişkisi
Model, ölmekte olan büyük bir yıldızdaki kaçak füzyonun meydana gelmesinden sonra ortaya çıkar; burada çeşitli çift ve tek numaralı elementlerin belirli bir kütlesi, hidrojen ve helyum elementlerinin biraz daha büyük bir kütlesiyle oluşur. Yeni oluşan elementler patlamayla fırlatılır ve sonunda galaksinin geri kalan yıldızlararası ortamına katılır .
Füzyon daha büyük ve daha büyük çekirdeklerle gerçekleştiğinde, enerji girdisi giderek daha büyük hale gelir ve enerji çıkışı giderek daha küçük hale gelir; Bu iki potansiyelin periyodik cetvelde buluştuğu nokta demir , atom numarası 26 ve nikel , atom numarası 28 etrafında bir yerdedir . Bundan daha ağır elementlerin füzyonu enerji açığa çıkarmaz ve bu nedenle tutarsızlık bulma olasılığı Oddo – Harkins kuralında daha düşük hale gelir.
Ayrıca bakınız
- Atomik numara
- Hidrojen
- Kozmik enflasyon
- İzotopların kararlılığına göre elementlerin listesi
- Nükleer füzyon
- Nükleer kimya
