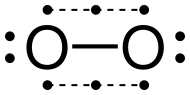
Oksijenin allotropları - Allotropes of oxygen
Oksijenin bilinen birkaç allotropu vardır . En bilineni, Dünya atmosferinde önemli seviyelerde bulunan ve dioksijen veya üçlü oksijen olarak da bilinen moleküler oksijendir (O 2 ) . Bir diğeri ise oldukça reaktif ozondur (O 3 ). Diğerleri:
- Atomik oksijen (O 1 ), bir serbest radikal .
- Singlet oksijen (O 2 *), moleküler oksijenin iki yarı kararlı durumundan biri.
- Tetraoksijen (O 4 ), başka bir yarı kararlı form.
-
Biri O olan altı farklı renkte fazda bulunan katı oksijen
8 ve bir diğeri metalik.
atomik oksijen
Oksijen atomları, belirtilen O ( 3 oksijen tek atomuna yakın molekülleri ile hızlı bir şekilde bir bağ eğilimi gibi P) ya da O (3P), çok reaktiftir. Dünya yüzeyinin üzerinde çok uzun süre doğal olarak var olmayan, ancak içinde uzaydan , bol varlığı ultraviyole radyasyonu bir sonuçlardan Alçak bir yörüngede atmosferde hangi oksijenin% 96 atom şeklinde ortaya çıkar.
Mars'ta Mariner , Viking ve SOFIA gözlemevi tarafından atomik oksijen tespit edildi .
dioksijen
Dünyadaki temel oksijenin ortak allotropu, O
2, Genellikle oksijen olarak bilinir, ancak denebilir dioksijen , iki atomlu oksijen , moleküler oksijen veya oksijen gazı elemanı kendisinden ve triatomic Allotrop ayırmak için ozon , O
3. Dünya atmosferinin önemli bir bileşeni (hacimce yaklaşık %21) olarak , elementel oksijene en yaygın olarak diyatomik formda rastlanır. Aerobik organizmalar , hücresel solunumdaki terminal oksidan olan atmosferik dioksijenin zayıf sigma bağında depolanan kimyasal enerjiyi serbest bırakır . Temel durum dioksijenin olarak bilinen , triplet oksijenden , 3 O 2 iki çiftlenmemiş elektrona sahip olduğu için,. İlk uyarılmış durum, singlet oksijen , 1 O 2, eşleşmemiş elektronlara sahip değildir ve yarı kararlıdır . İkili durum elektron tek sayıda gerektirir ve bu nedenle bu gibi elektronları kazanma-kaybetmeden dioksijen içinde olamaz süperoksit (iyon O-
2) veya dioksijenil iyonu ( O+
2).
O'nun temel durumu
2121 pm'lik bir bağ uzunluğuna ve 498 kJ/mol'lük bir bağ enerjisine sahiptir. Kaynama noktası -183 °C (90 K; -297 °F) olan renksiz bir gazdır. Kaynama noktası -196 °C (77 K; -321 °F) olan sıvı nitrojen ile soğutularak havadan yoğunlaştırılabilir. Sıvı oksijenin rengi soluk mavidir ve eşleşmemiş elektronlar nedeniyle oldukça belirgin bir şekilde paramanyetiktir ; Bir ip tarafından asılı duran bir şişede bulunan sıvı oksijen, bir mıknatıs tarafından çekilir.
tekli oksijen
Singlet oksijen , temel durumdaki triplet oksijenden daha yüksek enerjiye sahip iki yarı kararlı moleküler oksijen (O 2 ) durumu için kullanılan ortak addır . Elektron kabuklarındaki farklılıklar nedeniyle, tekli oksijen, farklı dalga boylarında ışığı emme ve yayma dahil, üçlü oksijenden farklı kimyasal ve fiziksel özelliklere sahiptir. Gül bengal , metilen mavisi veya porfirinler gibi boya moleküllerinden enerji transferi yoluyla veya hidrojen trioksitin suda kendiliğinden ayrışması veya hidrojen peroksitin hipoklorit ile reaksiyonu gibi kimyasal işlemlerle ışığa duyarlı hale getirilmiş bir işlemde üretilebilir .
Ozon
Triatomik oksijen (ozon, O 3 ), standart sıcaklık ve basınçta soluk mavi bir gaz olan oksijenin çok reaktif bir allotropudur . Sıvı ve katı Ç 3 sıradan O daha derin mavi renk var 2 ve onlar kararsız ve patlayıcıdır. Gaz halindeyken ozon, kauçuk ve kumaş gibi maddelere zarar verir ve akciğer dokusuna zarar verir . Hava elektriksel deşarja maruz kaldığında oluştuğu için elektrik motorlarından , lazer yazıcılardan ve fotokopi makinelerinden gelen keskin, klor benzeri bir koku olarak izleri tespit edilebilir . 1840 yılında Christian Friedrich Schönbein tarafından eski Yunanca ὄζειν (ozein: "koklamak") artı -on son eki tarafından "ozon" olarak adlandırıldı ve o sırada türetilmiş bir bileşiği belirtmek için yaygın olarak kullanıldı ve -one olarak İngilizceleştirildi .
Ozon termodinamik olarak kararsızdır ve daha yaygın olan dioksijen formuna tepki verme eğilimindedir. Bu sağlam O reaksiyonu ile oluşturulmaktadır 2 olduğunda atomik oksijen ile- üretilen UV radyasyonu olarak üst atmosfer O böler 2 . Ozon, ultraviyole ve stratosferde güçlü bir şekilde emilir ve stratosferde , güneş UV radyasyonunun mutajenik ve diğer zararlı etkilerine karşı biyosfer için bir kalkan görevi görür (bkz. ozon tabakası ). Troposferik ozon, otomobillerin egzozunda azot dioksitin fotokimyasal olarak parçalanmasıyla Dünya yüzeyinin yakınında oluşur . Yer seviyesindeki ozon , yaşlılar, çocuklar ve amfizem , bronşit ve astım gibi kalp ve akciğer rahatsızlıkları olan kişiler için özellikle zararlı olan bir hava kirleticidir . Bağışıklık sistemi , bir antimikrobiyal olarak ozon üreten (aşağıya bakınız).
döngüsel ozon
Siklik ozonun teorik olarak önceden O'dur 3 molekülü bir eşkenar üçgen yerine açık bir açı oksijen bağının üç atomu içerir.
tetraoksijen
Tetraoksijen, oxozone olarak bilindiği 1900'lerin başlarından beri var olduğundan şüpheleniliyordu. 2001 yılında Roma Üniversitesi'nde Fulvio Cacace liderliğindeki bir ekip tarafından tanımlandı. O molekülü
4Daha sonra O olarak tanımlanan katı oksijenin fazlarından birinde olduğu düşünülüyordu.
8. Cacace'in ekibi, O'nun
4muhtemelen iki dambıl benzeri O'dan oluşur
2 indüklenmiş dipol dağılım kuvvetleri tarafından gevşek bir şekilde bir arada tutulan moleküller.
Katı oksijenin evreleri
Katı oksijenin bilinen altı farklı fazı vardır. Bunlardan biri koyu kırmızı bir O
8küme. Oksijen, 96 GPa'lık bir basınca maruz kaldığında, hidrojene benzer şekilde metalik hale gelir ve selenyum (temel durumunda pembe-kırmızı bir renk sergileyen), tellür ve polonyum gibi daha ağır kalkojenlere daha çok benzer hale gelir. , her ikisi de önemli metalik karakter gösterir. Çok düşük sıcaklıklarda bu faz da süper iletken hale gelir .
Referanslar
daha fazla okuma
- Parklar, GD; Mellor, JW (1939). Mellor'un Modern İnorganik Kimyası (6. baskı). Londra: Longmans, Green and Co.
- Stwertka, Albert (1998). Öğeler Kılavuzu (Revize ed.). Oxford Üniversitesi Yayınları. ISBN'si 0-19-508083-1.