Lewis asit katalizi - Lewis acid catalysis
İçinde Lewis asidi katalizi organik reaksiyonlar, bir metal bazlı Lewis asidi , bir alt-tabaka reaktivitesini artırmak üzere bir elektron çifti alıcısına olarak hareket eder. Yaygın Lewis asit katalizörleri, alüminyum , boron , silikon ve kalay gibi ana grup metallerin yanı sıra birçok erken ( titanyum , zirkonyum ) ve geç ( demir , bakır , çinko ) d-blok metallerine dayanmaktadır. Metal atomu , substratta oksijen (hem sp 2 hem de sp 3 ), nitrojen , kükürt ve halojenler gibi elektronegatif atom taşıyan yalnız çiftli bir eklenti oluşturur . Kompleksleşme kısmi yük transfer karakterine sahiptir ve substratı nükleofilik saldırıya, heterolitik bağ bölünmesine veya 1,3-dienler ve 1,3-dipollerle siklo eklemeye doğru aktive ederek, yalnız çift donörü etkin bir şekilde daha elektronegatif hale getirir.
Karbon-karbon veya karbon-heteroatom bağı oluşumunu içeren birçok klasik reaksiyon, Lewis asitleri tarafından katalize edilebilir. Örnekler arasında Friedel-Crafts reaksiyonu , aldol reaksiyonu ve Diels-Alder reaksiyonu ve ene reaksiyonu gibi oda sıcaklığında yavaş ilerleyen çeşitli perisiklik işlemler yer alır . Reaksiyonları hızlandırmanın yanı sıra, Lewis asit katalizörleri birçok durumda bölge seçicilik ve stereo seçicilik uygulayabilir.
Lewis asit reaktiflerindeki erken gelişmeler, TiCl 4 , BF 3 , SnCl 4 ve AlCl 3 gibi kolayca bulunabilen bileşiklere odaklandı . Yıllar geçtikçe, belirli uygulamalar için tasarlanmış ligandları taşıyan çok yönlü katalizörler, Lewis asidi katalizli reaksiyonların hem reaktivitesinde hem de seçiciliğinde gelişmeyi kolaylaştırmıştır. Daha yakın zamanlarda, kiral ligandlara sahip Lewis asit katalizörleri, asimetrik kataliz için önemli bir araç sınıfı haline geldi .
Lewis asit katalizinin geliştirilmesindeki zorluklar, verimsiz katalizör devrini (ürüne yönelik katalizör afinitesinden kaynaklanan) ve genellikle yardımcı grupların kullanımını gerektiren stereoselektivite için iki noktalı bağlanmanın sık sık gerekliliğini içerir.
mekanizma
Polar mekanizmalı reaksiyonlarda, Lewis asit katalizi genellikle katalizörün Lewis bazik heteroatomlarına bağlanmasını ve elektron yoğunluğunun geri çekilmesini içerir, bu da sırayla heterolitik bağ bölünmesini kolaylaştırır ( Friedel-Crafts reaksiyonu durumunda ) veya substratı doğrudan nükleofilik saldırıya doğru aktive eder ( karbonil ekleme reaksiyonları durumunda ). İkilik Lewis asidi-teşvik asetal ikame reaksiyonlar durumunda olduğu gibi, bazı reaksiyonlarda önemli sonuçlara yol açabilir S , N 1 ve S , N 2 Aşağıda gösterilen mekanizma farklı stereo-kimyasal sonuçlar verebilir. Bisiklik bir sistemde ürün oranını inceleyen Danimarka ve meslektaşları , Lewis asidinin diş yapısına ve R' grubunun kimliğine bağlı olarak her iki mekanizmanın da çalışabileceğini gösterdi .

Olarak Diels-Alder ve 1,3-dipolar siklo reaksiyonları Lewis alt asitleri LUMO dien veya dipol doğru daha reaktif hale sırasıyla dienophile veya dipolarphile enerjisini.
Karbonil içeren substratlarla Lewis asit katalizi
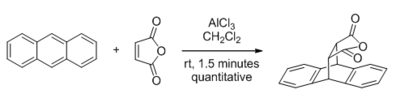
Lewis asitleri tarafından katalize edilebilen reaksiyon türleri arasında, karbonil içeren substratlara sahip olanlar en fazla dikkati çekmiştir. Yates Eaton anlamlı hızlanmasını rapor bu alandaki ilk büyük buluş, 1960 yılında Diels-Alder reaksiyonu ALCL ile 3 olduğunda maleik anhidrit dienophile olup.
Sınır yörünge analizine dayanan erken teorik çalışmalar, Lewis asit katalizinin dienofilin LUMO enerjisinin düşürülmesi yoluyla çalıştığını ortaya koydu. Ancak son çalışmalar, Lewis asit katalizli Diels-Alder reaksiyonlarının arkasındaki bu mantığın yanlış olduğunu göstermiştir. Lewis asitlerinin, dienofilin LUMO'sunun enerjisini düşürerek ve sonuç olarak normal elektron talebi orbital etkileşimini artırarak değil, etkileşen dien ve dienofil arasındaki kararsızlaştırıcı sterik Pauli itmesini azaltarak Diels-Alder reaksiyonunu hızlandırdığı bulunmuştur. Lewis asidi, bir donör-alıcı etkileşimi yoluyla dienofile bağlanır ve bu mekanizma aracılığıyla, işgal edilen yörünge yoğunluğunu dienofilin reaktif C=C çift bağından Lewis asidine doğru polarize eder. Dienofilin C=C çift bağı üzerindeki bu azaltılmış işgal edilmiş yörünge yoğunluğu, sırayla, gelen dien ile daha az itici bir kapalı-kabuk-kapalı-kabuk yörünge etkileşimine girecek, kararsızlaştırıcı sterik Pauli itmesini azaltacak ve dolayısıyla Diels- Kızılağaç reaksiyon bariyeri. Ek olarak, Lewis asidi katalizörü ayrıca Diels-Alder reaksiyonunun eşzamansızlığını arttırır ve dienofilin C=C çift bağı üzerinde bulunan işgal edilmiş π-orbitalini asimetrik hale getirir. Sonuç olarak, bu arttırılmış asenkronisite, kararsızlaştırıcı sterik Pauli itmesinde ekstra bir azalmaya ve ayrıca tepkenler üzerinde deforme olması için azalan bir baskıya yol açar, başka bir deyişle, kararsızlaştırıcı aktivasyon gerilimini (ayrıca bozulma enerjisi olarak da bilinir) azaltır. Bu çalışan katalitik mekanizma, çeşitli organik reaksiyonlarda etkili olan Pauli-düşürücü kataliz olarak bilinir .
Lewis asidi katalizli Diels-Alder reaksiyonlarının arkasındaki orijinal mantık yanlıştır, çünkü dienofilin LUMO'sunun enerjisini düşürmenin yanı sıra, Lewis asidi dienofilin HOMO'sunun enerjisini de düşürür ve dolayısıyla ters elektron talebini arttırır LUMO-HOMO yörünge enerjisi açıklık. Bu nedenle, gerçekten Lewis asit katalizörleri, dienofilin LUMO'sunu düşürerek normal elektron talebi orbital etkileşimini güçlendirir, ancak aynı zamanda dienofilin HOMO'sunun enerjisini de düşürerek ters elektron talebi orbital etkileşimini zayıflatır. Bu iki karşıt olay birbirini etkili bir şekilde iptal ederek, karşılık gelen katalize edilmemiş Diels-Alder reaksiyonları ile karşılaştırıldığında neredeyse değişmeyen yörünge etkileşimleri ile sonuçlanır ve bunu Lewis asidi katalizli Diels-Alder reaksiyonlarının arkasındaki aktif mekanizma yapmaz.
Hız hızlandırmaya ek olarak, Lewis asit katalizli reaksiyonlar bazen stereoindüksiyon modellerinin gelişimini uyaran gelişmiş stereoselektivite sergiler. Modellerin kökleri, teorik hesaplamalar , NMR spektroskopisi ve X-ışını kristalografisinde onlarca yıl süren araştırmalar yoluyla , 1990'ların başında oldukça sağlam bir şekilde kurulmuş olan Lewis asit-karbonil komplekslerinin yapılarının bilgisine sahiptir :
- σ-Karmaşıklaştırma: Lewis asidinin karbonil bileşiği ile yalnız oksijen çifti ile bir σ-bağ yoluyla etkileşime girdiği kompleks hem termodinamik olarak tercih edilir hem de katalitik olarak uygundur. Aldehitler ve ketonların birkaç geçiş metali kompleksi kristalografik olarak karakterize edilmiştir.
- Bükülmüş geometrisi: Metal-oksijen-karbon bağı açısı, 180 ° 'den, ve metal bir syn bir tarafından etkilenmediği sürece, daha küçük bir ikame edici için kenetleme daha büyük bir ikame edici ile bir grup.
- α,β-doymamış bileşikler için bir s-trans tercihi.
Karbonil bileşiklerine ekleme ve konjuge ekleme
Mukaiyama Aldol reaksiyonu ve Sakurai, reaksiyon ilave bakınız silil enol eterleri , sırasıyla, ve allylsilanes karbonil bileşiklerdir. Sadece Lewis asit katalizi altında bu reaksiyonlar sentetik olarak faydalı koşullar altında meydana gelir. Asiklik geçiş durumlarının 1,2- veya 1,4- ilavesi için her iki reaksiyonda da çalıştığına inanılır ve sterik faktörler stereoseçiciliği kontrol eder. Bu, lityum, bor ve titanyum enolatları ile aldol reaksiyonu için yaygın olarak kabul edilen katı Zimmerman-Traxler döngüsel geçiş durumu ile çelişmektedir . Sonuç olarak, silil enol eter veya alilsilan içindeki çift bağ geometrisi, ürün stereokimyasına iyi bir şekilde dönüşmez. Kumada tarafından önerilen Sakurai 1,2-eklemesi için bir model aşağıdaki şemada sunulmaktadır; syn- zaman diastereomeri baskın olan (E) silan kullanılır ve ne de biraz tercih edilir : (Z) silan kullanılır. Heathcock tarafından yapılan benzer bir analiz, basit substratlarla, moleküller arası Mukaiyama aldol reaksiyonu için esasen hiçbir diastereoseçicilik olmadığı gerçeğini açıklar.
Lewis asidi katalizörü, aldehit metal merkezi üzerinde şelat oluşturabildiğinde ve katı bir döngüsel ara ürün oluşturduğunda stereoselektivitede rol oynar . Stereokimyasal ürünü yaklaşımıyla sonra tutarlıdır nükleofil anti- halkası üzerinde daha çok kütleli ikameye.
Diels-Alder reaksiyonu
ZnCl 2 , BF 3 , SnCl 4 , AlCl 3 ve MeAlCl 2 gibi Lewis asitleri hem normal hem de ters elektron talepli Diels-Alder reaksiyonlarını katalize edebilir . Hızdaki artış genellikle çarpıcıdır ve izopren ve metil akrilat arasındaki reaksiyonda gösterildiği gibi, orto veya para benzeri ürünlere yönelik bölgesel seçicilik genellikle iyileştirilir .
Katalizlenen Diels-Alder reaksiyonunun uyumlu olduğuna inanılıyor . B3LYP / 6-31G (d) düzeyinde bir hesaplama çalışmada Ancak göstermiştir geçiş durum BF 3 propenal ve 1,3-bütadienden arasındaki Diels-Alder reaksiyonu termal reaksiyon daha fazla uyumsuz olan -katalize - karbonil grubundan daha uzak olan bağ, diğer bağın önünde oluşturulur.
Ene reaksiyonu
Karbonil-ene tepkimesiyle hemen hemen her zaman Lewis ile katalize edilmektedir, sentetik uygulamalarda asitleri. Kinetik izotop etkisi çalışmalarına dayanan katalize reaksiyon için kademeli veya büyük ölçüde asenkron bir mekanizma önerilmiştir . Bununla birlikte, diastereoseçiciliği yorumlamak için sıklıkla döngüsel geçiş durumları çağrılır. 1990'ların başındaki ufuk açıcı bir derlemede, Mikami ve meslektaşları, diastereoseçicilikte sterik kütlenin rolü de dahil olmak üzere, gözlemlenen birçok stereokimyasal sonucu rasyonalize edebilen geç, sandalye benzeri bir geçiş durumu önerdiler:
Ancak daha yakın zamanlarda, aynı grup kalay veya alüminyum Lewis asidi katalizli en reaksiyonları üzerinde HF/6-31G* hesaplamaları yaptı. Bu metil gloxylate gerekçe şelatlar kalay Lewis asitlerini ancak alüminyum olanlar, bu erken bir çağrılan geçiş zarf benzeri durum arasında en reaksiyonunun farklı stereokimyasal sonucu rasyonel (E) -2-büten ve metil glioksilat elde edilmiştir.
Sentezde uygulama
Lewis asidi katalizli karbonil ilave reaksiyonları, doğal ürün sentezinde karbon-karbon bağları oluşturmak için rutin olarak kullanılır . Aşağıda gösterilen ilk iki reaksiyon, Sakurai ve Mukaiyama reaksiyonlarının doğrudan uygulamaları olan sırasıyla (+)-likofleksin ve zaragozik asit C'nin sentezlerindendir. (+)-fawcettimine yolundaki üçüncü reaksiyon, bir Mukaiyama- Michael reaksiyonuna benzer bir Lewis-asit katalizli siklopropan açıklığıdır .
Lewis asitleri tarafından katalize edilen veya desteklenen Diels-Alder reaksiyonu , stereokimyasal kontrol ile tek bir adımda yapı iskelesi karmaşıklığını elde etmek için doğal ürün sentezinde güçlü ve yaygın olarak kullanılan bir yöntemdir . Aşağıda gösterilen iki reaksiyon, sırasıyla (-)-fusarisetin A'ya karşı bir molekül içi Diels-Alder reaksiyonu ve (-)-epibatidine karşı moleküller arası bir hetero-Diels-Alder reaksiyonudur.
Olarak , Friedel-Crafts alkilasyon, bir Lewis asidi - genellikle basit bir metal halojenür tuzu - bir alkil halojenür bir karbon-halojen bağı heterolitik bölünmesini teşvik eder ve bir oluşturur karbokatyonu maruz, elektrofilik aromatik ikame . Sentezde büyük ölçüde faydalı olmasına rağmen, reaksiyon genellikle karbokasyon yeniden düzenlenmesi, alkil göçü ve aşırı alkilasyondan kaynaklanan yan reaksiyonlardan muzdariptir . Benzer şekilde, Friedel-Crafts asilasyonunda, bir Lewis asidi, bir asit klorürden (veya bazen asit anhidritten) bir asilyum iyonunun üretilmesine yardımcı olur. Açilyum iyonunun genellikle aktif ara madde olduğu varsayılmasına rağmen, protonlanmış açilyum dikasyonunun, sonraki elektrofilik aromatik ikameye maruz kalan aktif elektrofil olduğuna dair kanıtlar vardır.
Friedel-Crafts reaksiyonunun önemli varyantları arasında klorometilasyon (formaldehit ve HCl ile), formilasyon (HCl ve CO veya CN - ile ) ve asil kaynağı olarak bir nitril ile asilasyon yer alır . Nitril bazlı asilasyon, amin grubunu korumadan anilinin doğrudan orto-asilasyonuna izin verdiği için özellikle yararlıdır . Reaksiyonun aşağıda gösterilen mekanizma yoluyla ilerlemesi için zayıf ve güçlü bir Lewis asidinin bir kombinasyonu gereklidir. Bu mekanizma tarafından yönlendirilen ve galyum trihalojenürlerin en güçlü Lewis asitleri arasında olduğu bilgisi ile donatılmış Merck'teki proses kimyagerleri, bir ilaç adayına yönelik bu durum için oldukça verimli koşullar geliştirebildiler.
Asimetrik Lewis asit katalizi
Ortak Kiral Ligandlar
Lewis asitleri tarafından asimetrik kataliz , metal merkezine koordine edilmiş kiral ligandlara sahip katalizörlere dayanır . Yıllar boyunca, az sayıda kiral ligand yapı iskelesi, genellikle ilgisiz mekanizmalardan oluşan geniş bir uygulama yelpazesi için uygun "ayrıcalıklı" katalitik özelliklere sahip olarak öne çıkmıştır. Asimetrik Lewis asit katalizindeki mevcut araştırma çabaları, de novo yeni yapı iskeleleri oluşturmaktan ziyade çoğunlukla bu ligandları kullanır veya değiştirir . "Ayrıcalıklı" yapı iskeleleri, kimyasal stabilite ve göreceli olarak detaylandırma kolaylığı da dahil olmak üzere birkaç ortak özelliği paylaşır. İskelelerin çoğunluğu çok dişlidir . Bunların çoğu ayrıca ligand içinde yüksek iskele sertliğine sahiptir. Birçoğunun oldukça olgun stereoindüksiyon modelleri mevcuttur. Jacobsen ve Zhou tarafından tanımlanan bazı "ayrıcalıklı" yapı iskeleleri aşağıda tanıtılmaktadır.
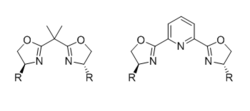
Bisoksazolinler (KUTU)
En yaygın kiral bisoksazolin (BOX) ligandları , bir bağlayıcı ile birleştirilen 4-pozisyonlarında hacimli bir grup tarafından ikame edilen iki özdeş kiral oksazolin kısmından oluşur. Bağlayıcı tek bir karbon birimi olduğunda ligand iki dişlidir, ancak bağlayıcı PyBOX ligandları durumunda bir piridin azotu gibi ek bir koordine edici atom taşıdığında üç dişlidir (genellikle meridyen). Ligand diş yapısının ve aktif ara geometrinin stereokimyasal sonuç üzerindeki etkisi kapsamlı bir şekilde gözden geçirilmiştir.
Birçok iki dişli BOX bazlı Lewis asidi katalizli reaksiyon, iki noktalı bağlanma için uygun substratlara sahip bakır(II) katalizörlerine dayanır. Stereokimyasal sonuç, ilgili kristal yapılara dayalı olarak önerilen bir bükülü kare düzlemsel ara madde ile tutarlıdır . Oksazolinin 4-pozisyonundaki ikame edici, substratın bir enantiotopik yüzünü bloke ederek enantioseçiciliğe yol açar. Bu, aşağıdaki aldol tipi reaksiyonda gösterilmiştir, ancak Mannich tipi reaksiyonlar, ene reaksiyonu , Michael ilavesi , Nazarov siklizasyonu ve hetero -Diels-Alder reaksiyonu gibi çok çeşitli reaksiyonlara uygulanabilir .
Öte yandan, meridyonel olarak üç dişli PyBOX ligandını taşıyan bir Lewis asidi üzerinde iki noktalı bağlanma, bir kare piramidal kompleks ile sonuçlanacaktır . Elektrofil olarak benziloksiasetaldehit kullanan bir çalışma , stereokimyasal sonucun ekvatoral olarak karbonil oksijen bağlanması ve eksenel olarak eter oksijen bağlanması ile tutarlı olduğunu göstermiştir.
BİNAP
Noyori tarafından geliştirilen BINAP (2,2'-difenilfosfino-1,1'-binaftil), bir binaftalen omurgasına yerleştirilmiş iki triarilfosfin parçasına sahip bir kiral difosfin ligandları ailesidir . Bir metal (genellikle geç geçiş metali) üzerine BINAP şelatlar oluşturmak üzere Cı 2 -Simetrik kompleksi. Aşağıda bir (R) -BINAP rutenyum kompleksinin yapısında gösterildiği gibi , bir oktahedral metal merkezde kalan dört koordinasyon bölgesi arasında , iki ekvator bölgesi (mor) ekvator fenil gruplarından güçlü bir şekilde etkilenirken, iki eksenel bölge ( yeşil) eksenel fenil gruplarından etkilenir.
Yapıya dayalı olarak, birçok BINAP bazlı Lewis asidi katalizli reaksiyonda gözlemlenen enantioselektiflik için modeller önerilmiştir. Örneğin, aşağıda gösterilen paladyum katalizli enantioselektif Diels-Alder reaksiyonunda, dienofilin ekvator bölgelerindeki metal merkezi koordine ettiği düşünülmektedir. Böylece fosfor üzerindeki ekvatoral fenil grubu Si- yüzünü tıkayarak mükemmel enantioseçicilik ile sonuçlanır. Nikel katalizli bir asimetrik enolat alkilasyon reaksiyonunun sonucunu rasyonalize etmek için çok benzer bir model kullanıldı, burada substrat aynı zamanda metal üzerinde şelat oluşturmasına izin veren bir yardımcı madde de içeriyor . Öte yandan, bakır(I) katalizli bir heteroen reaksiyonunun, metal merkezini değiştirerek alternatif bir stereoindüksiyon modu sunan bir tetrahedral ara madde boyunca ilerlediği düşünülmektedir .
BİNOL
BINOL (1,1'-binaftil-2,2'-diol) genellikle alüminyum, titanyum, zirkonyum ve çeşitli nadir toprak metalleri gibi oksofilik Lewis asidik metalleri ile birlikte kullanılır. BINOL'ün kendisinin ideal enantioselektif kontrol sağlamadığı durumlarda, 3,3' pozisyonlarında ( lithiation yoluyla ) ve 6,6' pozisyonlarında ( elektrofilik aromatik tarafından hazırlanan 6,6'-dibromür bileşiği aracılığıyla) ikame ile kolaylıkla detaylandırılabilir. ikame ) sterik yığın ve elektronik özellikleri modüle etmek için. Örneğin, hacimli 3,3'-disilil ikameli BINOL'e dayalı alüminyum katalizörler, katalitik asimetrik hetero -Diels-Alder reaksiyonunun ve Claisen yeniden düzenlemesinin erken örnekleri olarak geliştirilmiştir , 6,6'-pozisyonlarında elektron çeken grupların eklenmesiyle birlikte geliştirilmiştir. zirkonyum(IV) katalizörlerinin Lewis asitliğini ve dolayısıyla katalitik aktivitesini Mannich tipi bir reaksiyona doğru arttırmak için çok önemliydi . Ancak bugüne kadar, BINOL-yönelimli stereoindüksiyonu yöneten önemli faktörler için hiçbir model genel olarak kabul edilmemiştir.
TADDOL
TADDOL , tetraaril-1,3-dioksolan-4,5-dimetanol anlamına gelir. Titanyum TADDOLate katalizörlerinin karbonil ilavelerine ve siklo ilavelerine yönelik geniş uygulaması, Seebach ve çalışma arkadaşları tarafından tanıtıldı ve çok çeşitli reaksiyonlarda gözlemlenen seçicilikle uyumlu çalışan bir stereoindüksiyon modelinin ortaya konduğu yeni ufuk açıcı bir incelemede kapsamlı bir şekilde özetlendi. mekanizmanın net bir resmi olmamasına rağmen.
Uygulamalar
Birçok doğal ürünün sentezi için asimetri belirleme adımında Lewis asit katalizi kullanılmıştır . Aşağıda taksan iskeletinin sentezinden gösterilen ilk reaksiyon, bir konjugat karbonil ilave reaksiyonu için bir kiral fosforamidit ligandı tarafından desteklenen bakır bazlı bir katalizör kullanır . Ent - hyperforin sentezinden ikinci reaksiyon, asimetrik bir Diels-Alder reaksiyonu için bir demir-PyBOX katalizörü kullanır .