hidrojen halojenür - Hydrogen halide
Hidrojen halojenürler ( sulu fazdayken hidrohalik asitler ), Arrhenius asitleri olarak işlev gören iki atomlu , inorganik bileşiklerdir . Formül H X olup X'in biri halojen : flor , klor , brom , iyot ya da astatin . Bilinen tüm hidrojen halojenürler, Standart Sıcaklık ve Basınçta gazlardır .
| bileşik | Kimyasal formül | Bağ uzunluğu d (H−X) / pm (gaz fazı) |
model | dipol μ / D |
Sulu faz (asit) | Sulu faz p K bir değerler |
|---|---|---|---|---|---|---|
|
hidrojen florür (floran) |
HF | 1.86 | hidroflorik asit | 3.1 | ||
|
hidrojen klorür (kloran) |
HCl |  |
 |
1.11 | hidroklorik asit | -3.9 |
|
hidrojen bromür (broman) |
HBr |  |
 |
0.788 | hidrobromik asit | -5.8 |
|
hidrojen iyodür (iyodan) |
SELAM |  |
 |
0,382 | hidroiyodik asit | -10,4 |
|
hidrojen astatid astatin hidrit (astatan) |
Şapka |  |
 |
-0,06 | hidroastatik asit | ? |
|
hidrojen tennessid tennessin hidrit (tennessane) |
HT'ler | (tahmini 197 pm) | -0.24 ? | hidrotennessik asit | ? |
Vs. hidrohalik asitler
Hidrojen halojenürler, gaz fazında iyonlaşma eğilimi olmayan iki atomlu moleküllerdir (sıvılaştırılmış hidrojen florür suya biraz benzer bir polar çözücü olmasına rağmen). Böylece kimyagerler, hidrojen klorürü hidroklorik asitten ayırır. Birincisi, asit vermek için su ile reaksiyona giren oda sıcaklığında bir gazdır. Asit oluştuktan sonra, iki atomlu molekül ancak zorlukla yeniden üretilebilir, ancak normal damıtma ile değil . Genellikle asit ve moleküllerin adları, laboratuvar jargonunda "HCl", gaz halindeki hidrojen klorür değil, genellikle hidroklorik asit anlamına gelecek şekilde açıkça ayırt edilmez.
oluşum
Hidroklorik asit formundaki hidrojen klorür, mide asidinin önemli bir bileşenidir .
Hidrojen florür, klorür ve bromür de volkanik gazlardır .
sentez
Hidrojenin flor ve klor ile doğrudan reaksiyonu, sırasıyla hidrojen florür ve hidrojen klorür verir. Ancak endüstriyel olarak bu gazlar, halojenür tuzlarının sülfürik asit ile işlenmesiyle üretilir. Hidrojen bromür, hidrojen ve brom, bir platin katalizör varlığında yüksek sıcaklıklarda birleştirildiğinde ortaya çıkar . En az kararlı hidrojen halojenür, HI, iyodin hidrojen sülfit veya hidrazin ile reaksiyonuyla daha az doğrudan üretilir .
Fiziki ozellikleri
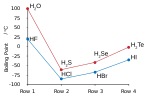
Hidrojen halojenürler , 19 °C'de kaynayan hidrojen florür hariç , standart sıcaklık ve basınç koşullarında (STP) renksiz gazlardır . Hidrojen halojenürlerin tek başına hidrojen florür , moleküller arasında hidrojen bağı sergiler ve bu nedenle HX serisinin en yüksek erime ve kaynama noktalarına sahiptir. HCl'den HI'ya kaynama noktası yükselir. Bu eğilim, moleküllerdeki elektron sayılarıyla bağıntılı olan, moleküller arası van der Waals kuvvetlerinin artan gücüne atfedilir . Konsantre hidrohalik asit çözeltileri görünür beyaz dumanlar üretir. Bu sis, hidrohalik asidin konsantre sulu çözeltilerinin küçük damlacıklarının oluşumundan kaynaklanır.
Reaksiyonlar
Yüksek derecede ekzotermik olan suda çözündükten sonra, hidrojen halojenürler karşılık gelen asitleri verir. Bu asitler çok güçlüdür ve sulu çözeltide hidronyum iyonları (H 3 O + ) vererek iyonlaşma eğilimlerini yansıtır . Hidroflorik asit hariç, hidrojen halojenürler güçlü asitlerdir ve asit kuvveti grupta aşağı doğru artar. Hidroflorik asit karmaşıktır çünkü gücü homokonjugasyonun etkileri nedeniyle konsantrasyona bağlıdır . Asetonitril gibi sulu olmayan çözücülerdeki çözeltiler olarak , hidrojen halojenürler ancak biraz asidiktir.
Benzer şekilde, hidrojen halojenürler amonyak (ve diğer bazlar) ile reaksiyona girerek amonyum halojenürler oluşturur:
- HX + NH 3 → NH 4 x
Organik kimyada, halokarbonları hazırlamak için hidrohalojenasyon reaksiyonu kullanılır. Örneğin, kloroetan ile üretilir hidroklorinasyonu arasında etilen :
- Cı 2 H 4 + HCI → CH 3 CH 2 CI
Ayrıca bakınız
- psödohalojen
- hipohalöz asit
- grup 13 hidritler
- grup 14 hidritler
- 15. grup hidritler
- grup 16 hidritler
