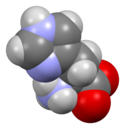
Histidin - Histidine
 |
|||
|
|
|||
| İsimler | |||
|---|---|---|---|
|
IUPAC adı
histidin
|
|||
| Diğer isimler
2-Amino-3-( 1H -imidazol-4-il)propanoik asit
|
|||
| tanımlayıcılar | |||
|
3B model ( JSmol )
|
|||
| chebi | |||
| CHEMBL | |||
| Kimyasal Örümcek | |||
| İlaç Bankası | |||
| ECHA Bilgi Kartı |
100.000.678 |
||
| fıçı | |||
|
PubChem Müşteri Kimliği
|
|||
| ÜNİİ | |||
|
CompTox Panosu ( EPA )
|
|||
|
|||
|
|||
| Özellikler | |||
| C 6 H 9 N 3 O 2 | |||
| Molar kütle | 155.157 g·mol -1 | ||
| 4,19g/100g @ 25 °C | |||
| Tehlikeler | |||
| Güvenlik Bilgi Formu | Bakınız: veri sayfası | ||
| NFPA 704 (ateş elması) | |||
| Ek veri sayfası | |||
|
Kırılma indisi ( n ), Dielektrik sabiti (ε r ), vb. |
|||
|
termodinamik
veriler |
Faz davranışı katı-sıvı-gaz |
||
| UV , IR , NMR , MS | |||
|
Aksi belirtilmediği sürece, veriler standart durumdaki malzemeler için verilmiştir (25 °C [77 °F], 100 kPa'da). |
|||
|
|
|||
| Bilgi kutusu referansları | |||
Histidin (sembol His veya H ), proteinlerin biyosentezinde kullanılan bir a-amino asittir . Bir içeren α-amino grubunun (olup protonlanmış -NH 3 + altında şeklinde biyolojik koşullar ), bir karboksilik asit (protonu giderilmiş -COO olan grup - ve bir biyolojik şartlar altında formu) imidazol olan (yan zincire kısmen protonlanmış), fizyolojik pH'da pozitif yüklü bir amino asit olarak sınıflandırılır . Başlangıçta sadece bebekler için gerekli olduğu düşünülen , şimdi daha uzun süreli çalışmalarda yetişkinler için de gerekli olduğu gösterilmiştir. Bu edilir kodlanmış tarafından kodonları CAU ve CAC.
Histidin ilk olarak 1896'da Alman doktor Albrecht Kossel ve Sven Gustaf Hedin tarafından izole edildi . Aynı zamanda bağışıklık tepkilerinde hayati bir inflamatuar ajan olan histaminin öncüsüdür . Asil radikali olup histidil .
İmidazol yan zincirinin özellikleri
Konjugat asidi (protonlanmış formu) imidazol yan zinciri histidin bir sahiptir p K bir yaklaşık 6.0. Bu nedenle, pH 6'nın altında, imidazol halkası çoğunlukla protonlanır ( Henderson-Hasselbalch denkleminde tanımlandığı gibi ). Ortaya çıkan imidazolyum halkası iki NH bağı taşır ve pozitif bir yüke sahiptir. Pozitif yük, her iki nitrojen arasında eşit olarak dağıtılır ve eşit derecede önemli iki rezonans yapısı ile temsil edilebilir . pH 6'nın üzerinde, iki protondan biri kaybolur. İmidazol halkasının kalan protonu, nitrojen üzerinde bulunabilir ve N1-H veya N3-H tautomerleri olarak bilinenlere yol açar . Yukarıdaki şekilde gösterilen N3-H tautomer, amino ve karboksil gruplarını taşıyan amino asit omurgasından uzakta #3 nitrojen üzerinde protonlanırken, N1-H totomer omurgaya yakın nitrojen üzerinde protonlanır. Histidinin imidazol/imidazolyum halkası tüm pH değerlerinde aromatiktir .
İmidazol yan zincirinin asit-baz özellikleri , birçok enzimin katalitik mekanizması ile ilgilidir . İçinde katalitik üçlü , histidin bazik azot bir proton özetleri serin , treonin , ya da sistein bir şekilde etkin hale getirmek için bir nükleofil . Bir histidin proton mekiğinde , histidin, protonları hızlı bir şekilde mekik etmek için kullanılır. Bunu, pozitif yüklü bir ara madde yapmak için bazik nitrojeni ile bir protonu soyutlayarak ve daha sonra asidik nitrojeninden protonu çıkarmak için başka bir molekülü, bir tamponu kullanarak yapabilir. İçinde karbonik anhidraz , bir histidin proton Servisi uzak bir hızla Servisi protonlar için kullanılır , çinko hızlı enzim aktif şeklini yeniden oluşturmak için TT-bağlı bir su molekülü. Hemoglobinin E ve F helislerinde histidin, karbon monoksitin yanı sıra dioksijen bağlanmasını da etkiler . Bu etkileşim, Fe(II)'nin O2 için afinitesini arttırır, ancak serbest hemde 20.000 kat daha güçlü olana kıyasla, hemoglobinde sadece 200 kat daha güçlü bağlanan CO'nun bağlanmasını destabilize eder .
İmidazol yan zincirinin tatomerizmi ve asit-baz özellikleri, 15 N NMR spektroskopisi ile karakterize edilmiştir . İki 15 N kimyasal kayma benzerdir ( sigma ölçeğinde nitrik aside göre yaklaşık 200 ppm, artan koruma, artan kimyasal kaymaya karşılık gelir ). NMR spektral ölçümleri, N1-H'nin kimyasal kaymasının hafifçe düştüğünü, buna karşın N3-H'nin kimyasal kaymasının önemli ölçüde düştüğünü gösterir (yaklaşık 190'a karşı 145 ppm). Bu değişiklik, muhtemelen komşu amonyuma hidrojen bağı nedeniyle N1-H tautomerinin tercih edildiğini gösterir . N3'teki koruma , aromatik halkanın azot yalnız çifti ile uyarılmış π* durumları arasında simetriye izin verilen bir etkileşimi içeren ikinci dereceden paramanyetik etki nedeniyle büyük ölçüde azalır . pH > 9'da, N1 ve N3'ün kimyasal kaymaları yaklaşık 185 ve 170 ppm'dir.
ligand

Histidin , birçok metal iyonu ile kompleksler oluşturur . Histidin artığının imidazol yan zincir yaygın olarak hizmet ligand olarak metalloprotein . Bir örnek, miyoglobin ve hemoglobinde Fe'ye bağlı eksenel tabandır. Poli-histidin etiketleri (altı veya daha fazla ardışık H kalıntısından oluşan), mikromolar afinite ile nikel veya kobaltlı kolonlara bağlanarak protein saflaştırması için kullanılır. Engerek Atheris squamigera'nın zehirinde bulunan doğal poli-histidin peptitlerinin Zn(2+), Ni(2+) ve Cu(2+)'yı bağladığı ve zehir metalloproteazlarının işlevini etkilediği gösterilmiştir. Ayrıca, metal bağlayıcı ve özellikle nikel-kobalt bağlayıcı proteinlerde histidin açısından zengin düşük karmaşıklık bölgeleri bulunur.
Metabolizma
biyosentez
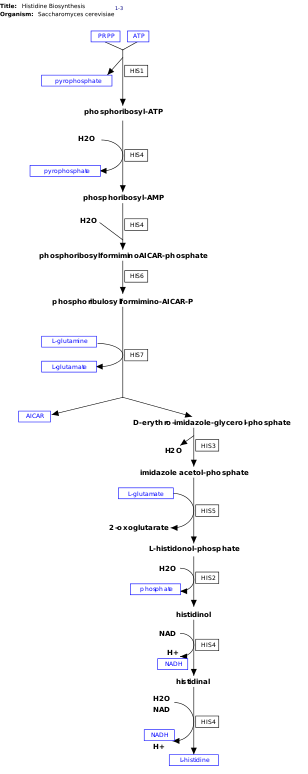
l- Histidin, insanlarda de novo sentezlenmeyen esansiyel bir amino asittir . İnsanlar ve diğer hayvanlar, histidin veya histidin içeren proteinleri yutmalıdır. Histidinin biyosentezi, E. coli gibi prokaryotlarda geniş çapta çalışılmıştır . E. coli'de histidin sentezi sekiz gen ürünü (His1, 2, 3, 4, 5, 6, 7 ve 8) içerir ve on adımda gerçekleşir. Bu mümkündür çünkü tek bir gen ürünü birden fazla reaksiyonu katalize etme yeteneğine sahiptir. Örneğin, yolda gösterildiği gibi, His4 yoldaki 4 farklı adımı katalize eder.
Histidin sentezlenir fosforibosil pirofosfat yapılır (PRPP), riboz-5-fosfat ile riboz-fosfat diphosphokinase içinde pentoz fosfat yolu . Histidin biyosentezinin ilk reaksiyonu, PRPP ve adenozin trifosfatın (ATP) ATP-fosforibosil transferaz enzimi tarafından yoğunlaştırılmasıdır . ATP-fosforibosil transferaz, görüntüde His1 ile gösterilir. His4 gen ürünü daha sonra, geri dönüşü olmayan bir adım olan fosforibosil-AMP (PRAMP) üreten yoğunlaştırma ürünü olan fosforibosil-ATP'yi hidrolize eder. His4 daha sonra His6 gen ürünü tarafından fosforibulosilformimino-AICAR-P'ye dönüştürülen fosforibosilformiminoAICAR-fosfat oluşumunu katalize eder. His7, d -eritro -imidazol-gliserol-fosfat oluşturmak için fosforibulosilformimino-AICAR-P'yi böler . Daha sonra His3, imidazol asetol-fosfat salan su oluşturur. His5 daha sonra l -histidinol-fosfat yapar ve bu daha sonra His2 tarafından histidinol yaparak hidrolize edilir . His4 , bir amino aldehit olan l- histidinal oluşturmak için l- histidinolün oksidasyonunu katalize eder . Son aşamada, l -histidinal isimli dönüştürülür l -histidin.
Tıpkı hayvanlar ve mikroorganizmalar gibi bitkiler de büyümeleri ve gelişmeleri için histidine ihtiyaç duyarlar. Mikroorganizmalar ve bitkiler, histidin sentezleyebilmeleri bakımından benzerdir. Her ikisi de histidini biyokimyasal ara madde fosforibosil pirofosfattan sentezler. Genel olarak, histidin biyosentezi bitkilerde ve mikroorganizmalarda çok benzerdir.
Biyosentezin düzenlenmesi
Bu yolun oluşması için enerji gerekir, bu nedenle ATP'nin varlığı yolun ilk enzimi olan ATP-fosforibosil transferazı (sağdaki resimde His1 olarak gösterilmiştir) aktive eder. ATP-fosforibosil transferaz, geri besleme inhibisyonu yoluyla düzenlenen, ürün olan histidin varlığında inhibe edildiği anlamına gelen hız belirleyici enzimdir.
bozulma
Histidin, trikarboksilik asit (TCA) döngüsünün ara ürünlerine dönüştürülebilen amino asitlerden biridir. Histidin, prolin ve arginin gibi diğer amino asitlerle birlikte, amino grubunun çıkarıldığı bir süreç olan deaminasyonda yer alır. Olarak prokaryotlar , histidin ilk histidase ile urocanate dönüştürülür. Daha sonra ürokanaz, ürokanatı 4-imidazolon-5-propionata dönüştürür. İmidazolonpropionaz , 4-imidazolon-5-propionattan formiminoglutamat (FIGLU) oluşturmak için reaksiyonu katalize eder . Formimino grubu tetrahidrofolata aktarılır ve kalan beş karbon glutamat oluşturur. Genel olarak, bu reaksiyonlar glutamat ve amonyak oluşumu ile sonuçlanır. Glutamat daha sonra glutamat dehidrojenaz ile deamine edilebilir veya α-ketoglutarat oluşturmak üzere transamine edilebilir.
Diğer biyolojik olarak aktif aminlere dönüşüm
- Histidin amino asidi, vücutta iltihaplanma için gerekli olan bir amin olan histamin için bir öncüdür .
- Histidin amonyak-liyaz enzimi , histidini amonyak ve ürokanik aside dönüştürür . Bu enzimin bir eksikliği nadir metabolik bozukluk mevcuttur histidinemia üreten urocanic asidürisi anahtar tanı bulgu olarak.
- Histidin, belirli metiltransferaz enzimleri tarafından iskelet kası hasarı için bir biyobelirteç görevi gören 3-metilhistidine dönüştürülebilir .
- Histidin ayrıca iskelet kasında bulunan bir dipeptit olan karnosin biyosentezi için bir öncüdür .
- Gelen Actinobacteria'lar ve bu gibi filamentli mantar, Neurospora crassa , histidin dönüştürülebilen antioksidan ergotiyonein .
Gereksinimler
ABD Tıp Enstitüsü'nün Gıda ve Beslenme Kurulu (FNB), 2002 yılında esansiyel amino asitler için Önerilen Diyet Ödeneklerini (RDA) belirledi . Histidin için, 19 yaş ve üstü yetişkinler için, 14 mg/kg vücut ağırlığı/gün.
Ayrıca bakınız
Referanslar
Dış bağlantılar