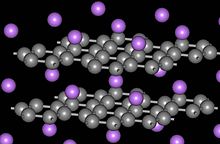
Grafit interkalasyon bileşiği - Graphite intercalation compound
Grafit interkalasyon bileşikleri ( GIC'ler ), Xn + veya Xn− iyonunun zıt yüklü karbon katmanları arasına eklendiği ( araya eklendiği ) CX m formülüne sahip karmaşık malzemelerdir . Tipik olarak m, 1'den çok daha azdır. Bu malzemeler, potansiyel uygulamaların bir dizi elektriksel ve redoks özelliklerini sergileyen derin renkli katılardır.
Hazırlık ve yapı
Bu malzemeler, grafitin güçlü bir oksitleyici veya güçlü bir indirgeyici madde ile işlenmesiyle hazırlanır:
- C + m X → CX m
Reaksiyon geri dönüşümlüdür.
Ev sahibi (grafit) ve misafir X, ücret transferi yoluyla etkileşime girer . Benzer bir süreç, ticari lityum iyon pillerin temelidir .
Bir grafit interkalasyon bileşiğinde, her katman mutlaka misafirler tarafından doldurulmaz. Sözde olarak aşama 1 bileşikleri , grafit katmanları ve ara katkılı tabakalar alternatif ve kademe 2 bileşikleri , bir birleştirilmiş tabaka ile alternatif arasında hiçbir konuk madde ile iki grafit katmanları. Gerçek bileşim değişebilir ve bu nedenle bu bileşikler, stokiyometrik olmayan bileşiklerin bir örneğidir . Kompozisyonun sahne ile birlikte belirtilmesi adettendir. Konuk iyonların katılmasıyla katmanlar birbirinden ayrılır.
Örnekler
Alkali ve alkali toprak türevleri

En iyi çalışılan grafit ara bileşiklerinden biri olan KC 8 , potasyumun grafit tozu üzerinde eritilmesiyle hazırlanır . Potasyum grafit tarafından emilir ve malzeme siyahtan bronza renk değiştirir. Elde edilen katı piroforiktir . Bileşim, potasyum-potasyum mesafesinin karbon çerçevesindeki altıgenler arasındaki mesafenin iki katı olduğu varsayılarak açıklanır. Anyonik grafit katmanları ile potasyum katyonları arasındaki bağ iyoniktir. Malzemenin elektriksel iletkenliği α-grafitten daha büyüktür. KC 8 , çok düşük kritik sıcaklık T c = 0.14 K olan bir süper iletkendir. KC 8'i ısıtmak , K atomları elimine edildiğinden bir dizi bozunma ürününün oluşmasına yol açar:
- 3 KC 8 → KC 24 + 2 K
KC 24 (mavi renkli), KC 36 , KC 48 ara ürünleri aracılığıyla , sonuçta KC 60 bileşiği elde edilir.
Stokiyometri MC 8 , M = K, Rb ve Cs için gözlenir. Daha küçük iyonlar M = Li + , Sr 2+ , Ba 2+ , Eu 2+ , Yb 3+ ve Ca 2+ için sınırlayıcı stokiyometri MC 6'dır . Kalsiyum grafit CaC
6yüksek oranda yönlendirilmiş pirolitik grafitin sıvı Li-Ca alaşımına 350 °C'de 10 gün daldırılmasıyla elde edilir . CaC'nin kristal yapısı
6R 3 m uzay grubuna aittir . Grafit ara katman mesafesi, Ca interkalasyonu üzerine 3.35'ten 4.524 A'ya yükselir ve karbon-karbon mesafesi 1.42'den 1.444 A'ya yükselir.
İle baryum ve amonyak , katyonları stokiyometri veren çözülmesiyle (Ba (NH 3 ) 2.5 ° C 10.9 (aşama 1)) veya bu , sezyum , hidrojen ve potasyum (CSC 8 mK 2 H 4/3 Cı 8 (aşama 1 )).
Diğer alkali metallerden farklı olarak Na interkalasyon miktarı çok azdır. Kuantum-mekanik hesaplamalar bunun oldukça genel bir fenomenden kaynaklandığını göstermektedir: alkali ve alkalin toprak metalleri arasında, periyodik tablonun aynı grubundaki diğer elementlerle karşılaştırıldığında, Na ve Mg genellikle belirli bir alt tabakaya en zayıf kimyasal bağlanmaya sahiptir. Bu fenomen, periyodik tablonun sütunlarında, iyonlaşma enerjisindeki eğilimler ile iyon-substrat eşleşmesi arasındaki rekabetten kaynaklanmaktadır. Bununla birlikte, iyonun birlikte-interkalasyon işlemi yoluyla bir çözücü kabuğuna sarıldığı durumlarda, grafite önemli ölçüde Na interkalasyonu meydana gelebilir. Karmaşık bir magnezyum(I) türü de grafit içine eklenmiştir.
Grafit bisülfat, perklorat, heksafloroarsenat: oksitlenmiş karbonlar
Ara bileşikler grafit bisülfat ve grafit perklorat, grafitin güçlü asitlerin varlığında güçlü oksitleyici maddelerle işlenmesiyle hazırlanabilir. Potasyum ve kalsiyum grafitlerin aksine, karbon katmanları bu süreçte oksitlenir: 48 C + 0.25 O 2 + 3 H 2 SO 4 → [C 24 ] + [HSO 4 ] − ·2H 2 SO 4 + 0.5 H 2 Ö
Grafit perklorat olarak, karbon atomuna sahip düzlemsel katları, 794 olan picometers ClO ayrılmış ayrı, 4 - iyonları. Grafit perklorat katodik indirgeme KC ısıtma benzerdir 8 , HCLO ardışık bir eleme uçları 4 .
Bir pozitif delik mekanizması kullanılarak tahmin edildiği gibi, hem grafit bisülfat hem de grafit perklorat, grafite kıyasla daha iyi iletkenlerdir. Grafitin [O 2 ] + [AsF 6 ] - ile reaksiyonu, [C 8 ] + [AsF 6 ] - tuzunu verir .
Metal halid türevleri
Bir dizi metal halojenür grafite karışır. Klorür türevleri en kapsamlı şekilde incelenmiştir. Örnekler arasında MCl 2 (M = Zn, Ni, Cu, Mn), MCl 3 (M = Al, Fe, Ga), MCl 4 (M = Zr, Pt), vb. sayılabilir . Malzemeler sıkı paketlenmiş metal katmanlarından oluşur. karbon tabakaları arasında halojenür tabakaları. Türev Cı ~ 8 FeCb 3 sergiler sıkma cam davranışı. Faz geçişlerini incelemek için özellikle verimli bir sistem olduğunu kanıtladı. Bir kademe n manyetik GIC, ardışık manyetik katmanları ayıran n grafit katmanına sahiptir. Aşama sayısı arttıkça ardışık manyetik katmanlardaki dönüşler arasındaki etkileşim zayıflar ve 2B manyetik davranış ortaya çıkabilir.
Halojen ve oksit grafit bileşikleri
Klor ve brom geri dönüşümlü olarak grafite karışır. İyot yapmaz. Flor geri dönüşümsüz tepki verir. Brom durumunda, aşağıdaki stokiyometriler bilinmektedir: n = 8, 12, 14, 16, 20 ve 28 için C n Br.
Geri dönüşümsüz olarak oluştuğundan, karbon monoflorür genellikle bir ara bileşik olarak sınıflandırılmaz. (CF) x formülüne sahiptir . Gaz halindeki florin 215-230 °C'de grafit karbon ile reaksiyonu ile hazırlanır . Renk grimsi, beyaz veya sarıdır. Karbon ve flor atomları arasındaki bağ kovalenttir. Tetracarbon monoflorür (Cı- 4 F) florin ve karışımı ile grafit işlenerek hazırlandığı hidrojen florür ile muamele edilmiştir. Bileşik siyahımsı mavi bir renge sahiptir. Karbon monoflorür elektriksel olarak iletken değildir. Bir tür birincil (şarj edilemeyen) lityum pillerde katot malzemesi olarak çalışılmıştır .
Grafit oksit , kararsız sarı bir katıdır.
Özellikler ve uygulamalar
Grafit interkalasyon bileşikleri, çeşitli elektronik ve elektriksel özellikleri nedeniyle uzun yıllardır malzeme bilimcilerini büyülemiştir.
süperiletkenlik
Süper iletken grafit interkalasyon bileşikleri arasında, CaC
6uygulanan basınç altında (15.1 K, 8 GPa'da) daha da artan en yüksek kritik sıcaklık Tc = 11,5 K sergiler . Bu bileşiklerdeki süperiletkenliğin, Fermi seviyesinin kabaca 2 eV (0.32 aJ) üzerinde yer alan serbest elektron benzeri bir bant olan ara katman durumunun rolü ile ilgili olduğu düşünülmektedir ; süperiletkenlik yalnızca ara katman durumu işgal edildiğinde oluşur. Saf CaC analizi
6açı çözümlü fotoemisyon spektroskopisi ölçümleri yapmak için ortaya çıkan yüksek kaliteli bir ultraviyole ışık kullanarak . π* bandında bir süperiletken boşluğun açılması, π*-ara katmanlar arası etkileşimden toplam elektron-fonon-bağlanma gücüne önemli bir katkıyı ortaya çıkardı.
Kimyasal sentezde reaktifler: KC 8
Bronz renkli malzeme KC 8 , bilinen en güçlü indirgeyici ajanlardan biridir. Ayrıca olarak kullanılmıştır katalizör olarak polimerizasyonlar ve şekilde birleştirme reaktif maddesi için aril halojenürler için bifeniller . Bir çalışmada, taze hazırlanmış KC 8 1-iodododecane (bir modifikasyonu teslim ile muamele edildi mikrometre içinde çözünür olan uzun alkil zincirleri çözünürlük sağlayan üzerinden yapıştırma ile ölçekli karbon trombositler) , kloroform . Bir başka potasyum grafit bileşiği olan KC 24 , bir nötron monokromatörü olarak kullanılmıştır. Potasyum iyon pilin icadı ile potasyum grafit için yeni bir temel uygulama tanıtıldı . Gibi lityum iyon pil , potasyum-iyon pil metalik bir anot yerine bir karbon-bazlı anot kullanmalıdır. Bu durumda potasyum grafitin kararlı yapısı önemli bir avantajdır.
Ayrıca bakınız
- Buckminsterfullerene interkalatlar
- kovalent süper iletkenler
- Karbon yerine altıgen düzlemsel bor levhaları kullanan magnezyum diborid
- pirolitik grafit
Referanslar
daha fazla okuma
- T. Enoki, M. Suzuki ve M. Endo (2003). Grafit interkalasyon bileşikleri ve uygulamaları . Oxford Üniversitesi Yayınları. ISBN'si 978-0-19-512827-7.
- Dresselhaus, MS ; Dresselhaus, G. (1981). "Grafitin interkalasyon bileşikleri". Fizikteki Gelişmeler . 30 (2): 139-326. Bibcode : 1981AdPhy..30..139D . doi : 10.1080/00018738100101367 .(187 sayfa), ayrıca Dresselhaus, MS olarak yeniden basılmıştır ; Dresselhaus, G. (2002). "Grafitin interkalasyon bileşikleri". Fizikteki Gelişmeler . 51 (1): 1–186. Bibcode : 2002AdPhy..51....1D . CiteSeerX 10.1.1.170.2655 . doi : 10.1080/00018730110113644 . S2CID 123597602 .
- D. Savoia; Trombini, C.; Umani-Ronchi, A.; et al. (1985). "Organik sentezde grafit üzerinde dağılmış potasyum-grafit ve metallerin uygulamaları" (PDF) . Saf ve Uygulamalı Kimya (PDF). 57 (12) : 1887. doi : 10.1351/pac198557121887 . S2CID 95591721 .
- Suzuki, Itsuko S.; Ting-Yu Huang; Masatsugu Suzuki (13 Haziran 2002). "Kademe-1 CoCl 2 grafit interkalasyon bileşiğinin manyetik faz diyagramı : Metamanyetik geçiş ve spin-flop geçişlerinin varlığı". Fiziksel İnceleme B . 65 (22): 224432. Bibcode : 2002PhRvB..65v4432S . doi : 10.1103/PhysRevB.65.224432 .
- Rancourt, Genel Müdür; C Meschi; Flandrios (1986). "S = 1/2 antiferromanyetik sonlu zincirleri etkin bir engellenme ile izole: CuCl 2 -intercalated grafit". Fiziksel İnceleme B . 33 (1): 347–355. Bibcode : 1986PhRvB..33..347R . doi : 10.1103/PhysRevB.33.347 . PMID 9937917 .