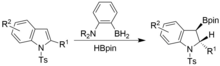Sinirli Lewis çifti - Frustrated Lewis pair
Kimyada, hüsrana uğramış bir Lewis çifti ( FLP ), bir Lewis asidi ve bir Lewis bazı içeren bir bileşik veya karışımdır ve bu, sterik engelleme nedeniyle klasik bir eklenti oluşturmak için birleşemez . Birçok FLP türü tasarlanmıştır ve birçok basit substrat aktivasyon sergiler.
Bazı FLPs H bölmek bu keşif 2 FLPs içine araştırma hızla büyümesine yol açmıştır. "Söndürülmemiş" reaktiviteleri nedeniyle, bu tür sistemler heterolize uğrayabilen substratlara karşı reaktiftir . Örneğin, birçok FLP, hidrojen moleküllerini böler . Bu nedenle, bir trisikloheksilfosfin (PCy 3 ) ve tris (pentaflorofenil) boran karışımı , ilgili fosfonyum ve borat iyonlarını vermek için hidrojen ile reaksiyona girer :
Bu reaktivite, hidrojenasyon reaksiyonlarını katalize eden FLP'ler üretmek için kullanılmıştır .
Küçük molekül aktivasyonu
Hayal kırıklığına uğramış Lewis çiftlerinin, ya heterolizi indükleyerek ya da koordinasyon yoluyla birçok küçük molekülü etkinleştirdiği gösterilmiştir.
Hidrojen
Bazı FLP'lerin ayrılabildiğinin ve dolayısıyla H 2'nin etkinleştirilebildiğinin keşfi, bu alandaki araştırmaların hızlı bir şekilde büyümesini tetikledi. H 2'nin aktivasyonu ve dolayısıyla kullanımı birçok kimyasal ve biyolojik dönüşüm için önemlidir. H serbest bırakılması için FLPs kullanılarak 2 metalsiz, bu genel olarak aktive H için kullanılan bir geçiş metallerinin maliyeti ve sınırlı olması nedeniyle yararlıdır 2 (Ni, Pd, Pt). FLP sistemleri, bu tür sistemlerin "söndürülmemiş" reaktivitesinden dolayı heterolize (örn. Hidrojen) uğrayabilen substratlara karşı reaktiftir . Örneğin, daha önce bir karışımı olduğu gösterilmiştir trisiklohekzilfosfin (PCY 3 ) ve tris (pentaflüorofenil) boran H reaksiyona girerek 2 ilgili elde fosfonyum ve borat iyonları:
Bu reaksiyonda, PCY 3 (Lewis Bazına) ve B (Cı- 6 F 5 ) 3 (Lewis asit) nedeniyle büyük sikloheksil ve pentafluorofenil gruplarından sterik engel bir ilave bileşiği oluşturmak olamaz. Borattan gelen fosfor ve hidrit üzerindeki proton artık 'aktive edilir' ve daha sonra bir organik substrata 'iletilebilir', bu da hidrojenasyonla sonuçlanır .
FLP ile dihidrojen aktivasyon mekanizması
H 2'nin FLP'ler tarafından aktivasyonu için mekanizma, hem moleküller arası hem de molekül içi vakalar için tartışılmıştır. Moleküller arası FLP'ler, Lewis Bazının Lewis Asitinden ayrı bir molekül olduğu yerlerdir, bu ayrı moleküllerin, Lewis Bazını ve Asiti bir araya getirmek için ikincil London dağılım etkileşimleri yoluyla etkileşime girdiği düşünülmektedir (organizasyon öncesi bir etki) burada küçük moleküller daha sonra etkileşime girebilir. FLP'ler ile. Moleküler düzeyde bu tür bir etkileşimin deneysel kanıtı belirsizdir. Ancak, hesaplamalı DFT (Yoğunluk Fonksiyonel Teorisi) çalışmalarına dayanan bu tür bir etkileşim için destekleyici kanıtlar vardır. Molekül içi FLP'ler, Lewis Asidi ve Lewis Bazının bir kovalent bağlayıcıyla bir molekülde birleştirildiği yerdir. Gelişmiş "organizasyon öncesi etkilere" rağmen, katı molekül içi FLP çerçevelerinin, esneklikte bir azalma nedeniyle küçük moleküllere karşı azaltılmış bir reaktiviteye sahip olduğu düşünülmektedir.
Diğer küçük moleküllü substratlar
FLPs de H dışındaki bir çok doymamış alt tabakalara karşı reaktif olan 2 . Bazı FLPs CO ile reaksiyona 2 , özellikle CO deoxygenative azalma, 2 metan.
Etilen ayrıca FLP'lerle reaksiyona girer:
Asit-baz çiftlerinin aynı anda hem nükleofilik hem de elektrofilik davranması için THF, 2,5-dihidrofuran, kumaran ve dioksan gibi siklik eterlerin halka açılması için bir yöntem sunar.
Katalizde kullanım
İmin, nitril ve aziridin hidrojenasyonu
İndirgenmesi iminler , nitriller , ve aziridinler birincil ve ikincil aminler , geleneksel olarak, metal hidrit belirteç ile, örneğin gerçekleştirilir lityum alüminyum hidrid ve sodyum siyanoborohidrit . Bu doymamış substratların hidrojenasyonu, metal katalizli reaksiyonlarla gerçekleştirilebilir. Metalsiz katalitik hidrojenasyon fosfonyum borat katalizörü (R kullanılarak gerçekleştirildi 2 PH) (Cı- 6 F 4 ) BH (Cı- 6 F 5 ) 2 (burada R = 2,4,6-Me 3 Cı 6 H 2 ) 1 . Bu tip metal içermeyen hidrojenasyon, yüksek maliyetli metal katalizörün yerini alma potansiyeline sahiptir.
İmin indirgeme mekanizmasının, iminyum tuzunu veren nitrojende protonasyonu içerdiği ileri sürülmektedir. Azot merkezinin bazikliği reaksiyon hızını belirler. Daha fazla elektron açısından zengin imin, elektron açısından fakir iminlere göre daha hızlı azalır. Ortaya çıkan iminyum merkezi , amini oluşturmak için borohidrür anyonu tarafından nükleofilik saldırıya uğrar . Küçük aminler borana bağlanarak diğer reaksiyonları söndürür. Bu sorun, çeşitli yöntemler kullanılarak aşılabilir: kullanılarak yüksek sıcaklıklarda 2) 1) Uygulama sterik B (Cı-imin korunması büyük imin ikame 3) 6 F 5 ) 3 , aynı zamanda, bir Lewis asidi yükseltici olarak görev yapan grubudur.
Enantiyoselektif imin hidrojenasyonu
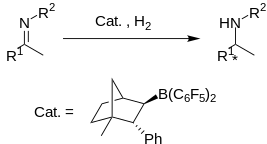
(1 R ) - ( + ) -camphor'dan türetilen kiral boronat Lewis asidi , bir tuz olarak izole edilebilen t Bu 3 P ile hayal kırıklığına uğramış bir Lewis çifti oluşturur . Bu FLP , bazı aril iminlerin enantiyoselektif hidrojenasyonunu yüksek verimle ancak orta düzeyde ee (% 83'e kadar) ile katalize eder .
Kavramsal olarak ilginç olmasına rağmen, protokol genellik eksikliğinden muzdariptir. İmin ikame edicilerinin artan sterik hacminin , amin ürününün veriminde ve ee'sinde düşüşe yol açtığı bulundu . metoksi ikameli iminler, üstün verim ve ee sergiler .
Asimetrik hidrosililasyon
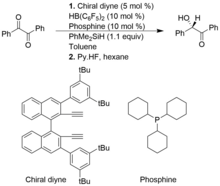
Bir grup katalizör, Frustrated Lewis çiftleri kiral alkenilboranlar ve fosfinler, 1,2-dikarbonil bileşiklerinin ve alfa-keto Esterlerin asimetrik Piers tipi hidrosillasyonları için faydalıdır ve bu da yüksek verimli enantioseçiciliğe sahip ürünlerle sonuçlanır. Bununla birlikte, geleneksel Piers tipi hidrosilizasyona kıyasla, asimetrik Piers tipi hidrosillasyonlar yeterince gelişmemiştir.
Aşağıdaki örnekte şiral alkenilboran, şiral diyne ve HB (C 6 F 5 ) 2'den in situ oluşturulur . FLP katalizörü tarafından PhMe 2 SiH'den Si-H bağının heterolitik bölünmesi, bir sililyum ve hidridoborat iyonik kompleksi oluşturur.
Alkin hidrojenasyonu
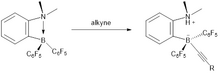
Aktive edilmemiş iç alkinlerin cis- alkenlere metal içermeyen hidrojenasyonu, FLP bazlı katalizörler kullanılarak kolayca elde edilir. Bu reaksiyon için durum H 2 bar kullanılarak nispeten yumuşak olan 2 . Mekanizma açısından, alkin malzeme önce hidroboratlanır ve ardından ortaya çıkan vinilboran bazlı FLP daha sonra dihidrojeni etkinleştirebilir. Bir protodeborylation aşama serbest bırakır -cis -alkenden nedeniyle elde edilen ürün, sin -hydroborylation işlemi ve katalizörün rejenere edilmesi. Alkin hidrojenasyonu için aktif olsalar da FLP bazlı katalizörler alkenlerin alkanlara hidrojenasyonunu kolaylaştırmaz.
Reaksiyon bir sin-hidroborasyondur ve sonuç olarak yüksek bir cis seçiciliği gözlenir. Cı katalitik devrinin son aşamasında 6 F 5 grup katalizör bozulmasını yerine alkan salınmasına neden olur, bir alkil grubu daha kolay ayrılır. Katalitik döngünün üç adımı vardır:
- Substrat bağlama (alkin hidroborasyonu)
- H 2 , N, N-Dimetil-2 geri kazanılması vinil ikame molekül içi protodeborylation, ardından vinilboran ile ayrılması, - [(pentafluorofenil) boril] anilin
- Cis-alken salınımı
Dahili alkinlerle, nitrojene bağlanan protonun florobenzenlere eklenebildiği rekabetçi bir reaksiyon meydana gelir. Bu nedenle, bu ekleme o kadar ilerlemiyor, alken oluşumu olumlu görünüyor.
Ancak terminal alkinler, borona hidroborasyon yoluyla değil, daha çok CH aktivasyonu yoluyla bağlanır. Bu nedenle, protonun alkine eklenmesi, ilk terminal alkin ile sonuçlanacaktır. Bu nedenle, bu hidrojenasyon işlemi terminal alkinler için uygun değildir ve sadece pentaflorobenzen verecektir.
Terminal alkinlerin ilgili alkenlere metal içermeyen hidrojenasyonu yakın zamanda bir piridon boran bazlı sistem kullanılarak başarıldı. Bu sistem, hidrojeni oda sıcaklığında kolayca aktive ederek bir piridon boran kompleksi verir. Bu kompleksin ayrışması, bir alkinin serbest boran tarafından hidroborasyonuna izin verir. Serbest piridon tarafından protodeborilasyon üzerine cis alken üretilir. Bu sistemle terminal alkinlerin hidrojenlenmesi mümkündür, çünkü CH aktivasyonu tersine çevrilebilir ve hidrojen aktivasyonu ile rekabet eder.
Borilasyon
Amin-boran FLP'ler, elektron açısından zengin aromatik heterosikllerin borilasyonunu katalize eder (Şema 1). Reaksiyon, FLP tarafından CH aktivasyonu yoluyla hidrojenin salınmasıyla yürütülür. Aromatik borilasyonlar, özellikle bor bileşiklerinin soy metallere kıyasla bolluğu, düşük maliyeti ve düşük toksisitesi nedeniyle, farmasötik geliştirmede sıklıkla kullanılır.
Reaksiyon için substratın, borilasyon mekanizmasına güçlü bir şekilde bağlı iki ana gereksinimi vardır. Birincisi, substrat elektron açısından zengin olmalıdır, tiyofen ile bir reaksiyonun olmaması örneklenirken, elektron açısından daha zengin türevleri - metoksitiyofen ve 3,4-etilendioksitiyofen - amino-boran ile bir reaksiyona girebilir. Ayrıca, 2-pozisyonunda kuvvetli elektron geri çeken tertbutiloksikarbonil (Boc) grubu ile 1-metilpirolün (reaksiyona girebilen) ikamesi , reaksiyonu tamamen inhibe eder. İkinci şart, aksi takdirde istenmeyen bir eklenti oluşturacak olan substratta bazik amin gruplarının olmaması içindir. Bu, hem 1-metil hem de N-benzilpirol türevlerinin reaksiyona girebilmesine karşın, pirol ile reaksiyonun olmamasıyla açıklanabilir.
Aynı yazarlar tarafından yapılan diğer çalışmalar, basitçe piperidinin (yukarıda gösterilen tetrametilpiperidinin aksine) amin R grubu olarak reaksiyon hızını hızlandırdığını ortaya koydu. Kinetik ve DFT çalışmaları yoluyla yazarlar, CH aktivasyon adımının daha büyük ikame edicilerden daha kolay olduğunu öne sürdüler.
Seviyelendirme de benzer koşullar altında, ancak N-tosil indoller kullanılarak gerçekleştirilebilir. Syn- hyrdoborylated indolinler elde edilir.
Bir dehidrojenatif işlemle tiollerde SH bağlarının borilasyonu da gözlenmiştir. Tert-Butanol ve tert-Butilamin gibi alkoller ve aminler, N / O atomunun yalnız çifti ile bor arasındaki güçlü bir π-bağı nedeniyle katalizi önleyen kararlı ürünler oluşturur, oysa aynısı tioller için geçerli değildir, bu nedenle başarılı katalize olanak sağlar. . Ayrıca Se-H bağlarının başarılı borilasyonu sağlanmıştır. Tüm durumlarda, H oluşumu 2 gaz reaksiyonları için büyük bir itici güçtür.
Karbon yakalama
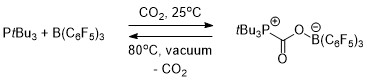
FLP kimyası kavramsal olarak karbon yakalama ile ilgilidir . Bir fosfin ve bir borandan oluşan hem moleküller arası (Şema 1) hem de molekül içi (Şema 2) FLP, karbon dioksiti seçici olarak yakalamak ve salmak için kullanıldı. FLP bir çözeltisi CO atmosferi kapsadığı zaman 2 , oda sıcaklığında, FLP-CO 2 elde edilmiş ve hemen beyaz bir katı olarak çökeltildi.
Arası FLP-CO Isıtma 2 CO yaklaşık yarısından salınması 5 saat için vakum altında 80 ° C de bromobenzen bileşik neden olmuştur 2 ve FLP iki kurucu bileşeni rejenere. Vakum altında oda sıcaklığında oturan birkaç saat daha sonra, toplam CO salımı 2 FLP yenilenmesi oluştu.
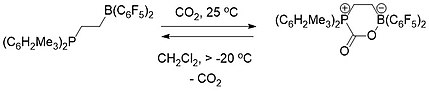
Molekül-içi FLP-CO 2 aksine bileşiği, oda sıcaklığında katı halde stabil ancak tam olarak diklorometan CO serbest içinde bir çözelti olarak 20 ° C'nin üzerindeki sıcaklıklarda bozulmuştur 2 ve FLP molekülü rejenere edilmesi.
Bu FLP karbon yakalama yöntemi, akış kimyası sistemlerinde çalışmak üzere uyarlanabilir.

![{\ displaystyle {\ ce {PCy3 + B (C6F5) 3 + H2 -> [HPCy3] + [HB (C6F5) 3] -}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3c7ea46199d1f74478288c7affc7bdd1fc964071)