halojensizleştirme - Dehalogenation
Olarak organik kimya halojenasyon Cı-halojen bağların bölünmesini içeren kimyasal reaksiyonların bir kümesidir. Dehalojenasyonlar, deflorinasyon, klorsuzlaştırma, debrominasyon ve deiyodinasyon dahil olmak üzere birçok çeşide sahiptir. Halojensizleştirmeleri araştırmaya yönelik teşvikler hem yapıcı hem de yıkıcı hedefleri içerir. Farmasötik ilaçlar gibi karmaşık organik bileşikler bazen halojensizleştirme ile üretilir. Birçok organohalojenür tehlikelidir, bu nedenle halojensizleştirmeleri detoksifikasyonlarının bir yoludur.
yollar
Bir organohalojenürlerden bir halojen atomunun çıkarılması, oldukça reaktif radikaller üretir. Bu gerçeğin birden fazla sonucu vardır:
- monodehalojenasyona genellikle ortaya çıkan radikalin bağlanması eşlik eder:
- 2 RX + 2 Li → RR + 2LiX
- bir çift halojenür karşılıklı olarak bitişik olduğunda (yakın), bunların çıkarılması tercih edilir. Visinal alkil dihalojenürler alkenlere dönüşür. Magnezyum kullanılabilir:
- R 2 C(X)C(X)R 2 + Mg → R 2 C=CR 2 + MgX 2
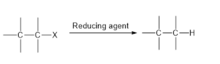
- halojensizleştirmeler, bir CX bağının bir CH bağı ile değiştirilmesi olan hidrojenoliz ile gerçekleştirilebilir . Bu tür reaksiyonlar katalize uygundur:
- RX + H 2 → RH + HX
Florür vs klorür vs bromür vs iyodür
Halojen giderme hızı, karbon ve halojen atomu arasındaki bağın gücüne bağlıdır. H: C-halojen bağlarının bağ ayrışma enerjileri olarak tanımlanmaktadır 3 , C-I (234 kJmol-1), 'H 3 , C-Br (293 kJmol-1),' H 3 C-CI (351 kJmol-1) ve H, 3 CF (452 kJmol-1). Bu nedenle, aynı yapılar için halojensizleştirme için bağ ayrışma oranı şöyle olacaktır: F < Cl < Br < I. Ek olarak, alkil halojenür için halojen giderme hızı da sterik ortama göre değişir ve bu eğilimi takip eder: birincil > ikincil > üçüncül halojenürler.
Uygulamalar
Organoklor bileşikleri en bol bulunan organohalojenürler olduğundan, çoğu halojen giderme C-Cl bağlarının manipülasyonunu gerektirir.
Alkali ve alkali toprak metaller
Yüksek elektropozitif metaller, metal-halojen değişiminde birçok organik halojenür ile reaksiyona girer :
- RX + 2 M → RM + MX
Ortaya çıkan organometalik bileşik hidrolize karşı hassastır:
- RM + H 2 O → RH + M-OH
Organolityum kimyası ve organomagnezyum kimyasında yoğun olarak çalışılmış örnekler bulunur . Bazı açıklayıcı vakalar takip eder.
Lityum-halojen değişimi , halojensizleştirme için önemsiz bir yol sağlar. Halojen giderme işlemi için sodyum metali kullanılmıştır. Yeni bileşiğin oluşumu için Grignard ajanı ve su varlığında aren-halojenürlerden halojen atomunun çıkarılması Grignard bozunması olarak bilinir. Grignard reaktifleri kullanılarak halojen giderme, iki aşamalı bir hidrodehalojenleştirme işlemidir. Reaksiyon, alkil/aren-magnezyum-halojen bileşiğinin oluşumu ile başlar, ardından dehalojene edilmiş ürün oluşturmak için proton kaynağı ilave edilir. Egorov ve çalışma arkadaşları, 600°C'de 3P durumunda atomik magnezyum kullanılarak benzil halojenürlerin halojensizleştirilmesini rapor ettiler. Reaksiyonun ürünü olarak toluen ve bi-benziller üretildi. Morrison ve çalışma arkadaşları ayrıca magnezyum kullanılarak flaş vakumlu piroliz ile organik halojenürlerin halojensiz hale getirildiğini bildirdi.
Geçiş metali kompleksleri ile
Birçok düşük değerli ve elektronca zengin geçiş metali, stokiyometrik dehalojenasyonu etkiler. Reaksiyon, organik sentez bağlamında, örneğin Cu-destekli Ullmann eşleşmesi bağlamında pratik ilgiye ulaşır .
Örnekler vanadyum, krom, manganez ve demir ve kobalt ile bulunabilir. B12 vitamini ve koenzim F430 , tetrakloroeten'i etene sırayla klorsuzlaştırma yeteneğine sahipken, hematinin tetrakloroeten'i vinil klorüre klorsuzlaştırdığı gösterildi.
Jayant ve çalışma arkadaşları, trikloretenlerin halojensizleştirilmesi için iki fazlı sistem geliştirdiler. Kinetik model, iki faz arasında kütle transferi yapılırken reaksiyon sürecinin tek fazda gerçekleşmesini sağlar.
daha fazla okuma
- Gotpagar, J.; Grulke, E.; Bhattacharyya, D.; Trikloroetilenin indirgeyici halojensizleştirilmesi: kinetik modeller ve *Hetflejš, J.; Czakkoova, M.; Rericha, R.; Vcelak, J. delor 103'ün sodyum hidridoalüminat ile katalizörlü halojensizleştirilmesi. Chemosfer 2001, 44, 1521.
- Kagoşima, H.; Hashimoto, Y.; Oguro, D.; Kutsuna, T.; Saigo, K. Trofenilfosfin/germanyum (IV) klorür kombinasyonu: a-bromo karboksilik asit türevlerinin indirgenmesi için yeni bir ajan. Dörtyüzlü, 1998, 39, 1203-1206