siklopropan - Cyclopropane

|
|||
|
|
|||
|
|
|||
| İsimler | |||
|---|---|---|---|
|
Tercih edilen IUPAC adı
siklopropan |
|||
| tanımlayıcılar | |||
|
3B model ( JSmol )
|
|||
| chebi | |||
| CHEMBL | |||
| Kimyasal Örümcek | |||
| ECHA Bilgi Kartı |
1000.771 |
||
| fıçı | |||
|
PubChem Müşteri Kimliği
|
|||
| ÜNİİ | |||
|
CompTox Panosu ( EPA )
|
|||
|
|||
|
|||
| Özellikleri | |||
| Cı- 3 , H 6 | |||
| Molar kütle | 42.08 g/mol | ||
| Görünüm | renksiz gaz | ||
| Koku | tatlı kokulu | ||
| Yoğunluk | 1.879 g/L (1 atm, 0 °C) | ||
| Erime noktası | −128 °C (−198 °F; 145 K) | ||
| Kaynama noktası | −33 °C (−27 °F; 240 K) | ||
| Asit (s K a ) | ~46 | ||
| -39.9 · 10 -6 cm 3 / mol | |||
| Tehlikeler | |||
| Ana tehlikeler | Son derece yanıcı Boğucu |
||
| Güvenlik Bilgi Formu | Harici MSDS | ||
| NFPA 704 (ateş elması) | |||
|
Aksi belirtilmedikçe, veriler standart durumdaki malzemeler için verilmiştir (25 °C [77 °F], 100 kPa'da). |
|||
|
|
|||
| Bilgi kutusu referansları | |||
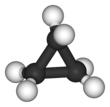
Siklopropan olan sikloalkan moleküler formül (CH 2 ) 3 üç oluşan metilen grubu (CH 2 bir halka oluşturmak üzere birbirine bağlanabilir). Halkanın küçük boyutu , yapıda önemli halka gerilimi yaratır . Siklopropanın kendisi esas olarak teorik olarak ilgi çekicidir ancak türevlerinin çoğu ticari veya biyolojik öneme sahiptir.
Tarih
Siklopropan, ilk makalesinde madde için doğru yapıyı da öneren August Freund tarafından 1881'de keşfedildi . Freund, 1,3-dibromopropan ile sodyum ile muamele ederek, doğrudan siklopropana yol açan intramoleküler bir Wurtz reaksiyonuna neden oldu. Reaksiyonun verimi, 1887'de Gustavson tarafından sodyum yerine çinko kullanılarak geliştirildi. Henderson ve Lucas, 1929'da anestetik özelliklerini keşfedene kadar siklopropanın ticari bir uygulaması yoktu; endüstriyel üretim 1936'da başlamıştı. Modern anestezik pratiğinde yerini diğer ajanlar aldı.
Anestezi
Siklopropan, o zamanlar pahalı olan bu ajanı korumak için karbondioksit absorpsiyonlu kapalı bir sistem kullanan Amerikalı anestezist Ralph Waters tarafından klinik kullanıma sunuldu . Siklopropan, minimum %17,5 alveolar konsantrasyonu ve 0,55 kan/gaz bölme katsayısı ile nispeten güçlü, tahriş edici olmayan ve hoş kokulu bir ajandır . Bu, siklopropan ve oksijenin solunmasıyla anestezi indüksiyonunun hızlı olduğu ve rahatsız edici olmadığı anlamına geliyordu. Bununla birlikte, uzun süreli anestezinin sonunda, hastalar kan basıncında ani bir düşüş yaşayabilir ve bu da potansiyel olarak kardiyak ritim bozukluğuna yol açabilir : "siklopropan şoku" olarak bilinen bir reaksiyon. Bu nedenle, yüksek maliyeti ve patlayıcı özelliğinin yanı sıra, son zamanlarda sadece anestezi indüksiyonu için kullanılmış ve 1980'lerin ortalarından beri klinik kullanıma sunulmamıştır. Silindirler ve akış ölçerler turuncu renkliydi.
Farmakoloji
Siklopropan GABA A ve glisin reseptörlerinde inaktiftir ve bunun yerine bir NMDA reseptör antagonisti olarak görev yapar . Ayrıca Bileşik AMPA reseptörü ve nikotinik asetilkolin reseptörleri ve bazı aktive K 2P kanalları .
Yapı ve yapıştırma
Siklopropanın üçgen yapısı, karbon-karbon kovalent bağları arasındaki bağ açılarının 60° olmasını gerektirir. Molekül D 3h moleküler simetriye sahiptir . Halka gerilimine ek olarak, molekül ayrıca hidrojen atomlarının gölgelenmiş konformasyonundan dolayı burulma gerilimine de sahiptir . Bu nedenle, karbon atomları arasındaki bağlar, tipik bir alkandan önemli ölçüde daha zayıftır ve bu da çok daha yüksek reaktivite ile sonuçlanır.
Karbon merkezleri arasındaki bağ genellikle bükülmüş bağlar olarak tanımlanır . Bu modelde, karbon-karbon bağları, yörüngeler arası açı 104° olacak şekilde dışa doğru bükülür. Bükülmüş bağlanmanın olağandışı bir sonucu, siklopropandaki CC bağlarının normalden daha zayıf olmasına rağmen, karbon atomlarının da normal bir alkan bağından daha yakın olmasıdır: 151 pm'ye karşı 153 pm (ortalama alken bağı: 146 pm).
Siklopropanın üç CC σ bağının altı elektronunun delokalizasyonu, E str ile referans olarak sikloheksan ile siklobütanla (26,2 kcal/mol) karşılaştırıldığında yalnızca biraz daha büyük siklopropan türünün ("yalnızca" 27.6 kcal/mol) açıklaması olarak verilmiştir. =0 kcal/mol. Bu stabilizasyon, örneğin benzende yüksek derecede stabilize edici bir etki olan olağan π aromatikliğinin aksine σ aromatikliği olarak adlandırılır . Diğer çalışmalar, siklopropanda σ-aromatikliğin rolünü ve indüklenmiş bir halka akımının varlığını desteklemez; bu tür çalışmalar, siklopropanın enerjik stabilizasyonu ve anormal manyetik davranışı için alternatif bir açıklama sağlar.
sentez
Siklopropan önce yoluyla üretilmiştir Wurtz eşlemesi olan, 1,3-dibromopropan edildi siklize kullanılarak sodyum . Bu reaksiyonun verimi , halojen giderici ajan olarak çinko ve katalizör olarak sodyum iyodür kullanılarak geliştirilebilir.
- BrCH 2 CH 2 CH 2 Br + 2 Na → (CH 2 ) 3 + 2 NaBr
Siklopropan halkaların hazırlanması olarak adlandırılır siklopropanasyon .
siklopropanlar
 1-Aminosiklopropan-1-karboksilik asit , bitki hormonu etilenin biyosentezinde önemli bir rol oynar .
1-Aminosiklopropan-1-karboksilik asit , bitki hormonu etilenin biyosentezinde önemli bir rol oynar .
Siklopropan türevleri çoktur. Birçok biyomolekül ve farmasötik ilaç , siklopropan halkasına sahiptir. Ünlü örnek , bir bitki hormonu olan etilenin öncüsü olan aminosiklopropan karboksilik asittir . Piretroidler birçok böcek temelini oluşturur. Birkaç siklopropan yağ asidi bilinmektedir.
Reaksiyonlar
CC bağlarının artan π-karakteri nedeniyle, siklopropan bazı durumlarda bir alken gibi reaksiyona girebilir. Örneğin bu maruz hidrohalojenlenmesiyle ile asitler mineral için vermek doğrusal alkil halojenürler. İkame edilmiş siklopropanlar da Markovnikov kuralına göre reaksiyona girer . İkame edilmiş Capson olabilir oksidatif eklemek için geçiş metalleri olarak adlandırılan bir işlemde, Cı-C aktivasyonu .
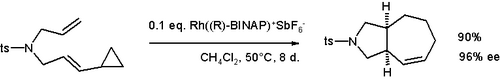
Vinil gruplarına bitişik siklopropil grupları, halka genişleme reaksiyonlarına girebilir . Örnekler, vinilsiklopropan yeniden düzenlemesini ve divinilsiklopropan-sikloheptadien yeniden düzenlemesini içerir . Bu reaktivite, siklobütenler gibi olağandışı siklik bileşikler veya aşağıda gösterilen siklohepten gibi bisiklik türler oluşturmak için kullanılabilir .
Emniyet
Siklopropan son derece yanıcıdır. Bununla birlikte, gerilme enerjisine rağmen, diğer alkanlardan önemli ölçüde daha patlayıcı değildir .
Ayrıca bakınız
- Tetrahedran , bir tetrahedronun yüzlerini oluşturan dört kaynaşmış siklopropan halkası içerir.
- Propellane , tek bir merkezi karbon-karbon bağını paylaşan üç siklopropan halkası içerir.
- siklopropen
- metilensiklopropan