taç eter - Crown ether
Taç eterler , birkaç eter grubu içeren bir halkadan oluşan halkalı kimyasal bileşiklerdir . En yaygın taç eterler ve siklik oligomerler arasında etilen oksit , tekrar birimi etilenoksi, yani, -CH 2 CH 2 -'dur. Bu dizinin önemli üyeleri tetramer ( n = 4), pentamer ( n = 5) ve heksamerdir ( n = 6). "Taç" terimi, bir katyona bağlı bir taç eterin yapısı ile bir kişinin kafasına oturan bir taç arasındaki benzerliği ifade eder . Bir taç eter adındaki ilk sayı, döngüdeki atomların sayısını belirtir ve ikinci sayı, oksijen olan atomların sayısını belirtir . Crown eterler, etilen oksitin oligomerlerinden çok daha geniştir ; önemli bir grup katekolden türetilmiştir .
Taç eterler, belirli katyonları güçlü bir şekilde bağlayarak kompleksler oluşturur . Oksijen atomları, halkanın iç kısmında bulunan bir katyonla koordine olmak için iyi bir şekilde yerleştirilmiştir, oysa halkanın dışı hidrofobiktir. Elde edilen katyonlar genellikle polar olmayan çözücülerde çözünür tuzlar oluşturur ve bu nedenle taç eterler faz transfer katalizinde faydalıdır . Dişlilik, polieter çeşitli katyonlar için taç eter çekimini etkiler. Örneğin, 18-taç-6, potasyum katyonu için yüksek afiniteye, sodyum katyonu için 15-taç-5 ve lityum katyonu için 12-taç-4'e sahiptir. Potasyum iyonları için 18-taç-6'nın yüksek afinitesi, toksisitesine katkıda bulunur. Hala katyonları bağlayabilen en küçük taç eter 8-taç-4'tür ve deneysel olarak onaylanmış en büyük taç eter 81-taç-27'dir. Kron eterler, potasyum katyonuna afinitesi olan tek makrosiklik ligand değildir. İyonoforlar gibi valinomycin da diğer katyonlar fazla potasyum katyon için belirgin bir tercih kullanmaz.
Taç eterlerin , taç eterin Lewis bazik oksijen atomları ve elektrofilik Lewis asit merkezi arasındaki elektrostatik, σ-deliği (bkz. halojen bağı ) etkileşimleri yoluyla Lewis asitleriyle koordine olduğu gösterilmiştir .
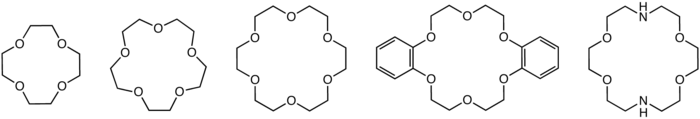 Yaygın taç eterlerinin yapıları: 12-taç-4 , 15-taç-5 , 18-taç-6 , dibenzo-18-taç-6 ve bir aza-taç eter
Yaygın taç eterlerinin yapıları: 12-taç-4 , 15-taç-5 , 18-taç-6 , dibenzo-18-taç-6 ve bir aza-taç eter
Tarih
1967'de DuPont'ta çalışan bir kimyager olan Charles Pedersen , iki değerlikli katyonlar için bir kompleks oluşturucu madde hazırlamaya çalışırken bir taç eter sentezlemenin basit bir yöntemini keşfetti . Stratejisi, iki katekolat grubunu her bir molekül üzerindeki bir hidroksil aracılığıyla bağlamayı gerektiriyordu . Bu bağlantı, katyonu kısmen sarabilen ve fenolik hidroksillerin iyonlaşmasıyla bağlı dikasyonu nötralize edebilen çok dişli bir ligandı tanımlar . Potasyum katyonlarını güçlü bir şekilde kompleksleştiren bir yan ürünü izole etmesine şaşırdı . Potasyumun 16-taç-4'te çözünmesiyle ilgili daha önceki çalışmalara atıfta bulunarak , siklik polieterlerin , alkali metal katyonlarını bağlayabilen yeni bir kompleks oluşturucu madde sınıfını temsil ettiğini fark etti . Taç eterlerin sentezi ve bağlayıcı özellikleriyle ilgili sistematik çalışmaları, ufuk açıcı bir dizi makalede rapor etmeye başladı. Organik sentez alanları , faz transfer katalizörleri ve diğer gelişmekte olan disiplinler, taç eterlerin keşfinden yararlandı. Pedersen, özellikle dibenzo taç eterlerini popüler hale getirdi.

Pedersen , taç eterlere giden sentetik yollar ve bunların bağlayıcı özelliklerinin keşfi için 1987 Nobel Kimya Ödülü'nü paylaştı .
katyonlar için afinite
Şelat etkisi ve makrosiklik etki nedeniyle , taç eterler, bölünmüş veya asiklik analoglarından farklı katyonlar için daha güçlü afiniteler sergiler . Burada alkali metal iyonları için katyon seçiciliği, esas olarak iyonun boyutuna ve yük yoğunluğuna ve taç eterin boşluk boyutuna bağlıdır.
| taç eter | Boşluk Boyutu/Å | Favori Alkali İyon | Etkili İyon Yarıçapı/Å |
|---|---|---|---|
| 12-taç-4 | 0.6-0.75 | Li + | 0.76 |
| 15-taç-5 | 0.86-0.92 | Hayır + | 1.02 |
| 18-taç-6 | 1.34-1.55 | K + | 1.38 |
| 21-taç-7 | 1.7-2.1 | cs + | 1.67 |
Belirli bir taç eterin lityum , sodyum ve potasyum katyonlarına olan afiniteleri , yük yoğunluklarındaki yüksek farklılıklara atfedilen birçok büyüklükte değişebilir. Potasyum, rubidyum ve sezyum katyonları arasında afinitelerdeki değişiklikler daha az belirgindir, çünkü yük yoğunlukları önceki dönemlerde alkali metallerden daha az değişir.
Potasyum katyonlarına olan yüksek afinitesinin yanı sıra, 18-crown-6 ayrıca protonlanmış aminlere bağlanabilir ve hem çözelti hem de gaz fazında çok kararlı kompleksler oluşturabilir. Lizin gibi bazı amino asitler yan zincirlerinde bir birincil amin içerir . Bu protonlanmış amino grupları, 18-taç-6'nın boşluğuna bağlanabilir ve gaz fazında kararlı kompleksler oluşturabilir. Protonlanmış aminlerin üç hidrojen atomu ile 18-taç-6'nın üç oksijen atomu arasında hidrojen bağları oluşur. Bu hidrojen bağları, kompleksi kararlı bir katkı maddesi yapar. Lüminesan sübstitüentleri omurgalarına dahil ederek, bu bileşiklerin hassas iyon probları oldukları kanıtlanmıştır, çünkü fotoaktif grupların absorpsiyonunda veya floresansındaki değişiklikler, mevcut çok düşük metal konsantrasyonları için ölçülebilir. Bazı çekici örnekler, antrasenler (9 ve/veya 10 konumları yoluyla) veya naftalenler (2 ve 3 konumları aracılığıyla) gibi poliaromatik türlere bağlanan oksijen ve/veya nitrojen donörleri içeren makro döngüleri içerir. Taç eterler tarafından boya iyonoforlarının bazı modifikasyonları , zincirli katyonların zincir uzunluklarına bağlı olan yok olma katsayıları sergiler .
Ayrıca bakınız
Referanslar
Dış bağlantılar
- Pedersen, Charles (1987). "Nobel Dersi" (PDF) . Nobel Ödülü .
- moleküler taç

