Krom (VI) oksit peroksit - Chromium(VI) oxide peroxide
|
|
| İsimler | |
|---|---|
| Diğer isimler
krom (VI) oksit peroksit,
krom pentoksit |
|
| Tanımlayıcılar | |
|
3B model ( JSmol )
|
|
|
PubChem Müşteri Kimliği
|
|
|
|
|
|
| Özellikleri | |
| Cr O 5 | |
| Molar kütle | 131,991 g · mol −1 |
| çözünür (stabilizatör olmadan ayrışır) | |
|
Aksi belirtilmedikçe, veriler standart hallerinde (25 ° C [77 ° F], 100 kPa) malzemeler için verilmiştir. |
|
|
|
|
| Bilgi kutusu referansları | |
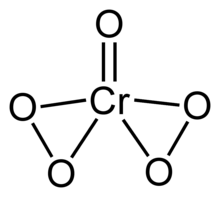
Krom (VI) peroksit veya krom oksit peroksit , CrO 5 formülüne sahip kararsız bir bileşiktir . Bu bileşik, krom atomu başına toplam beş oksijen atomu oluşturan bir okso ligand ve iki perokso ligand içerir.
Hazırlık ve özellikler
Krom (VI) peroksit, sodyum kromat veya potasyum dikromat gibi metal kromatların veya dikromatların solüsyonlarına asitleştirilmiş hidrojen peroksit solüsyonlarının eklenmesiyle oluşturulur . Genelde sarı kromatlar veya turuncu dikromatlar, krom (VI) peroksit oluştukça koyu maviye döner. Kromat veya dikromat, hidrojen peroksit ve bir asitle reaksiyona girerek krom peroksit ve su verir.
- CrO 4 2− + 2 H 2 O 2 + 2 H + → CrO 5 + 3 H 2 O
Bu yöntemle, krom (VI) peroksit birkaç saniye sonra ayrışacak ve krom (III) bileşikleri oluştukça yeşile dönecektir.
- 2 CrO 5 + 7 H 2 O 2 + 6 H + → 2 Cr 3+ + 10 H 2 O + 7 O 2
Bu ayrışmayı önlemek için , kromat / dikromat çözeltisinin üzerine bir organik çözücü katmanı ekleyerek dietil eter , bütan-1-ol veya amil asetat gibi suyla karışmayan organik çözücülerde krom (VI) oksit peroksiti stabilize etmek mümkündür ve hidrojen peroksit ilavesi sırasında sallama. Bu şekilde, krom (VI) peroksit (yeni oluştuğu sulu fazda kararsız), karışmayan organik çözücü içinde çözülür. Bu durumda çok daha uzun bir süre gözlemlenebilir.
CrO 5 kararsızdır ve Cro oluşturmak üzere bekletme üzerine ayrışır 3 . Ketonlar ve birincil alkoller ile uyumsuzdur , çünkü onları aldehitlere ve karboksilik asitlere oksitlerken kendisi Cr 3 + 'e indirgenir . Bu nedenle, CrO 5 , iki reaktif perokso ligandının varlığından dolayı kromatlardan ve dikromatlardan bile daha iyi bir oksitleyici ajandır, ancak düşük stabilitesi nedeniyle organik sentezlerde kullanılmamaktadır.
Türevler
Bu bileşiğin eterat, bipiridil ve piridil komplekslerinin organik kimyada etkili oksidanlar olduğu bulunmuştur. Piridil kompleksinin yapısı kristalografik olarak belirlenmiştir.
Fotoğraf Galerisi
Referanslar
Dış bağlantılar
- Deneysel ayrıntılar ve fotoğraf (Almanca)
- Kimyaya parmaklarını kaybetmek üzerine YouTube'a (8 Kasım 2012). Profesör Martyn Poliakoff ait Nottingham Üniversitesi ile sentezini gösterir Periyodik Videolar .
| Bu inorganik bileşikle ilgili makale bir taslaktır . Wikipedia'yı genişleterek yardım edebilirsiniz . |




