Klorlu asit - Chlorous acid
| |

| |
| İsimler | |
|---|---|
|
IUPAC adı
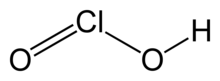
klorlu asit
| |
| Tanımlayıcılar | |
|
3D modeli ( JSmol )
|
|
| Chebi | |
| ChemSpider | |
| KEGG | |
|
pubchem CID
|
|
| |
| |
| Özellikleri | |
| H Cı O 2 | |
| Molar kütle | 68.46 g / mol |
| Asit (s K a ) | 1.96 |
| Eşlenik baz | klorit |
|
Aksi belirtilmediği sürece, veriler, malzemeler için verilmiştir , standart duruma (25 ° C [77 ° F] 100 kPa). | |
|
<Bu daha sonraki aşamada Bkz> doğrulamak ( ne <bakınız bu daha sonraki aşamada> ?)
| |
| Bilgikutusu kaynakları | |
Klorlu asit bir bir inorganik bileşik , formül HClO ile 2 . Bu ise , zayıf asit . Klor sahip oksidasyon durumunu bu asidin +3. Saf madde, kararsız bozucu için hipoklorik asit (Cı oksidasyon durumu + 1) ve klorik asit (Cı oksitlenme durumu + 5):
- 2 HClO 2 → HClO + HClO 3
Asit saf madde elde etmek zor olsa da, bunların konjuge baz, klorit , bu asitten türetilmiş, stabildir. Bu anyonun bir tuzu örneğin iyi bilinen sodyum klorit . Bu ve ilgili tuzları zaman zaman üretiminde kullanılan klorin dioksit .
Hazırlık
HClO 2 baryum ya da kurşun klorit ve seyreltik reaksiyonu yoluyla hazırlanabilir sülfürik asit :
- Ba (ClO 2 ) 2 + H 2 SO 4 BASO → 4 + 2 HClO 2
- Pb (ClO 2 ) 2 + H 2 SO 4 kurşun sülfat ile karıştırılan → 4 + 2 HClO 2
istikrar
orantısını olan eğilimi, oksitleme potansiyeli karşı koyar, ancak klorlu asit, güçlü bir oksidize edici ajandır.
Klor sadece halojen , formül HXO bir izole edilebilir asit oluşturmak üzere 2 . Ne bromöz asit veya iyot içeren asit hiç izole edilmiştir. Birkaç tuzları bromöz asit , bromites, bilinen, ancak edilir iodites .
Referanslar
![]() İlgili çoklu ortam klorlu asit ortak bir havuz deposundan en
İlgili çoklu ortam klorlu asit ortak bir havuz deposundan en
- ^ A b Egon Wiberg, Arnold Frederick Holleman (2001) İnorganik Kimya , Elsevier ISBN 0-12-352651-5
| Bu inorganik bileşik, madde lı a, saplama . Sen Vikipedi'ye katkıda bulunabilirsiniz genişletmeden . |
