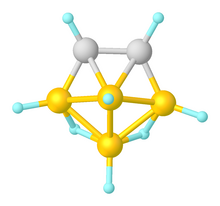
karboran - Carborane
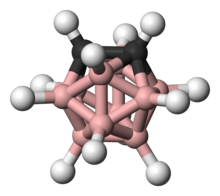
Karboranlar , küme çerçevesinde diğer metalik ve metalik olmayan elementleri de içerebilen bor , karbon ve hidrojen atomlarından oluşan elektronla delokalize (klasik olarak bağlı olmayan) kümelerdir . İlgili birçoğu gibi bor hidritler , bu kümeler olan polyhedra ya da polihedrayı fragmanlarını ve benzer olarak sınıflandırılır closo- , nido- , arachno- , hypho- bir tam (temsil olup temel, vb closo- ) bir çokgen veya bir ( nido- ), iki ( arakno- ), üç ( hifo- ) veya daha fazla köşesi olmayan bir çokyüzlü . Karboranlar, heteroboranların dikkate değer bir örneğidir .
Karboranların kafes çerçevesinde en az 5 ve en fazla 14 atomu olduğu bilinmektedir (metal atomları dahil edilmişse 15) ama çoğunluğunun iki kafes karbon atomu vardır; Bunların, en iyi bilinen serisi olmasıdır Closo -C 2 B n- H , n + 2 sistemleri, n = 3 için 12. Bununla birlikte, 1 ila 6 karbon atomuna sahip olan kafes karboranlar hazırlanmıştır gibi bir dizi var karboran mono- ve dianyonlar. İkozahedral CB 11 H 12 − anyonu, poliklorlu türevi H(CHB 11 Cl 11 ) bir süperasit olan güçlü bir eşlenik aside sahiptir .
İkosahedral yük duyarsız Closo -carboranes, 1,2-, 1,7-, ve 1,12-Cı- 2 B 10 , H 12 (sırasıyla orto -, meta - ve para gayri terminolojide -carborane) özellikle stabil olan ve ticari olarak mevcuttur. Bu bor bakımından zengin kümeler , klasik organik moleküllerle eşleşen kimyasal reaktivite ile benzersiz organomimetik özellikler sergiler , ancak yapısal olarak metal bazlı inorganik ve organometalik türlere benzer.
Cı- 2 B 10 , H 12 , diğer karboran kümeleri ve metallacarboranes (aşağıya bakınız) ısıya dayanıklı polimerler, nükleer atık, kataliz, yeni elektroaktif malzemelerden radyoaktif metallerin geri kazanılmasını da dahil olmak üzere, geniş bir uygulama aralığında, kullanılabilir ve edilmektedir birlikte izomerleri, tıbbi uygulamalar. Diğer elektron-delokalize çokyüzlü kümeler için olduğu gibi, bu küme bileşiklerinin elektronik yapısı Wade-Mingos kuralları ile tanımlanabilir .
Yukarıda belirtildiği gibi, karboranlar bor hidritleri ( boranlar ) ile yakından ilişkilidir ve bu nedenle karbon atomlarının bor atomlarından bir daha fazla değerlik elektronuna sahip olması nedeniyle yapısal olarak hidrokarbonlardan çok farklıdır (karboranların dikkate değer bir özelliği, kafesin karbon atomları genellikle hidrokarbonlardan oldukça farklı olarak 6 veya daha fazla komşu atoma doğrudan bağlıdır).
Karboranlar ve boranlar, elektron-delokalize klasik olmayan bağlarını kolaylaştırmak için 3 boyutlu kafes (küme) geometrilerini benimser, hidrokarbonlar ise tipik olarak zincirler veya halkalardır; Örneğin, B 4 H 10 , bir yer alır Arachno bütan izomerleri ise, kafes geometrisi , n ve - izo -C 4 H 10 , B 4'ten fazla elektronlar ile 4 H 10 , doğrusal ya da dallı zincirli yapıları kabul eder. Örnekleri arasında nido ve Arachno - karboranlar 2,3-Cı bulunmaktadır 2 B 4 H 8 ve 1,3-C 2 B 7 , H 13 , sırasıyla. Karboranların geometrik izomerleri mevcut olabilir, bu da bir bileşiğin adında sayısal öneklerin kullanılmasını gerektirir; bu, daha önce değinilen 1,2-, 1,7- ve 1,2-C 2 B 10 H 12 ikosahedral kümelerle gösterilmektedir.
Hazırlık
Karboranlar birçok farklı yolla hazırlanmıştır, en yaygın olanı dikarbon karboranları oluşturmak için bor hidrit kümelerine alkinil reaktiflerinin eklenmesidir. Örneğin, pentaboranın(9) asetilen ile yüksek sıcaklıktaki reaksiyonu, diğer ürünlerin yanı sıra birkaç klozo-karboran verir:
- nido -B 5 H 9 + C 2 H 2 closo -1,5-C 2 B 3 H 5 , closo -1,6-C 2 B 4 H 6 , 2,4-C 2 B 5 H 7
Reaksiyon daha düşük sıcaklıklarda yürütüldüğünde, açık kafesli bir karboran elde edilir:
- nido -B 5 H 9 + C 2 H 2 nido -2,4-C 2 B 4 H 8
Diğer prosedürler, üç veya dört kafes karbon atomu içeren karboranlar üretir ( ref. [1],[4],[5] )
monokarba türevleri
Mono karboranlar, B n C kafesli kümelerdir . 12 köşeli türev en iyi çalışılır, ancak birkaç tanesi bilinmektedir.
Tipik olarak, bor hidrit kümelerine tek karbonlu reaktiflerin eklenmesiyle hazırlanırlar. Tek karbonlu reaktifler arasında siyanür , izosiyanürler ve formaldehit bulunur . Örneğin, monokardodekaborat ([CB 11 H 12 ] - ) dekaboran ve formaldehitten üretilir , ardından boran dimetilsülfit ilave edilir . Monokarboranlar, zayıf şekilde koordine olan anyonların öncüleridir .
Dikarba kümeleri
Dicarbaboranlar, iki karbon merkezinin kaynağı olarak alkinler kullanılarak bor hidritlerinden hazırlanabilir. Ek olarak Closo -C 2 B n- H , n + 2 , yukarıda belirtilen dizi gibi, çeşitli açık kafesli DBE türleri dahil olmak üzere bilinen edilir nido -C 2 B 3 H 7 (B ile izo-ve izoelektronik 5 H 9 ) ve Arachno -C 2 B 7 H 13 .
İkosahedral sentezleri Closo -dicarbadodecaborane türevlerinin (R 2 Cı- 2 B 10 , H 10 ), R, istihdam alkinler 2 Cı- 2 kaynak ve decaboran (B 10 , H 14 B sağlamak için) 10 birim.
Tricarba, tetracarba, pentacarba ve hexacarba kümeleri
Çeşitli yollarla elde kemiklerini ikiden fazla karbon atomuna sahip olan Karboranlar, türevleri bulunur nido -C 3 B 3 H 7 , nido -C 3 B 8 H 11 , nido -C 4 B 2 H 6 , nido -C 4 B 4 H 8 , nido -C 5 BH 6 + ve Arachno -H 6 Cı 6 B 6 Et 6 ( referans [1] ).
izomerizm
Birçok dikarbaboran, karbon merkezlerinin nispi konumlarında farklılık gösteren izomerler olarak bulunur. Üç daha önce sözü edilen ikosahedral C ek olarak, 2 B 10 , H 12 bileşikleri, izomerizm de bazı küçük bulunan Closo , -carborane sistemleri, örneğin, 1,2- ve 1,6-Cı- 2 B 4 H 6 , 2,3- ve 2,4-C 2 B 5 H 7 , 1,2- ve 1,6-C 2 B 6 H 8 ve 2,3- ve 2,4-C 2 B 5 H 7 ve ayrıca açıkta -cage karboranlar gibi 2,3- ve 2,4-Cı- 2 B 4 H 8 ve 1,2 ve 1,3-Cı- 2 B 9 H 13 .
Genel olarak, bitişik olmayan kafes karbon atomlarına sahip izomerler, bitişik karbonlara sahip olanlardan termal olarak daha kararlıdır, böylece ısıtma, çerçevedeki karbon atomlarının karşılıklı olarak ayrılmasını indükleme eğilimindedir. Bu 1,6-C 1,2- termal izomerizasyonu ile gösterilmiştir 2 B 4 H 6 ve 1,2- 1,7-C 2 B 10 , H 12 . 1,12-Cı oluşumu 2 B 10 , H 12 ( para bir ayrışma ile birlikte çok daha yüksek sıcaklıklarda (600 ° ilgili C) gerektirmektedir izomer -carborane) ( ref. [1], [4] ve [5] ) .
Reaksiyonlar
Karboranlar çok çeşitli reaksiyonlara girerler. Deprotone Closo kullanılarak -dicarbadodecaboranes organolityum reaktifleri Dilityo türevlerini verir.
- C 2 B 10 H 12 + 2 BuLi → Li 2 C 2 B 10 H 10 + 2 BuH
Bu inceltilmiş bileşikler, örneğin klorofosfinler, klorosilanlar ve kükürt gibi çeşitli elektrofillerle reaksiyona girer.
Karboranların baz kaynaklı bozunması , kafes çerçevesinde bir veya daha fazla geçiş metali veya ana grup metal atomu içeren karboranlar olan metalakarboranlar üreten geçiş metalleri için ligandlar olarak kullanılabilen anyonik nido türevlerini verir . En ünlüsü [C 2 B 9 H 11 ] 2- formülüyle dikarbollittir . Bu ligandlar sandviç kompleksler oluşturur. Metallakarboranlar üzerindeki çalışmaların büyük kısmı, 12 köşeli MC 2 B 9 ve M 2 C 2 B 8 kümeleri ve 7 köşeli MC 2 B 4 ve M 2 C 2 B 3 (üç katlı ve çok katlı sandviç) kümeleri üzerinde odaklanmıştır, ancak değişen sayıda karbon, bor ve metal atomuna sahip kümeler gibi 6 ila 15 köşeli metalakarboranlar da hazırlanmıştır (bkz. ref. [1], [4] ve [5] ). MC sahip Diborolyl metali kompleksleri 3 oda 2 ve M, 2 C 3 B 2 metallacarborane başka türünü temsil kafesleri, aynı zamanda yaygın olarak incelenmiştir.
Araştırma
Dicarbollide kompleksleri uzun yıllardır birçok uygulama için değerlendirilmiştir, ancak ticari uygulamalar nadirdir. Bis(dikarbollid) [Co(C 2 B 9 H 11 ) 2 ] − , radyo atıklardan 137 Cs + 'nın uzaklaştırılması için bir çökeltici olarak kullanılmıştır .
Karboranların tıbbi uygulamaları araştırılmıştır. C-fonksiyonelleştirilmiş karboranlar, boron nötron yakalama tedavisi için bir bor kaynağını temsil eder .
Bazı metal kompleksleri katalitik özellikler sergiler.
Bileşik H (CHB 11 Cı 11 ) a, superacid ile izole edilebilir tuzu oluşturan, protonlanmış benzen , Cı 6 H+
7. Fulleren , C 60'ı protonlar .