Buckminsterfullerene - Buckminsterfullerene
|
|
|||
| İsimler | |||
|---|---|---|---|
|
Tercih edilen IUPAC adı
(C 60 - I h )[5,6]fuleren |
|||
| Diğer isimler
Buckytopları; Fulleren-Cı- 60 ; [60]fuleren
|
|||
| tanımlayıcılar | |||
|
3B model ( JSmol )
|
|||
| 5901022 | |||
| chebi | |||
| Kimyasal Örümcek | |||
| ECHA Bilgi Kartı |
100.156.884 |
||
|
PubChem Müşteri Kimliği
|
|||
| ÜNİİ | |||
|
CompTox Panosu ( EPA )
|
|||
|
|||
|
|||
| Özellikler | |||
| Cı- 60 | |||
| Molar kütle | 720,660 g·mol -1 | ||
| Dış görünüş | Koyu iğne benzeri kristaller | ||
| Yoğunluk | 1.65 g / cc 3. | ||
| suda çözünmez | |||
| Buhar basıncı | 0,4–0,5 Pa (T ≈ 800 K); 14 Pa (T ≈ 900 K) | ||
| Yapı | |||
| Yüz merkezli kübik, cF1924 | |||
| Fm 3 m, No. 225 | |||
|
a = 1.4154 nm
|
|||
| Tehlikeler | |||
| GHS piktogramları |

|
||
| GHS Sinyal kelimesi | Uyarı | ||
| H315 , H319 , H335 | |||
| P261 , P264 , P271 , P280 , P302+352 , P304+340 , P305+351+338 , P312 , P321 , P332+313 , P337+313 , P362 , P403+233 , P405 , P501 | |||
|
Aksi belirtilmediği sürece, veriler standart durumdaki malzemeler için verilmiştir (25 °C [77 °F], 100 kPa'da). |
|||
|
|
|||
| Bilgi kutusu referansları | |||
| hakkında bir dizi makalenin bir parçası |
| Nanomalzemeler |
|---|
 |
| Karbon nanotüpler |
| Fullerenler |
| Diğer nanoparçacıklar |
| Nano yapılı malzemeler |
Buckminsterfullerene , C 60 formülüne sahip bir fulleren türüdür . Yirmi altıgen ve on iki beşgenden oluşan bir futbol topunu andıran kafes benzeri bir kaynaşmış halka yapısına ( kesik ikosahedron ) sahiptir . Her karbon atomunun üç bağı vardır. Mor bir çözelti üretmek için hidrokarbon çözücülerde çözünen siyah bir katıdır. Bileşik, çok az gerçek dünya uygulaması bulunmasına rağmen, yoğun bir çalışma aldı.
oluşum
Buckminsterfullerene, en yaygın doğal olarak oluşan fullerendir. Küçük miktarlarda kurumda bulunabilir . Uzayda da vardır . Nötr C 60 , gezegenimsi bulutsularda ve çeşitli yıldız türlerinde gözlemlenmiştir . İyonlaşmış biçime, Cı- 60 + , tespit edilmiştir yıldızlararası ortamın ve taşıyıcı bazılarının yaygın yıldızlararası bantlar .
Tarih

Buckyball moleküllerinin teorik tahminleri 1960'ların sonlarında ve 1970'lerin başında ortaya çıktı, ancak bu raporlar büyük ölçüde fark edilmedi. Buckminsterfullerene ilk olarak 1984 yılında Eric Rohlfing, Donald Cox ve Andrew Kaldor tarafından süpersonik bir helyum ışını içinde karbonu buharlaştırmak için bir lazer kullanılarak üretildi. 1985 yılında işlerini tarafından tekrarlandı Harold Kroto , James R. Heath , Sean O'Brien, Robert Curl ve Richard Smalley de Rice Üniversitesi'nden C yapısını tanıdı 60 Bukminsterfuleren olarak.
Eşzamanlı ama Kroto-Smalley çalışmasına bağlı olmayan astrofizikçiler, dev kırmızı karbon yıldızlarından gelen kızılötesi emisyonları incelemek için spektroskopistlerle birlikte çalışıyorlardı. Smalley ve ekibi, kırmızı karbon yıldızı tarafından yayılanla aynı dalga boyunda potansiyel olarak kızılötesi yayan karbon kümeleri oluşturmak için bir lazer buharlaştırma tekniği kullanabildiler. Bu nedenle Smalley ve ekibine, fullerenler üretmek için grafit üzerinde lazer tekniğini kullanma ilhamı geldi.
C 60 , 1985 yılında Robert Curl, Harold Kroto ve Richard Smalley tarafından keşfedilmiştir. Kullanarak lazer buharlaşma ve grafit da Cı bulunan n- kümeleri (burada n > 20 ve hatta) olan en yaygın ° C, 60 ve C 70 . Katı bir dönen grafit disk, karbonun bir lazer ışını kullanılarak buharlaştırıldığı ve daha sonra yüksek yoğunluklu bir helyum gazı akışından geçirilen sıcak plazma oluşturan yüzey olarak kullanıldı. Karbon türleri daha sonra soğutuldu ve iyonlaştırıldı, bu da kümelerin oluşmasına neden oldu. Kümeler moleküler kütlelerde değişiyordu, ancak Kroto ve Smalley , plazmanın daha uzun süre reaksiyona girmesine izin vererek daha da geliştirilebilecek bir C 60 kümesinde baskınlık buldu . Ayrıca, C 60 molekülünün kafes benzeri bir yapı, düzenli bir kesik ikosahedron oluşturduğunu keşfettiler .
Kroto, Curl ve Smalley , buckminsterfullerene ve ilgili molekül sınıfı fullerene keşfindeki rollerinden dolayı 1996 Nobel Kimya Ödülü'ne layık görüldü .
720 atomik kütle biriminde güçlü bir tepe noktası olan deneysel kanıt, 60 karbon atomlu bir karbon molekülünün oluştuğunu gösterdi, ancak yapısal bilgi sağlamadı. Araştırma grubu, reaktivite deneylerinden sonra, en olası yapının küresel bir molekül olduğu sonucuna vardı. Fikir, bir ikosahedral simetri kapalı kafes yapısının temeli olarak hızla rasyonalize edildi . Kroto, ünlü fütürist ve mucit Buckminster Fuller'ın jeodezik kubbe yapılarından , bu özel maddenin buckminsterfullerene olarak adlandırılmasındaki etkiler olarak bahsetti .
1989'da fizikçiler Wolfgang Krätschmer , Konstantinos Fostiropoulos ve Donald R. Huffman , ince karbon tozu (kurum) filmlerinde olağandışı optik absorpsiyonlar gözlemlediler. Kurum , elektrot malzemesinin buharlaştığı ve söndürme atmosferinde kurum oluşturan yoğunlaştığı bir helyum atmosferinde iki grafit elektrot arasındaki bir ark işlemiyle üretilmişti . Diğer özelliklerin yanı sıra, is IR spektrumları C önerilenlere yakın uyum içinde dört ayrı bantlar gösterdi 60 .
Moleküler yapının karakterizasyonu ve doğrulanması üzerine bir başka makale, aynı yıl (1990) ince film deneylerini takip etti ve ayrıca ark tarafından oluşturulan kurumdan buharlaşabilen ve benzen çözünür bir malzemenin ekstraksiyonu hakkında ayrıntılı bilgi verdi . Bu ekstre vardı TEM ve X-ışını küresel C dizileri ile tutarlı bir kristal analizi 60 moleküller, yaklaşık 1.0 nm Waals çapı der van gibi C için 720 Da beklenen molekül kütlesinde 60 (C ve 840 Da 70 olarak) kendi kütle spektrumları . Metod, materyali günde gram miktarlarda hazırlamak için basit ve etkiliydi (1990), bu da fulleren araştırmalarını hızlandırdı ve bugün bile fullerenlerin ticari üretimi için uygulanıyor.
C 60'a giden pratik yolların keşfi, fullerenlerin incelenmesini içeren yeni bir kimya alanının keşfedilmesine yol açtı.
etimoloji
Allotropu keşfedenler, yeni keşfedilen moleküle , C 60'a benzeyen birçok jeodezik kubbe yapısı tasarlayan ve 1984'teki keşiften önce 1983'te ölen Buckminster Fuller'ın adını verdiler. Ancak bu, Fuller'in jeodezik kubbeleri olarak biraz yanıltıcıdır. yalnızca altıgenleri veya beşgenleri üçgenlere bölerek inşa edilir, bunlar daha sonra köşeleri bir kürenin yüzeyine sığdırmak için radyal olarak dışa doğru hareket ettirerek deforme olur. Geometrik olarak konuşursak, buckminsterfullerene, bir Goldberg polihedronunun doğal olarak oluşan bir örneğidir . Buckminsterfullerene için yaygın, kısaltılmış bir isim buckyballs'dur .
sentez
İs grafit lazerle ablasyon tarafından üretilen ya da Piroliz arasında aromatik hidrokarbonlar . Fullerenler, bir Soxhlet ekstraktörü kullanılarak organik çözücüler ile kurumdan ekstrakte edilir . Bu adım, bir C kadar% 75 içeren bir çözelti verir 60 , hem de diğer fullerenesden. Bu fraksiyonlar kromatografi kullanılarak ayrılır . Genel olarak, fullerenler bir hidrokarbon veya halojenli hidrokarbon içinde çözülür ve alümina kolonları kullanılarak ayrılır.
Yapı
Buckminsterfullerene, 60 köşesi ve 32 yüzü (20 altıgen ve hiçbir beşgenin bir köşeyi paylaşmadığı 12 beşgen) ve her çokgenin köşelerinde bir karbon atomu ve her çokgen kenarı boyunca bir bağı olan, kesik bir ikosahedrondur . Waals çapı der Van a C
60molekül yaklaşık 1.01 nanometredir (nm). Bir C'nin çekirdeğinden çekirdek çapına
60molekül yaklaşık 0.71 nm'dir. C
60molekülün iki bağ uzunluğu vardır. 6:6 halka bağları (iki altıgen arasındaki) " çift bağ " olarak kabul edilebilir ve 6:5 bağlardan (altıgen ile beşgen arasındaki) daha kısadır. Ortalama bağ uzunluğu 0.14 nm'dir. Yapıdaki her bir karbon atomu, diğer 3 karbon atomu ile kovalent olarak bağlanmıştır.
Özellikler
Bir süre için buckminsterfullerene, dalga-parçacık ikiliği sergilediği gözlemlenen bilinen en büyük moleküldü ; teorik olarak her nesne bu davranışı sergiler. 2020'de boya molekülü ftalosiyanin , daha çok ışığa, elektronlara ve diğer küçük parçacıklara ve moleküllere atfedilen ikiliği sergiledi.
Molekül stabildir, yüksek sıcaklıklara ve yüksek basınçlara dayanır.
C
60C'ye altı tersinir, tek elektronlu indirgeme geçirir6−
60, ancak oksidasyon geri döndürülemez. İlk indirgeme için ≈1.0 V ( Fc / Fc+
), Cı gösteren 60 orta düzeyde etkili bir elektron alıcı olup. C
60pentagonal halkalarda elektron delokalizasyonunu zayıflatan ve C ile sonuçlanan çift bağlardan kaçınma eğilimindedir.
60" süperaromatik " olmamak . Cı- 60 çok elektron eksikli gibi davranır alken ve kolayca reaksiyona girer ile elektron bakımından zengin türleri.
C'de bir karbon atomu
60molekül, bir C veren bir nitrojen veya bor atomu ile ikame edilebilir
59Sırasıyla N veya C 59 B.
| tarafından merkezli | tepe noktası | Kenar 5-6 |
Kenar 6–6 |
Yüz Altıgen |
Yüz Pentagon |
|---|---|---|---|---|---|
| resim |

|
|
|
|

|
| projektif simetri |
[2] | [2] | [2] | [6] | [10] |
Çözüm
| çözücü | Çözünürlük (g/L) |
|---|---|
| 1-kloronaftalin | 51 |
| 1-metilnaftalin | 33 |
| 1,2-diklorobenzen | 24 |
| 1,2,4-trimetilbenzen | 18 |
| tetrahidronaftalin | 16 |
| karbon disülfid | 8 |
| 1,2,3-tribromopropan | 8 |
| ksilen | 5 |
| bromoform | 5 |
| kümen | 4 |
| toluen | 3 |
| benzen | 1.5 |
| karbon tetraklorür | 0.447 |
| kloroform | 0.25 |
| n - heksan | 0.046 |
| sikloheksan | 0.035 |
| tetrahidrofuran | 0.006 |
| asetonitril | 0.004 |
| metanol | 0.00004 |
| Su | 1,3 × 10 −11 |
| pentan | 0.004 |
| oktan | 0.025 |
| izooktan | 0.026 |
| dekan | 0.070 |
| dodekan | 0.091 |
| tetradekan | 0.126 |
| dioksan | 0.0041 |
| mesitilen | 0,997 |
| diklorometan | 0.254 |
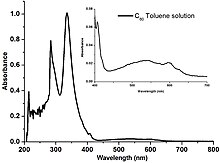
Fullerenler aromatik çözücülerde ve karbon disülfidde az çözünür , ancak suda çözünmez. Saf C çözeltileri 60 buharlaşması üzerine bir kahverengi bir tortu bırakır koyu mor bir renge sahiptir. Bu renk değişikliğinin nedeni, bireysel C60 molekülleri tarafından yeşil ışık absorpsiyonundan sorumlu moleküler seviyeler bandının nispeten dar enerji genişliğidir . Böylece tek tek moleküller bir miktar mavi ve kırmızı ışığı iletir ve bu da mor bir renge neden olur. Kuruma üzerine, moleküller arası etkileşim, enerji bantlarının örtüşmesi ve genişlemesi ile sonuçlanır, böylece mavi ışık geçirgenliğini ortadan kaldırır ve mordan kahverengiye renk değişimine neden olur.
C
60kafes içinde bazı çözücüler ("solvatlar") ile kristalleşir. Örneğin, C kristalizasyonu 60 içinde benzen çözeltisi formülü ile triklinik kristaller elde 60 · 4C 6 H 6 . Diğer solvatları gibi, bu hali hazırda serbest bırakır bilinen FCC C vermek üzere benzen 60 . C 60 ve C'nin milimetrik boyutlu kristalleri
70 hem solvatlar hem de saf fullerenler için çözeltiden yetiştirilebilir.
Sağlam
Katı buckminsterfullerende, C 60 molekülleri fcc ( yüz merkezli kübik ) motifini benimser . Yaklaşık -20 °C'de dönmeye başlarlar. Bu değişiklik, bir fcc yapısına birinci dereceden bir faz geçişi ve kafes sabitinde 1.411'den 1.4154 nm'ye küçük, ancak ani bir artış ile ilişkilidir.
C
60katı grafit kadar yumuşaktır , ancak hacminin %70'inden daha azına sıkıştırıldığında süper sert bir elmas formuna dönüşür (bkz. toplu elmas nanoçubuk ). C
60filmler ve çözelti, güçlü doğrusal olmayan optik özelliklere sahiptir; özellikle, optik absorpsiyonları ışık yoğunluğu ile artar (doyurabilir absorpsiyon).
C
60≈1.6 eV'de optik absorpsiyon eşiği ile kahverengimsi bir katı oluşturur. 0.1-0.3 eV düşük aktivasyon enerjisine sahip n-tipi bir yarı iletkendir ; bu iletkenlik, içsel veya oksijenle ilgili kusurlara atfedilir. Fcc C 60 , safsızlık atomlarını barındırmak için yeterince büyük (sırasıyla 0,6 ve 0,2 nm) oktahedral ve tetrahedral bölgelerinde boşluklar içerir. Bu boşluklara alkali metaller katkılandığında , C 60 bir yarı iletkenden bir iletkene ve hatta süper iletkene dönüşür.
Kimyasal reaksiyonlar ve özellikleri
hidrojenasyon
C 60 , küçük bir derecede aromatik karakter sergiler, ancak yine de lokalize çift ve tek C–C bağ karakterlerini yansıtır. Bu nedenle, C 60 vermek polyhydrofullerenes hidrojen ile eklemesine de maruz kalabilirler. C 60 ayrıca Huş ağacı redüksiyonuna tabi tutulur . Örneğin, Cı- 60 ve ardından sıvı amonyak içinde lityum ile tepkimeye girer, ters C gibi polyhydrofullerenes arasında butanol ile vermek karışımı 60 H 18 , Cı- 60 , H 32 , Cı- 60 , H 36 ° C ile, 60 H 32 görünen ürün olması. Yükseltgenmiştir yeniden polyhydrofullerenes bu karışımı olabilir 2,3-dikloro-5,6-disiyano-1,4-benzokinon Cı vermek üzere 60 tekrar.
Seçici bir hidrojenasyon yöntemi mevcuttur. C 60'ın aynı koşullar altında 9,9',10,10'-dihidroantrasen ile reaksiyonu, reaksiyon zamanına bağlı olarak, sırasıyla ve seçici olarak C 60 H 32 ve C 60 H 18'i verir.
Cı- 60 , bir modifiye edilmiş malanoik "yüksek yoğunluk, oda sıcaklığı, ortam basıncı için bir araç haline gelebilir organometalik buckyballs (ÖBBS) olarak adlandırılan düşündüren, hidrojene edilebilir , hidrojen depolama ". Bu ÖBBS bir atomlarını bağlanmasıyla oluşturulan geçiş metaline C (TM) 60 veya C 48 B 12 organometalik Buckyball'un iç boyunca eşit olarak dağıtılması, bu TM atomuna çok sayıda hidrojen atomuna bağlanması ve daha sonra. Çalışma H, teorik miktarda bulundu 2 de OBB alınabilir çevre basıncı 9 yaklaşımlar ağırlıkça% , hidrojen yakıtı için optimum olarak belirlenmiş olan bir kütle payı , ABD Enerji Bakanlığı .
halojenasyon
İlavesi , flor , klor ve brom C oluşur 60 .
Flor atomu Cl ise, bir 1,2-ilave edilmesi için yeteri kadar küçük olan 2 ve Br 2 uzaktan Cı atomu eklenti nedeniyle sterik faktörler . Örneğin, C 60 Br 8 ve C 60 Br 24 , Br atomunun her biri diğerine göre 1,3- ya da 1,4-pozisyonda bulunmaktadır.
Çeşitli koşullar altında C halojene türevleri, geniş bir sayısı 60 , diğer olası olanları üzerindeki bir ya da iki izomer üzerinde olağanüstü seçiciliği olan bazı üretilebilir.
Flor ve klor ilavesi genellikle C 60 çerçevesinin tambur şeklinde bir molekül halinde düzleşmesiyle sonuçlanır .
Oksijen atomlarının eklenmesi
C çözeltileri 60 için oksijenli edilebilir epoksit C 60 ° C O. ozonlama 60 257K bir ara ozonid C verir 1,2-ksilen içinde 60 O 3 C 2 formları halinde ayrıştırılabilir, 60 ° C O. Ayrıştırma 60 O 3 296'da K epoksit verir, ama fotoliz O atomunun, bir 5,6-kenar köprüleyen bir ürün elde edilir.
Cycloadditions
Diels-Alder reaksiyonu genel olarak fonksiyonel hale C'ye kullanılır 60 . C reaksiyonu 60 uygun ikame edilmiş dien ile karşılık gelen katılma ürünü verir.
C arasında Diels-Alder reaksiyonu 60 ve 3,6-diaril-1,2,4,5-tetrazinler tanıyor C 62 . C 62 , dört üyeli bir halkanın dört altı üyeli halka ile çevrelendiği bir yapıya sahiptir.
Cı- 60 molekülleri aynı zamanda, bir [2 + 2] ile bağlanabilmektedir siklo dambıl-şekilli bileşik C vererek 120 . Bağlantı, C 60'ın katalitik miktarda KCN ile yüksek hızlı titreşimli öğütülmesiyle elde edilir . Reaksiyon, Cı gibi tersine çevrilebilir olan 120 ayırdığını iki ° C'ye geri 60 (350 ° F, 177 ° C) 450 K sıcaklıkta ısıtıldığında molekülleri. Yüksek basınç ve sıcaklık altında, C arasında değişen [2 + 2] siklo tekrar 60 polimerize fulleren zincirleri ve ağlar ile sonuçlandığını göstermektedir. Bu polimerler oluşturulduktan sonra ortam basıncında ve sıcaklığında stabil kalır ve oda sıcaklığının üzerinde ferromanyetik olma gibi oldukça ilginç elektronik ve manyetik özelliklere sahiptir .
Serbest radikal reaksiyonlar
C Reaksiyonlar 60 ile serbest radikallerin kolaylıkla meydana gelir. Cı zaman 60 disülfit RSSR radikal Cı ile karıştırılır 60 SR • kendiliğinden karışımın ışıma üzerine formları.
Cı radikal türleri stabilitesi 60 Y'nin • büyük ölçüde bağlıdır sterik faktörler zaman Y'nin tert- butil bromid olduğu, fotolizlendi ve C ile reaksiyona girmesine izin 60 , bir tersinir arası kafes Cı-C bağı oluşturulur:
Siklopropanasyon (Bingel reaksiyonu)
Siklopropanlama ( Bingel Reaksiyon C) işlevselleştirilmesi için bir başka yaygın yöntemdir 60 . C 60'ın siklopropanasyonu, çoğunlukla sterik faktörlerden dolayı 2 altıgenin birleşme yerinde meydana gelir.
İlk siklopropanasyon C β-bromomalonat muamele ile gerçekleştirilmiştir 60 , bir baz varlığında reaksiyona sokulur. Siklopropanasyon, diazometanlarla da kolayca meydana gelir . Örneğin, kolayca C difenildiazometan reaksiyona girerek 60 bileşik C verecek şekilde 61 Ph 2 . Fenil-Cı- 61 -butirik asit metil ester, siklopropanasyon kullanım için çalışılmıştır ile türev hazırlandı organik güneş hücreleri .
Redoks reaksiyonları – C 60 anyonları ve katyonları
Cı- 60 anyonlar
LUMO C 60 ile, üç kat dejenere HOMO - LUMO ayrılması nispeten küçük. Bu küçük boşluk, fullerid anyonlarına yol açan hafif potansiyellerde C 60 azalmasının meydana gelmesi gerektiğini düşündürür , [C 60 ] n − ( n = 1–6). Buckminsterfullerenin ve anyonlarının 1-elektron indirgenmesinin orta nokta potansiyelleri aşağıdaki tabloda verilmiştir:
| 213 K'da C 60'ın indirgenme potansiyeli | |
|---|---|
| yarı reaksiyon | E ° (D) |
| C 60 + e - ⇌ C- 60 |
-0,169 |
|
C- 60+ e - ⇌ C2− 60 |
-0.599 |
|
C2− 60+ e - ⇌ C3− 60 |
-1.129 |
|
C3− 60+ e - ⇌ C4− 60 |
-1.579 |
|
C4− 60+ e - ⇌ C5− 60 |
−2.069 |
|
C5− 60+ e - ⇌ C6− 60 |
-2.479 |
Cı- 60 şekilleri çeşitli yük transferi kompleksleri , örneğin, tetrakis (dimetilamino) etilen :
- C 60 + C 2 (NMe 2 ) 4 → [C 2 (NMe 2 ) 4 ] + [C 60 ] -
Bu tuz , 16 K'da ferromanyetizma sergiler .
Cı- 60 katyonları
C 60 zorlukla oksitlenir. Ultra-kuru metilen klorür ve [ n Bu 4 N] [AsF 6 ] gibi son derece yüksek oksidasyon direncine ve düşük nükleofiliteye sahip bir destekleyici elektrolit ile döngüsel voltametri kullanılarak üç tersinir oksidasyon prosesi gözlemlenmiştir .
| Düşük sıcaklıklarda C 60 oksidasyonunun indirgeme potansiyelleri | |
|---|---|
| yarı reaksiyon | E ° (D) |
| C 60 ⇌ C+ 60 |
+1.27 |
|
C+ 60⇌ C2+ 60 |
+1.71 |
|
C2+ 60⇌ C3+ 60 |
+2.14 |
Metal kompleksleri
C 60 , daha yaygın alkenlere benzer kompleksler oluşturur. Kompleksler molibden , tungsten , platin , paladyum , iridyum ve titanyum olarak rapor edilmiştir . Pentakarbonil türleri fotokimyasal reaksiyonlarla üretilir .
- M(CO) 6 + C 60 → M( η 2 -C 60 )(CO) 5 + CO (M = Mo, W)
Platin kompleksi durumunda, kararsız etilen ligandı, bir termal reaksiyonda ayrılan gruptur:
- Pt( η 2 -C 2 H 4 )(PPh 3 ) 2 + C 60 → Pt( η 2 -C 60 )(PPh 3 ) 2 + C 2 H 4
Titanosen kompleksleri de bildirilmiştir:
- ( η 5 - Cp ) 2 Ti( η 2 -(CH 3 ) 3 SiC≡CSi(CH 3 ) 3 ) + C 60 → ( η 5 -Cp) 2 Ti( η 2 -C 60 ) + (CH 3 ) 3 SiC≡CSi(CH 3 ) 3
C 60 ile eklentiler için Vaska kompleksi gibi eşgüdümlü doymamış öncüler :
- trans -Ir(CO)Cl(PPh 3 ) 2 + C 60 → Ir(CO)Cl( η 2 -C 60 )(PPh 3 ) 2
Böyle bir iridyum kompleksi, [Ir( η 2 -C 60 )(CO)Cl(Ph 2 CH 2 C 6 H 4 OCH 2 Ph) 2 ], metal merkezin birbirini kucaklayan iki elektronca zengin 'kol' yansıttığı yerde hazırlanmıştır. C 60 konuğu.
Endohedral fullerenler
Metal atomu veya H gibi bazı küçük moleküller, 2 ve soy gaz Cı içinde kapsüllenebilir 60 kafes. Bu endohedral fullerenler genellikle bir ark reaktöründe metal atomlarında doping veya lazer buharlaştırma ile sentezlenir. Bu yöntemler, düşük endohedral fulleren verimleri verir ve daha iyi bir yöntem, kafesin açılmasını, atomlar veya moleküllerde paketlenmesini ve belirli organik reaksiyonlar kullanılarak açıklığın kapatılmasını içerir . Ancak bu yöntem henüz olgunlaşmamıştır ve sadece birkaç tür bu şekilde sentezlenmiştir.
Endohedral fullerenler, kapsüllenmiş atom veya molekülün yanı sıra fullerenin kendisinden tamamen farklı olabilen farklı ve ilgi çekici kimyasal özellikler gösterir. Kapsüllenmiş atomların C 60 kafesi içinde dairesel hareketler gerçekleştirdiği gösterilmiştir ve hareketi NMR spektroskopisi kullanılarak takip edilmiştir .
Teknolojideki potansiyel uygulamalar
C 60'ın optik absorpsiyon özellikleri, güneş tayfı ile eşleşir, bu da C 60 bazlı filmlerin fotovoltaik uygulamalar için faydalı olabileceğini düşündürür. Yüksek elektronik afinitesi nedeniyle verici/alıcı tabanlı güneş pillerinde kullanılan en yaygın elektron alıcılarından biridir. C 60 –polimer hücrelerinde %5.7'ye varan dönüşüm verimlilikleri rapor edilmiştir .
Sağlıkta potansiyel uygulamalar
Yutma ve riskler
C 60 ışığa duyarlıdır, bu nedenle C 60'ı ışığa maruz bırakmak, bozulmasına ve tehlikeli hale gelmesine neden olur. Işığa maruz kalmış C 60 solüsyonlarının yutulması kanser (tümör) gelişmesine yol açabilir. Bu nedenle, C 60 ürünlerinin insan tarafından yutulmasına yönelik yönetimi, çok karanlık ortamlarda detaylandırma, büyük opaklığa sahip şişelere yerleştirme ve karanlık yerlerde saklama ve düşük ışık koşullarında tüketim ve sorunlar hakkında uyarmak için etiketler kullanma gibi dikkatli önlemler gerektirir. ışıkla.
Zeytinyağı veya suda çözünen C 60 çözeltilerinin, ışıktan korundukları sürece kemirgenler için toksik olmadığı bulunmuştur.
Aksi takdirde, bir çalışma, C 60'ın vücutta normalden daha uzun süre, özellikle birikme eğiliminde olan karaciğerde kaldığını ve bu nedenle zararlı sağlık etkilerine neden olma potansiyeline sahip olduğunu buldu.
C60 içeren yağlar ve riskler
2011-2012 yıllarında yapılan bir deneyde, sıçanlara zeytinyağında C 60 solüsyonu uygulandı ve yaşam sürelerinin önemli ölçüde uzaması sağlandı. O zamandan beri, C 60'lı birçok yağ, antioksidan ürünler olarak satıldı, ancak bu, onları toksik hale getirebilecek ışığa duyarlılık sorununu ortadan kaldırmaz. Daha sonraki bir araştırma, ışığa maruz kalmanın yağdaki C 60 çözeltilerini bozduğunu , onu toksik hale getirdiğini ve tüketildikten sonra kanser (tümör) geliştirme riskinde 'büyük' bir artışa yol açtığını doğruladı .
Işığın etkisiyle bozulmayı önlemek için, C 60 yağlarının çok karanlık ortamlarda yapılması, büyük opaklığa sahip şişelere doldurulması ve karanlıkta tutulması, ayrıca düşük ışık koşullarında tüketilmeye uygun olması ve uyarı için etiketler kullanılması gerekir. C 60 için ışığın tehlikeleri .
Bazı üreticiler, yağlarla ilgili olası sorunlardan kaçınmak için C 60'ı suda çözmeyi başarmışlardır , ancak bu, C 60'ı ışıktan korumaz , dolayısıyla aynı önlemlere ihtiyaç vardır.
Referanslar
bibliyografya
- Katz, EA (2006). "Fullerene İnce Filmler Fotovoltaik Malzeme Olarak" . Soga'da, Tetsuo (ed.). Güneş enerjisi dönüşümü için nanoyapılı malzemeler . Elsevier. s. 361-443. ISBN'si 978-0-444-52844-5.
daha fazla okuma
- Kroto, HW; Heath, JR; O'Brien, SC; Kıvrılma, RF; Smalley, RE (Kasım 1985). "C 60 : Buckminsterfullerene". Doğa . 318 (14): 162-163. Bibcode : 1985Natur.318..162K . doi : 10.1038/318162a0 . S2CID 4314237 .- C 60'ın orijinal keşfini anlatan
- Hebgen, Peter; Goel, Anish; Howard, Jack B.; Rainey, Lenore C.; Vander Sande, John B. (2000). "Difüzyon Alevlerinde Fullerenler ve Nanoyapılar" (PDF) . Yanma Enstitüsü Tutanakları . 28 : 1397–1404. CiteSeerX 10.1.1.574.8368 . doi : 10.1016/S0082-0784(00)80355-0 .– 2000 yılında 28. Uluslararası Yanma Sempozyumunda yayınlanan yanma araştırması ile C 60 sentezini açıklayan rapor
Dış bağlantılar
- Bristol Üniversitesi Kimya Bölümü tarafından gerçekleştirilen C 60'ın keşfinin tarihçesi
- Wisconsin-Madison Üniversitesi tarafından açıklanan buckminsterfullerene kısa bir genel bakış
- Ming Kai Koleji tarafından buckminsterfullerenin özelliklerini detaylandıran bir rapor
- Donald R. Huffman ve C sentezine ilişkin Wolfgang Krätschmer kağıt 60 içinde Nature , 1990 yılında yayınlanan
- Oak Ridge Ulusal Laboratuvarı tarafından C 60'ın kapsamlı bir açıklaması
- Connexions Science Encyclopaedia'da buckminsterfullerene hakkında bir makale
- Buckminsterfullerenin sayısal nicel özellikleri hakkında Sussex Üniversitesi tarafından derlenen kapsamlı istatistiksel veriler
- Bristol Üniversitesi tarafından yazılan ve desteklenen buckminsterfullerene adanmış bir web portalı
- Bristol Üniversitesi Kimya Bölümü tarafından yazılan ve desteklenen buckminsterfullerene adanmış başka bir web portalı
- Tamamen C 60'a ve keşfine, yapısına, üretimine, özelliklerine ve uygulamalarına ayrılmış kısa bir makale
- American Chemical Society'nin buckminsterfullerene ile ilgili tam makalesi
- Buckminsterfullerene , Videoların Periyodik Tablosunda (Nottingham Üniversitesi)