Azimut kuantum sayısı - Azimuthal quantum number

| hakkında bir dizi makalenin bir parçası |
| Kuantum mekaniği |
|---|
Azimut kuantum sayısı a, kuantum sayısı bir için yörüngeler olarak belirleyen bir yörüngesel açısal momentumu ve orbital şeklini tarif etmektedir. Azimut kuantum sayısı benzersiz tarif kuantum sayısı bir dizi ikinci kuantum durumu bir elektronun (diğerleri temel kuantum sayısı , manyetik kuantum sayısı ve dönüş kuantum sayısı ). Bu da bilinir yörüngesel açısal momentum kuantum sayısı, yörünge kuantum sayısı ya da ikinci kuantum sayısı ve olarak sembolize edilen ℓ (belirgin ell ).
türetme
Atomun elektronlarının enerji durumlarıyla bağlantılı dört kuantum sayısı vardır: n , ℓ , m ℓ ve m s . Bunlar , bir atomdaki tek bir elektronun tam, benzersiz kuantum durumunu belirtir ve onun dalga fonksiyonunu veya yörüngesini oluşturur . Dalga fonksiyonunu elde etmek için çözerken, Schrödinger denklemi ilk üç kuantum sayısına yol açan üç denkleme indirgenir. Bu nedenle, ilk üç kuantum sayısının denklemlerinin tümü birbiriyle ilişkilidir. Azimut kuantum sayısı, dalga denkleminin kutupsal kısmının çözümünde, aşağıda gösterildiği gibi, genellikle en iyi şekilde küresel simetriye sahip modellerle çalışan küresel koordinat sistemine bağlı olarak ortaya çıktı .
Bir atom elektron var açısal momentum , L , kendi kuantum sayısı ile ilgilidir ℓ aşağıdaki denklemle:
burada ħ olan düşük Planck sabitesi , L 2 yörüngesel açısal momentum operatörü ve elektron dalga fonksiyonu olan. Kuantum sayısı ℓ her zaman negatif olmayan bir tamsayıdır: 0, 1, 2, 3, vb. L' nin açısal momentum operatörü olarak kullanılması dışında gerçek bir anlamı yoktur . Açısal momentumdan bahsederken, sadece kuantum sayısını ℓ kullanmak daha iyidir .
Atomik orbitaller, harflerle gösterilen farklı şekillere sahiptir. Çizimde, s , p ve d harfleri ( spektroskopiden kaynaklanan bir kural ) atomik yörüngenin şeklini tanımlar .
Dalga fonksiyonları küresel harmonikler şeklini alır ve Legendre polinomları tarafından tanımlanır . Farklı ℓ değerleriyle ilgili çeşitli yörüngelere bazen alt kabuklar denir ve aşağıdaki gibi küçük Latin harfleriyle (tarihsel nedenlerle seçilmiştir) adlandırılır:
Azimut kuantum sayısı için kuantum alt kabukları Azimut
sayısı ( ℓ )tarihi
mektupMaksimum
elektronTarihsel
isimŞekil 0 s 2 s arp küresel 1 P 6 p rincipal üç dambıl şeklinde polar hizalı yörünge; x, y ve z'nin her kutbunda bir lob (+ ve − eksenleri) 2 NS 10 d iffuse dokuz dambıl ve bir çörek (veya "benzersiz şekil #1" , küresel harmoniklerin bu resmine bakın , üçüncü sıra merkez ) 3 F 14 f undamental “benzersiz şekil #2” ( küresel harmoniklerin bu resmine bakın , alt sıra orta ) 4 G 18 5 H 22 6 ben 26 f alt kabuğundan sonraki harfler , j harfi ve halihazırda kullanılanlar hariç, alfabetik sırayla f harfini takip eder .
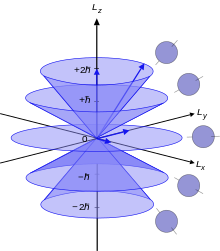
Farklı açısal momentum durumlarının her biri 2(2 ℓ + 1) elektron alabilir. Bu üçüncü kuantum sayısı çünkü m ℓ (gevşek bir şekilde düşünülebilir nicelenmiş z ekseni açısal momentumun vektörünün projeksiyon) çalışır - ℓ için ℓ tamsayı birimlerinde ve böylece 2 vardır ℓ + 1, mümkün devletler. Her farklı n , ℓ , m ℓ orbitali, karşıt spinlere sahip (kuantum sayısı m s = ±½ ile verilen) iki elektron tarafından işgal edilebilir ve toplamda 2(2 ℓ + 1) elektron verir. Tabloda verilenden daha yüksek ℓ değerine sahip orbitallere kesinlikle izin verilir, ancak bu değerler şimdiye kadar keşfedilen tüm atomları kapsar.
Ana kuantum sayısının belirli bir değeri için n , olası ℓ değerleri 0 ile n − 1 arasında değişir ; bu nedenle, n = 1 kabuğu yalnızca bir s alt kabuğuna sahiptir ve yalnızca 2 elektron alabilir, n = 2 kabuğu bir s ve bir p alt kabuğuna sahiptir ve toplamda 8 elektron alabilir, n = 3 kabuğu s , p ve d'ye sahiptir alt kabuklar ve maksimum 18 elektrona sahiptir, vb.
Bir basit bir elektron modeli ile sonuçlanır enerji düzeyleri , tek başına temel sayısına bağlı olarak. Daha karmaşık atomlarda, bu enerji seviyeleri tüm n > 1 için bölünür ve daha yüksek ℓ durumlarını düşük ℓ durumlarının üzerine yerleştirir . Örneğin, 2p'nin enerjisi 2s'den daha yüksektir, 3d, 3p'den daha yüksek oluşur, bu da 3s'nin üzerindedir, vb. Bu etki sonunda periyodik tablonun blok yapısını oluşturur. Bilinen hiçbir atom , temel durumunda üçten ( f ) daha yüksek ℓ değerine sahip bir elektrona sahip değildir .
Açısal momentum kuantum sayısı, ℓ , çekirdekten geçen düzlemsel düğümlerin sayısını yönetir. Düzlemsel bir düğüm, elektromanyetik dalgada tepe ve çukur arasındaki orta nokta olarak tanımlanabilir ve sıfır büyüklükleri vardır. Bir s yörüngesinde, çekirdekten hiçbir düğüm geçmez, bu nedenle karşılık gelen azimut kuantum sayısı ℓ 0 değerini alır. Bir p yörüngesinde, bir düğüm çekirdeği geçer ve bu nedenle ℓ , 1 değerine sahiptir .
n değerine bağlı olarak , bir açısal momentum kuantum sayısı ℓ ve aşağıdaki seri vardır. Listelenen dalga boyları bir hidrojen atomu içindir :
- , Lyman serisi (ultraviyole)
- , Balmer serisi (görünür)
- , Ritz–Paschen serisi ( yakın kızılötesi )
- , Brackett serisi ( kısa dalga boyu kızılötesi )
- , Pfund serisi ( orta dalga boyu kızılötesi ).
Kuantize açısal momentumun eklenmesi
İki ayrı nicelenmiş açısal momentumun toplamı olan nicelenmiş bir toplam açısal momentum verildiğinde ve ,
kuantum sayısı , büyüklüğü ile bağlantılı arasında olabilir için tamsayıdır adımda ve tek tek açısal momentumun büyüklüklerinin tekabül kuantum sayılardır.
Atomdaki bir elektronun toplam açısal momentumu

Nedeniyle spin-yörünge etkileşimi atomunda, yörünge açısal momentumu artık sırabağımsızdır ile Hamiltoniyenin , ne yapar dönüşünü . Bu nedenle bunlar zamanla değişir. Ancak toplam açısal momentum J tek elektronlu Hamiltoniyen ile değişir ve bu nedenle sabittir. J ile tanımlanır
L olmanın yörüngesel açısal momentum ve S sıkma. Toplam açısal momentum , yörünge açısal momentum ile aynı komütasyon ilişkilerini sağlar , yani
aşağıdakilerden
burada J i , J x , J y ve J z'yi temsil eder .
Zaman içinde sabit olan sistemi tanımlayan kuantum sayıları şimdi j ve m j olup, J'nin dalga fonksiyonu üzerindeki etkisi ile tanımlanır.
Böylece j , toplam açısal momentumun normuyla ve m j , belirli bir eksen boyunca izdüşümüyle ilişkilidir . J sayısı için özel bir öneme sahip olan göreli kuantum kimyasında genelde simge in özelliğine sahip, elektron konfigürasyonu süper ağır elemanları .
Kuantum mekaniğindeki herhangi bir açısal momentumda olduğu gibi , J'nin diğer eksenler boyunca izdüşümü J z ile birlikte tanımlanamaz , çünkü bunlar değişmez.
Yeni ve eski kuantum sayıları arasındaki ilişki
j ve m, j , birlikte parite bir kuantum halde , üç yerine kuantum sayıları ℓ , m ℓ ve m s (izdüşümü bir dönüş belirtilen bir eksen boyunca). Önceki kuantum sayıları ikincisiyle ilişkilendirilebilir.
Ayrıca, özvektörler ve j , s , m, j da ve parite, özvektörler ve Hamiltoniyen'in , doğrusal kombinasyonları olan özvektörler ve ℓ , s , m, ℓ ve m, s .
açısal momentum kuantum sayılarının listesi
- İçsel (veya spin) açısal momentum kuantum sayısı veya basitçe spin kuantum sayısı
- yörünge açısal momentum kuantum sayısı (bu makalenin konusu)
- manyetik kuantum sayısı , yörünge momentumu kuantum sayısıyla ilgili
- toplam açısal momentum kuantum sayısı
Tarih
Azimut kuantum sayısı, atomun Bohr modelinden alındı ve Arnold Sommerfeld tarafından belirlendi . Bohr modeli, atomun Rutherford atom modeli ile kombinasyon halinde spektroskopik analizinden türetilmiştir . En düşük kuantum seviyesinin sıfır açısal momentuma sahip olduğu bulundu. Sıfır açısal momentuma sahip yörüngeler, bir boyutta salınan yükler olarak kabul edildi ve bu nedenle "sarkaç" yörüngeleri olarak tanımlandı, ancak doğada bulunamadı. Üç boyutlu olarak yörüngeler , (en düşük enerjili durumda) büyük bir daire içinde salınan bir atlama ipine benzer şekilde, çekirdeği geçen herhangi bir düğüm olmaksızın küresel hale gelir .
Ayrıca bakınız
- açısal momentum operatörü
- Kuantum mekaniğine giriş
- Küresel simetrik potansiyelde parçacık
- açısal momentum kuplajı
- Clebsch-Gordan katsayıları
Referanslar
- ^ Eisberg, Robert (1974). Atomların, Moleküllerin, Katıların, Çekirdeklerin ve Parçacıkların Kuantum Fiziği . New York: John Wiley & Sons Inc. s. 114-117. ISBN'si 978-0-471-23464-7.
- ^ RB Lindsay (1927). "Atomik modellerde "sarkaç" yörüngeleri üzerine not" . Proc. Natl. Acad. Sci . 13 (6): 413–419. Bibcode : 1927PNAS...13..413L . doi : 10.1073/pnas.13.6.413 . PMC 1085028 . PMID 16587189 .





















![[J_i, J_j ] = i \hbar \epsilon_{ijk} J_k](https://wikimedia.org/api/rest_v1/media/math/render/svg/1c774fd99fb91eb8937cbaaa6b6af2eaf88e7ad6)
![\sol[J_i, J^2 \sağ] = 0](https://wikimedia.org/api/rest_v1/media/math/render/svg/df773fc4aa955999fbf21070fb2d56ae4252b0ef)

