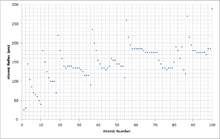
Atom yarıçapı - Atomic radius
Atomik yarıçap a kimyasal element de büyüklüğünün bir ölçüsüdür atomu , merkezinden genellikle ortalama veya tipik mesafe çekirdeği çevreleyen sınırına kabukları arasında elektron . Sınır, iyi tanımlanmış bir fiziksel varlık olmadığından, atom yarıçapının eşdeğer olmayan çeşitli tanımları vardır. Atom yarıçapının yaygın olarak kullanılan dört tanımı şunlardır: Van der Waals yarıçapı , iyonik yarıçap , metalik yarıçap ve kovalent yarıçap . Tipik olarak, yarıçaplarını ayrı ayrı ölçmek için atomları izole etmenin zorluğu nedeniyle, atom yarıçapı kimyasal olarak bağlı bir durumda ölçülür; ancak teorik hesaplamalar, atomları ayrı ayrı ele aldığında elbette daha basittir. Çevreye, araştırmaya ve duruma olan bağımlılıklar çok sayıda tanımlamaya yol açar.
Tanıma bağlı olarak, terim atomlar için geçerli olabilir yoğun madde , kovalent bağlanması olarak moleküller , ya da iyonize ve uyarılmış hal ; ve değeri deneysel ölçümlerle elde edilebilir veya teorik modellerden hesaplanabilir. Yarıçapın değeri atomun durumuna ve bağlamına bağlı olabilir.
Elektronların belirli yörüngeleri veya kesin olarak tanımlanmış aralıkları yoktur. Bunun yerine, konumları , keskin bir kesme olmaksızın çekirdekten uzaklaştıkça kademeli olarak azalan olasılık dağılımları olarak tanımlanmalıdır ; bunlara atomik orbitaller veya elektron bulutları denir . Ayrıca, yoğun madde ve moleküllerde, atomların elektron bulutları genellikle bir dereceye kadar örtüşür ve elektronların bazıları iki veya daha fazla atomu kapsayan geniş bir bölge üzerinde dolaşabilir.
Çoğu tanım altında, izole edilmiş nötr atomların yarıçapları 30 ila 300 pm ( bir metrenin trilyonda biri) veya 0,3 ila 3 angström arasında değişir . Bu nedenle, bir atomun yarıçapı, çekirdeğinin yarıçapının (1-10 fm ) 10.000 katından fazladır ve görünür ışığın (400-700 nm ) dalga boyunun 1/1000'inden azdır .
Birçok amaç için atomlar küreler olarak modellenebilir. Bu yalnızca kaba bir tahmindir, ancak sıvıların ve katıların yoğunluğu , sıvıların moleküler eleklerden difüzyonu , kristallerdeki atom ve iyonların düzenlenmesi ve boyut ve şekil gibi birçok fenomen için nicel açıklamalar ve tahminler sağlayabilir. moleküllerin .
Tarih
1920'de, X-ışını kristalografisini kullanarak atomların boyutlarını belirlemenin mümkün hale gelmesinden kısa bir süre sonra , aynı elementin tüm atomlarının aynı yarıçapa sahip olduğu öne sürüldü. Bununla birlikte, 1923'te, daha fazla kristal verisi elde edildiğinde, bir atomun bir küre olarak yaklaşımının, aynı atomu farklı kristal yapılarda karşılaştırırken mutlaka geçerli olmadığı bulundu.
Tanımlar
Atom yarıçapının yaygın olarak kullanılan tanımları şunları içerir:
- Van der Waals yarıçapı : En basit tanımıyla, kovalent veya metalik etkileşimlerle başka şekilde bağlı olmayan elementin iki atomunun çekirdekleri arasındaki minimum mesafenin yarısı. Van der Waals yarıçapı, Van der Waals kuvvetlerinin diğer etkileşimlerin baskın olduğu elementler (metaller gibi) için bile tanımlanabilir. Çünkü Van Waals der etkileşimleri atom polarizasyon kuantum dalgalanmaların ortaya , (genellikle daha kolay bir şekilde ölçülebilir veya hesaplanabilir) polarisability yarıçapı dolaylı Waals der Van tanımlamak için kullanılabilir.
- İyonik yarıçap : Belirli bir iyonizasyon durumundaki bir elementin iyonlarının, o iyonu içeren kristal tuzlardaki atom çekirdeklerinin aralığından çıkarılan nominal yarıçapı. Prensip olarak, iki bitişik karşıt yüklü iyonlar arasındaki aralık ( uzunluk arasında iyonik bağ aralarında) iyonik yarıçaplarının toplamına eşit olmalıdır.
- Kovalent yarıçap : Bir elementin atomlarının, diğer atomlara kovalent olarak bağlandığında , moleküllerdeki atom çekirdekleri arasındaki ayrımdan çıkarsanan nominal yarıçapı . Prensipte, bir molekülde birbirine bağlı iki atom arasındaki mesafe (bu kovalent bağın uzunluğu), kovalent yarıçaplarının toplamına eşit olmalıdır.
- Metalik yarıçap : Bir elementin atomlarının diğer atomlara metalik bağlarla birleştirildiğinde nominal yarıçapı .
- Bohr yarıçapı : Atomun Bohr modeli (1913) tarafından tahmin edilen en düşük enerjili elektron yörüngesinin yarıçapı . Yalnızca hidrojen , tek iyonize helyum ve pozitronyum gibi tek elektronlu atomlara ve iyonlara uygulanabilir . Model artık modası geçmiş olmasına rağmen, hidrojen atomu için Bohr yarıçapı hala önemli bir fiziksel sabit olarak kabul edilmektedir.
Ampirik olarak ölçülen atom yarıçapı
Aşağıdaki tablo, 1964'te JC Slater tarafından yayınlandığı gibi, elementler için ampirik olarak ölçülen kovalent yarıçapları göstermektedir . Değerler , yaklaşık 5 pm doğrulukla pikometre (pm veya 1×10 −12 m) cinsindendir . Yarıçap arttıkça kutunun gölgesi kırmızıdan sarıya değişir; gri, veri eksikliğini gösterir.
|
Grup (sütun) |
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |||
|
Nokta (satır) |
|||||||||||||||||||||
| 1 |
H 25 |
o |
|||||||||||||||||||
| 2 |
Li 145 |
Be 105 |
B 85 |
Cı- 70 |
K 65 |
O 60 |
F 50 |
Ne |
|||||||||||||
| 3 |
Na 180 |
mg 150 |
Al 125 |
Si 110 |
S 100 |
S 100 |
cl 100 |
Ar |
|||||||||||||
| 4 |
K 220 |
yaklaşık 180 |
sc 160 |
Ti 140 |
V 135 |
Cr 140 |
Mn 140 |
Fe 140 |
Co 135 |
Ni 135 |
Cu 135 |
çinko 135 |
ga 130 |
Ge 125 |
As 115 |
Se 115 |
br 115 |
Kr |
|||
| 5 |
Rb 235 |
Sr 200 |
Y, 180 |
Zr 155 |
nb 145 |
Pzt 145 |
Tc 135 |
130 Rupi |
Rh 135 |
Yüz 140 |
Ag 160 |
Cd 155 |
155 yılında |
Sn 145 |
Sb 145 |
Te 140 |
ben 140 |
Xe |
|||
| 6 |
Cs 260 |
Ba 215 |
* |
Lu 175 |
Hf 155 |
Ta 145 |
W 135 |
Yeniden 135 |
OS 130 |
Ir 135 |
Bölüm 135 |
Au 135 |
Hg 150 |
190 TL |
Pb 180 |
160 Bi |
Po 190 |
NS |
Rn |
||
| 7 |
Cum |
Ra 215 |
** |
lr |
Rf |
db |
Çavuş |
bh |
hs |
dağ |
Ds |
Rg |
Müşteri |
Nh |
fl |
Mc |
Sv. |
Ts |
og |
||
| * |
La 195 |
MS 185 |
Pr 185 |
Nd 185 |
öğleden sonra 185 |
Sm 185 |
AB 185 |
Gd 180 |
TB 175 |
dy 175 |
Ho 175 |
Er 175 |
tm 175 |
Yb 175 |
|||||||
| ** |
Ac 195 |
th 180 |
Pa 180 |
U 175 |
np 175 |
Pu 175 |
Am 175 |
Santimetre |
bk |
bkz. |
Es |
FM |
md |
Numara |
|||||||
Genel eğilimlerin açıklaması
Atom yarıçapının artan atom numarasına göre değişme şekli, elektronların sabit kapasiteli kabuklarda düzenlenmesiyle açıklanabilir. Negatif yüklü elektronlar çekirdekteki pozitif yüklü protonlar tarafından çekildiğinden , kabuklar genellikle artan yarıçapa göre doldurulur . Periyodik tablonun her satırı boyunca atom numarası arttıkça, ek elektronlar aynı en dış kabuğa girer; artan nükleer yük nedeniyle yarıçapı yavaş yavaş daralır. Soy gazda en dıştaki kabuk tamamen doludur; bu nedenle, bir sonraki alkali metalin ek elektronu, atom yarıçapındaki ani artışı hesaba katarak bir sonraki dış kabuğa gidecektir.
Artan nükleer yük, kalkanlama olarak bilinen bir fenomen olan artan elektron sayısıyla kısmen dengelenir ; bu da atomların boyutunun neden genellikle her sütunda arttığını açıklıyor. Bununla birlikte, lantanit büzülmesi olarak bilinen dikkate değer bir istisna vardır : 5d element bloğu, 4f elektronlarının zayıf koruması nedeniyle beklenenden çok daha küçüktür.
Esasen, artan proton sayısı nedeniyle atom yarıçapı periyotlar boyunca azalır. Bu nedenle, protonlar ve elektronlar arasında daha büyük bir çekim vardır, çünkü zıt yükler çeker ve daha fazla proton daha güçlü bir yük oluşturur. Daha büyük çekim, elektronları protonlara yaklaştırır ve parçacığın boyutunu azaltır. Bu nedenle, atom yarıçapı azalır. Gruplarda aşağı doğru atom yarıçapı artar. Bunun nedeni, daha fazla enerji seviyesinin olması ve dolayısıyla protonlar ve elektronlar arasında daha büyük bir mesafe olmasıdır. Ek olarak, elektron koruması çekimin azalmasına neden olur, böylece kalan elektronlar pozitif yüklü çekirdekten daha uzağa gidebilir. Bu nedenle, boyut veya atom yarıçapı artar.
Aşağıdaki tablo, bir elementin atom yarıçapını etkileyen ana olayları özetlemektedir:
| faktör | prensip | ile arttır... | eğilimi | yarıçap üzerindeki etkisi |
|---|---|---|---|---|
| elektron kabukları | Kuantum mekaniği | asal ve azimut kuantum sayıları | her sütunu aşağı artır | atom yarıçapını arttırır |
| nükleer yük | çekirdekteki protonlar tarafından elektronlara etki eden çekici kuvvet | atomik numara | her dönem boyunca artış (soldan sağa) | atom yarıçapını azaltır |
| kalkan | iç elektronlar tarafından en dış kabuk elektronlarına etki eden itici kuvvet | iç kabuklardaki elektron sayısı | 2. faktörün etkisini azaltmak | atom yarıçapını arttırır |
lantanit kasılma
4f- elektronlar alt kabuğa kademeli doldurulan, lantan ( Z için = 57) iterbiyum ( Z = 70), alt kabuklar daha fazla dışarı doğru artan çekirdek yükü koruma özellikle etkili değildir. Lantanitleri hemen takip eden elementler, beklenenden daha küçük ve hemen üstlerindeki elementlerin atom yarıçaplarıyla neredeyse aynı olan atom yarıçaplarına sahiptir. Bu nedenle lutetyum biraz daha küçük aslında itriyum , hafniyum olarak hemen hemen aynı atom çapındaki (ve kimya) sahip olan zirkonyum ve tantal benzer bir atom yarıçapa sahiptir niobium ve benzeri. Lantanid büzülmesinin etkisi platine ( Z = 78) kadar fark edilir , bundan sonra eylemsiz çift etkisi olarak bilinen göreli bir etkiyle maskelenir .
Lantanit kasılması nedeniyle, aşağıdaki 5 gözlem çizilebilir:
- Ln 3+ iyonlarının boyutu atom numarası ile düzenli olarak azalır. Fajans kurallarına göre , Ln 3+ iyonlarının boyutundaki azalma , kovalent karakteri arttırır ve Ln(OH) 3'teki Ln 3+ ve OH − iyonları arasındaki temel karakteri , Yb(OH) 3 ve Lu( ) noktasına kadar azaltır. OH) 3 , sıcak konsantre NaOH içinde zorlukla çözülebilir. Dolayısıyla Ln 3+' nın büyüklük sırası verilmiştir: La 3+ > Ce 3+ > ..., ... > Lu 3+ .
- İyonik yarıçaplarında düzenli bir azalma var.
- Atom numarasındaki artışla birlikte indirgeyici ajan olarak hareket etme eğilimlerinde düzenli bir azalma vardır.
- D-blok geçiş elemanlarının ikinci ve üçüncü sıraları özellik olarak oldukça yakındır.
- Sonuç olarak, bu elementler doğal minerallerde birlikte bulunur ve ayrılmaları zordur.
d-blok kasılması
D-blok kasılması, lantanid büzülmesinden daha az belirgindir ancak benzer bir nedenden kaynaklanır. Bu durumda, bu atom yarıçapları ve hemen ilk satır, aşağıdaki elemanları kimyaları etkiler 3d-elektron zayıf koruyucu kapasitesi geçiş metalleri arasından, galyum ( Z için = 31), brom ( Z = 35).
Hesaplanmış atom yarıçapları
Aşağıdaki tablo, 1967'de Enrico Clementi ve diğerleri tarafından yayınlanan teorik modellerden hesaplanan atom yarıçaplarını göstermektedir . Değerler pikometre (pm) cinsindendir.
|
Grup (sütun) |
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||
|
Nokta (satır) |
||||||||||||||||||||
| 1 |
H 53 |
O 31 |
||||||||||||||||||
| 2 |
Li 167 |
Be 112 |
B 87 |
C 67 |
K 56 |
O 48 |
F 42 |
38 numara |
||||||||||||
| 3 |
Na 190 |
mg 145 |
Al 118 |
Si 111 |
S 98 |
S 88 |
cl 79 |
ar 71 |
||||||||||||
| 4 |
K 243 |
yaklaşık 194 |
sc 184 |
Ti 176 |
V 171 |
Cr 166 |
Mn 161 |
Fe 156 |
Ortak 152 |
Ni 149 |
Cu 145 |
çinko 142 |
Ga 136 |
Ge 125 |
As 114 |
Se 103 |
br 94 |
88 kuruş |
||
| 5 |
Rb 265 |
Sr 219 |
Y 212 |
Zr 206 |
Not 198 |
Mo 190 |
tc 183 |
Ru 178 |
Rh 173 |
Bölüm 169 |
Ag 165 |
Cd 161 |
156 yılında |
Sn 145 |
SB 133 |
Te 123 |
ben 115 |
Xe 108 |
||
| 6 |
Cs 298 |
Ba 253 |
* |
Lu 217 |
Hf 208 |
Ta 200 |
W 193 |
Yeniden 188 |
işletim sistemi 185 |
IR 180 |
Bölüm 177 |
Au 174 |
Hg 171 |
156 TL |
Pb 154 |
Bi 143 |
Po 135 |
at 127 |
Rn 120 |
|
| 7 |
Cum |
Ra |
** |
lr |
Rf |
db |
Çavuş |
bh |
hs |
dağ |
Ds |
Rg |
Müşteri |
Nh |
fl |
Mc |
Sv. |
Ts |
og |
|
| * |
La 226 |
CE 210 |
Pr 247 |
Nd 206 |
öğleden sonra 205 |
Sm 238 |
AB 231 |
Gd 233 |
tb 225 |
dy 228 |
Ho 226 |
Er 226 |
tm 222 |
Yb 222 |
||||||
| ** |
AC |
NS |
baba |
sen |
np |
Pu |
NS |
Santimetre |
bk |
bkz. |
Es |
FM |
md |
Numara |
||||||
Ayrıca bakınız
- Elementlerin atom yarıçapları (veri sayfası)
- Kimyasal bağ
- kovalent yarıçap
- Bağ uzunluğu
- sterik engel
- Kinetik çap
Notlar
- Ampirik ve hesaplanmış veriler arasındaki fark: Ampirik veriler, "gözlem veya deneyimden kaynaklanan veya bunlara dayanan" veya "sistem ve teori verilerine gereken önemi vermeksizin yalnızca deneyime veya gözleme dayanan" anlamına gelir. Başka bir deyişle, veriler fiziksel gözlem yoluyla ölçülür ve benzer sonuçlar üreten diğer deneylerle incelenir . Hesaplanan veriler ise teorik modellerden elde edilir. Bu tür tahminler, yarıçapları deneysel olarak ölçülemeyen elementler için özellikle yararlıdır (örneğin, keşfedilmemiş veya yarı ömrü çok kısa olanlar).