Antimon trisülfür - Antimony trisulfide
|
|

|
|
| İsimler | |
|---|---|
|
IUPAC adı
diantimon trisülfid, antimon(III) sülfür
|
|
| Diğer isimler
antimon sülfür, antimon sülfür, antimon seskisülfid, antimon vermilion, siyah antimon, antimon kükürt
|
|
| tanımlayıcılar | |
|
3B model ( JSmol )
|
|
| Kimyasal Örümcek | |
| ECHA Bilgi Kartı |
100.014.285 |
|
PubChem Müşteri Kimliği
|
|
| ÜNİİ | |
|
CompTox Panosu ( EPA )
|
|
|
|
|
|
| Özellikler | |
| SB 2 S 3 | |
| Molar kütle | 339.715 |
| Dış görünüş | gri / siyah ortorombik kristal (stibnite) |
| Yoğunluk | 4.562g cm −3 ( stibnit ) |
| Erime noktası | 550 °C (1.022 °F; 823 K) (stibnit) |
| Kaynama noktası | 1.150 °C (2.100 °F; 1.420 K) |
| 0.00017 g/100 mL (18 °C) | |
| -86.0·10 −6 cm 3 /mol | |
|
Kırılma indisi ( n D )
|
4.046 |
| Termokimya | |
|
Isı kapasitesi ( C )
|
123.32 J/K mol |
|
Std
oluşum entalpisi (Δ f H ⦵ 298 ) |
-157,8 kJ/mol |
| Tehlikeler | |
| NFPA 704 (ateş elması) | |
| Ölümcül doz veya konsantrasyon (LD, LC): | |
|
LD 50 ( ortalama doz )
|
> 2000 mg/kg (sıçan, ağızdan) |
| NIOSH (ABD sağlığa maruz kalma sınırları): | |
|
PEL (İzin Verilebilir )
|
TWA 0.5 mg / m 3 (Sb gibi) |
|
REL (Önerilen)
|
TWA 0.5 mg / m 3 (Sb gibi) |
| Bağıntılı bileşikler | |
|
Diğer anyonlar
|
Antimon trioksit Antimon triselenid Antimon tellürid |
|
Diğer katyonlar
|
Arsenik trisülfid Bizmut(III) sülfür |
|
Bağıntılı bileşikler
|
antimon pentasülfid |
|
Aksi belirtilmedikçe, veriler standart durumdaki malzemeler için verilmiştir (25 °C [77 °F], 100 kPa'da). |
|
| Bilgi kutusu referansları | |
Antimon trisülfid (Sb 2 S 3 ) doğada kristalli mineral stibnit ve amorf kırmızı mineral (aslında bir mineraloid) metastibnit olarak bulunur . Güvenlik kibritlerinde , askeri mühimmatta, patlayıcılarda ve havai fişeklerde kullanılmak üzere üretilmiştir . Ayrıca yakut renkli cam üretiminde ve plastiklerde alev geciktirici olarak kullanılmaktadır. Tarihsel olarak stibnit formu, 16. yüzyılda üretilen resimlerde gri bir pigment olarak kullanılmıştır. Antimon trisülfid da görüntü hassas olarak kullanılmıştır Fotokondüktörün içinde vidikon kamera tüpleri. 1.8-2.5 eV doğrudan bant aralığına sahip bir yarı iletkendir . Uygun doping ile p ve n tipi malzemeler üretilebilir.
Hazırlık ve reaksiyonlar
Sb 2 S 3 , 500–900 °C sıcaklıktaki elementlerden hazırlanabilir:
- 2 Sb + 3 S → Sb 2 S 3
Sb 2 S 3 olduğunda çökeltilir , H 2 S Sb (III) 'ün bir solüsyonundan geçirilir. Bu reaksiyon, H köpürme, antimon saptanması için, bir gravimetrik yöntemle olarak kullanılmıştır 2 sıcak Sb (III) bileşiğinin bir çözeltisi içinden S HCI yataklarının Sb bir turuncu bir şekilde 2 S 3 , reaksiyon koşulları altında kararır.
Sb 2 S 3 hali hazırda oksitleyici maddeler ile kuvvetli bir şekilde reaksiyona sokulması, oksidize edilir. Havada mavi bir alevle yanar. Kadmiyum, magnezyum ve çinko kloratlarla akkor reaksiyona girer. Sb 2 S 3 ve kloratların karışımları patlayabilir.
Sb burada antimon cevherlerden antimon ekstraksiyonunda alkali sülfit yöntemi kullanılmakta ise 2 S 3 reaksiyona girer thioantimonate (III) tuzları (aynı zamanda thioantimonite adlandırılır) oluşturmak üzere
- 3 Na 2 S + Sb 2 S 3 → 2 Na 3 SbS 3
Farklı thioantimonate (III) iyonları içeren tuzlar sayıda Sb hazırlanabilir 2 S 3 , bu aşağıdakileri içerir:
- [SbS 3 ] 3− , [SbS 2 ] - , [Sb 2 S 5 ] 4− , [Sb 4 S 9 ] 6− , [Sb 4 S 7 ] 2− ve [Sb 8 S 17 ] 10−
" Schlippe tuzu ", Na 3 SbS 4 ·9H 2 O, Sb 2 S 3 kükürt ve sodyum hidroksit ile kaynatıldığında bir tiyoantimonat(V) tuzu oluşur . Reaksiyon şu şekilde temsil edilebilir:
- Sb 2 S 3 + 3 S 2− + 2 S → 2 [SbS 4 ] 3−
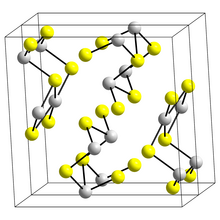
Yapı
Siyah yapısı iğne benzeri Sb şeklinde 2 S 3 , antimonit , antimon atomuna trigonal piramit ve kare piramit, iki farklı koordinasyon ortamlarında olan bağlantılı şeritleri oluşmaktadır. Bi 2 S 3 ve Sb 2 Se 3'te benzer şeritler meydana gelir . Kırmızı form, metastibnit, amorftur. Son zamanlarda yapılan çalışmalar, stibnit (I) olarak adlandırılan ve daha önce tanımlanan yüksek sıcaklık formu, stibnit (II) ve stibnit (III) olarak adlandırılan stibnitin sıcaklığa bağlı çok sayıda yapısı olduğunu göstermektedir. Diğer makale, antimonun gerçek koordinasyon polihedrasının aslında M1 bölgesinde (3+4) ve M2 bölgesinde (5+2) koordinasyonla SbS 7 olduğunu göstermektedir . Bu koordinasyonlar ikincil bağların varlığını dikkate alır. İkincil bağların bazıları kohezyon sağlar ve paketleme ile bağlantılıdır.

