Antimon triklorür - Antimony trichloride

|
|||
|
|
|||
| İsimler | |||
|---|---|---|---|
|
Tercih edilen IUPAC adı
antimon triklorür |
|||
|
Sistematik IUPAC adı
triklorostiban |
|||
| Diğer isimler
Antimon(III) klorür, Antimon yağı, Antimon klorür, Stibous klorür, Triklorostibin
|
|||
| tanımlayıcılar | |||
|
3B model ( JSmol )
|
|||
| chebi | |||
| Kimyasal Örümcek | |||
| ECHA Bilgi Kartı |
100.030.031 |
||
| AT Numarası | |||
| fıçı | |||
| ağ | Antimon+triklorür | ||
|
PubChem Müşteri Kimliği
|
|||
| RTECS numarası | |||
| ÜNİİ | |||
| BM numarası | 1733 | ||
|
CompTox Panosu ( EPA )
|
|||
|
|||
|
|||
| Özellikleri | |||
| Cı 3 Sb | |||
| Molar kütle | 228.11 g·mol -1 | ||
| Görünüm | Renksiz katı, çok higroskopik | ||
| Koku | Keskin, keskin | ||
| Yoğunluk | 3.14 g / cm ' 3 (25 ° C) 2.51 g / cm' 3 (150 ° C) |
||
| Erime noktası | 73.4 °C (164.1 °F; 346.5 K) | ||
| Kaynama noktası | 223,5 °C (434.3 °F; 496.6 K) | ||
| 601.1 g/100 ml (0 °C) 985.1 g/100 mL (25 °C) 1.357 kg/100 mL (40 °C) |
|||
| çözünürlük | Çözünür aseton , etanol , CH 2 Cı 2 , feniller , eter , dioksan , CS 2 , CCI 4 , CHC! 3 , sikloheksan , oksiklorür, selenyum (IV) 'ün içinde çözünmeyen piridin , kinolin , organik bazlar |
||
| Çözünürlük olarak asetik asit | 143.9 g/100 g (0 °C) 205,8 g/100 g (10 °C) 440,5 g/100 g (25 °C) 693,7 g/100 g (45 °C) |
||
| Çözünürlük olarak aseton | 537.6 g/100 g (18 °C) | ||
| Çözünürlük içinde benzoil klorür | 139,2 g/100 g (15 °C) 169,5 g/100 g (25 °C) 2,76 kg/100 g (70 °C) |
||
| Çözünürlük içinde hidroklorik asit | 20 °C: 8,954 g/g (%4,63 w/w) 8,576 g/g ( %14,4 w/w) 7,898 g/g (%36,7 w/w) |
||
| Çözünürlük içinde p-simen | 69,5 g/100 g (-3,5 °C) 85,5 g/100 g (10 °C) 150 g/100 g (30 °C) 2,17 kg/100 g (70 °C) |
||
| Buhar basıncı | 13,33 Pa (18,1 °C) 0,15 kPa (50 °C) 2,6 kPa (100 °C) |
||
| -86,7 · 10 -6 cm 3 / mol | |||
|
Kırılma indisi ( n D )
|
1.46 | ||
| yapı | |||
| ortorombik | |||
| 3,93 D (20 °C) | |||
| Termokimya | |||
|
Isı kapasitesi ( C )
|
183.3 J/mol·K | ||
|
Std molar
entropi ( S |
110.5 J/mol·K | ||
|
Std
oluşum entalpisi (Δ f H ⦵ 298 ) |
-381.2 kJ/mol | ||
|
Gibbs serbest enerjisi (Δ f G ˚)
|
-322,5 kJ/mol | ||
| Tehlikeler | |||
| Güvenlik Bilgi Formu | ICSC 1224 | ||
| GHS piktogramları |
 
|
||
| GHS Sinyal kelimesi | Tehlike | ||
| H314 , H411 | |||
| P273 , P280 , P305+351+338 , P310 | |||
| NFPA 704 (ateş elmas) | |||
| Alevlenme noktası | Yanıcı değil | ||
| Ölümcül doz veya konsantrasyon (LD, LC): | |||
|
LD 50 ( ortalama doz )
|
525 mg/kg (oral, sıçan) | ||
| NIOSH (ABD sağlığa maruz kalma sınırları): | |||
|
PEL (İzin Verilebilir )
|
TWA 0.5 mg / m 3 (Sb gibi) | ||
|
REL (Önerilen)
|
TWA 0.5 mg / m 3 (Sb gibi) | ||
| Bağıntılı bileşikler | |||
|
Diğer anyonlar
|
Antimon triflorür Antimon tribromür Antimon triiyodür |
||
|
Diğer katyonlar
|
Azot triklorür Fosfor triklorür Arsenik triklorür Bizmut klorür |
||
|
Aksi belirtilmediği sürece, veriler standart durumdaki malzemeler için verilmiştir (25 °C [77 °F], 100 kPa'da). |
|||
|
|
|||
| Bilgi kutusu referansları | |||
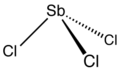
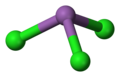
Antimon triklorür olan kimyasal bileşik ile , formül SBCL 3 . Keskin kokulu, yumuşak, renksiz bir katıdır ve simyacılar tarafından antimon yağı olarak bilinirdi .
Hazırlık
Antimon triklorür, klorun antimon , antimon tribromür , antimon trioksit veya antimon trisülfid ile reaksiyona girmesiyle hazırlanır . Ayrıca, antimon trioksitin konsantre hidroklorik asit ile işlenmesiyle de yapılabilir .
Reaksiyonlar
SBCL 3 kolayca hidrolize edilir ve SBCL örnekleri 3 nemden korunmalıdır. Sınırlı miktarda su ile hidrojen klorür salan antimon oksiklorür oluşturur :
- SbCl 3 + H 2 O → SbOCl + 2 HCl
Daha fazla su ile Sb oluşturur
4Ö
5Cl
2argon dönüştürür altında ° 460 ısıtılması ile olan Sb
8Ö
11Cl
12.
SBCL 3 , örneğin, hali hazırda halojenürler ile kompleksler oluşturur, ancak stoichiometries bileşime iyi değildir veya (Cı
5H
5NH)SbCl
4bozulmuş Sb III oktahedralı bir zincir anyonu içerir . Aynı şekilde tuz (C
4H
9NH
3)
2SbCl
5polimerik bir bileşim anyonunu içerir [SbCl2−
5]
nçarpık oktahedral ile Sb III .
Bir sterokimyasal olarak etkin yalın çifti nitrojen donor ligandları, L, kompleksleri ile örneğin Ψ-köşeli bipyramidal LSbCl için, oluşturulan 3 ve Ψ-oktahedral L
2SbCl
3.
SBCL 3 ancak bazı kompleksler, örneğin sadece bilinen bir zayıf Lewis bazıdır karbonil kompleksleri , Fe (CO)
3(SbCl
3)
2ve Ni(CO)
3SbCl
3.
yapı
Gaz fazında SBCL 3 97,2 bir Cı-SBCL açısı ° ve 233 um bir bağ uzunluğuna sahip piramit şeklindedir. SBCL olarak 3 her Sb moleküler SBCL kalıcılığı gösteren 234 pm ila üç Cı atomuna sahip 3 Ancak bir başka beş komşu Cı atomunun, iki 346 pm, 361 pm bir ve iki 374 pm de bulunmaktadır, birim. Bu sekiz atomun iki uçlu bir üçgen prizma oluşturduğu düşünülebilir. Bu mesafeler , 250 pm'de üç, 324 pm'de iki ve ortalama 336 pm'de üç yakın komşusu olan BiCl 3 ile karşılaştırılabilir . Burada dikkat edilmesi gereken nokta, Bi'nin sekiz yakın komşusunun hepsinin Sb'nin en yakın sekiz komşusundan daha yakın olması ve Bi'nin daha yüksek koordinasyon sayıları benimseme eğilimini göstermesidir.
kullanır
SBCL 3 a, reaktif tespit edilmesi için , A vitamini ve ilgili karotenoidler olarak Carr fiyat testi . Antimon triklorür karotenoid ile reaksiyona girerek kolorimetri ile ölçülebilen mavi bir kompleks oluşturur .
Antimon triklorür de olarak kullanılmıştır suş arttırmak için louche etkisi de pelin . Geçmişte buzağıların boynuzlarını kesmek zorunda kalmadan çözmek ve çıkarmak için kullanılmıştır.
Ayrıca polimerizasyon, hidrokraking ve klorlama reaksiyonları için bir katalizör olarak kullanılır; bir şekilde de mordanlama ; ve diğer antimon tuzlarının üretiminde. Çözeltisi kloral, aromatikler ve A vitamini için analitik bir reaktif olarak kullanılır . Sentetik organik dönüşümde bir Lewis asidi katalizörü olarak çok potansiyel bir kullanıma sahiptir.
Sıvı hidrojen sülfür içindeki bir antimon triklorür çözeltisi iyi bir iletkendir, ancak bunların uygulamaları hidrojen sülfürün sıvı olması için gereken çok düşük sıcaklık veya yüksek basınçla sınırlıdır.
Popüler kültürde referanslar
Popüler İngiliz programı Büyük ve Küçük Tüm Yaratıklar'ın üçüncü sezonunun 12. bölümünde ( Bilge ve Harika Her Şey kitabının altıncı bölümünden uyarlanmıştır ), nedeni daha sonra saptanan bir nonspesifik gastroenterit olayının ardından birkaç buzağı öldü . boynuz koçanlarını çözmek için kullanılan bir solüsyonda bulunan antimon triklorürün yutulması olabilir.