Antimon pentaklorür - Antimony pentachloride
|
|
|||

|
|||
| İsimler | |||
|---|---|---|---|
|
IUPAC adları
Antimon pentaklorür
Antimon(V) klorür |
|||
| Diğer isimler
Antimonik klorür
Antimon perklorür |
|||
| tanımlayıcılar | |||
|
3B model ( JSmol )
|
|||
| Kimyasal Örümcek | |||
| ECHA Bilgi Kartı |
100.028.729 |
||
| AT Numarası | |||
|
PubChem Müşteri Kimliği
|
|||
| RTECS numarası | |||
| ÜNİİ | |||
|
CompTox Panosu ( EPA )
|
|||
|
|||
|
|||
| Özellikleri | |||
| Cl 5 Sb | |||
| Molar kütle | 299.01 g·mol -1 | ||
| Görünüm | renksiz veya kırmızımsı sarı (dumanlı) sıvı, yağlı | ||
| Koku | keskin, saldırgan | ||
| Yoğunluk | 2.336 g / cc 3 (20 ° C) 2.36 g / cm ' 3 (25 ° C) |
||
| Erime noktası | 2,8 °C (37.0 °F; 275,9 K) | ||
| Kaynama noktası | 140 °C (284 °F; 413 K) 106 °C'den 79 °C'den (174 °F; 352 K) 22 mmHg'de 92 °C'de (198 °F; 365 K) 30 mmHg'de |
||
| tepki verir | |||
| çözünürlük | alkol , HCl , tartarik asit , CHCl 3 , CS 2 , CCl 4 içinde çözünür | ||
| Çözünürlük olarak selenyum (IV) 'oksiklorür | 62,97 gr/100 gr (25 °C) | ||
| Buhar basıncı | 0,16 kPa (25 °C) 4 kPa (40 °C) 7,7 kPa (100 °C) |
||
| -120,0 · 10 -6 cm 3 / mol | |||
|
Kırılma indisi ( n D )
|
1.59255 | ||
| viskozite | 2.034 cP (29.4 °C) 1.91 cP (35 °C) |
||
| yapı | |||
| trigonal bipiramidal | |||
| 0 D | |||
| Termokimya | |||
|
Isı kapasitesi ( C )
|
120,9 J/mol·K (gaz) | ||
|
Std molar
entropi ( S |
295 J/mol·K | ||
|
Std
oluşum entalpisi (Δ f H ⦵ 298 ) |
-437.2 kJ/mol | ||
|
Gibbs serbest enerjisi (Δ f G ˚)
|
-345,35 kJ/mol | ||
| Tehlikeler | |||
| GHS piktogramları |
 
|
||
| GHS Sinyal kelimesi | Tehlike | ||
| H314 , H411 | |||
| P273 , P280 , P305+351+338 , P310 | |||
| soluma tehlikesi | Toksik | ||
| NFPA 704 (ateş elmas) | |||
| Alevlenme noktası | 77 °C (171 °F; 350 K) | ||
| Ölümcül doz veya konsantrasyon (LD, LC): | |||
|
LD 50 ( ortalama doz )
|
1115 mg/kg, (sıçan, oral) | ||
| NIOSH (ABD sağlığa maruz kalma sınırları): | |||
|
PEL (İzin Verilebilir )
|
TWA 0.5 mg / m 3 (Sb gibi) | ||
|
REL (Önerilen)
|
TWA 0.5 mg / m 3 (Sb gibi) | ||
| Bağıntılı bileşikler | |||
|
Diğer anyonlar
|
antimon pentaflorür | ||
|
Diğer katyonlar
|
fosfor pentaklorür | ||
|
Bağıntılı bileşikler
|
antimon triklorür | ||
|
Aksi belirtilmediği sürece, veriler standart durumdaki malzemeler için verilmiştir (25 °C [77 °F], 100 kPa'da). |
|||
|
|
|||
| Bilgi kutusu referansları | |||
Antimon pentaklorür , SbCl 5 formülüne sahip kimyasal bir bileşiktir . Renksiz bir yağdır, ancak tipik örnekler safsızlıklar nedeniyle sarımsıdır. Eğiliminden dolayı hidroliz eden için hidroklorik asit , SBCL 5 oldukça aşındırıcı madde ve cam veya saklanmalıdır PTFE kaplar.
Hazırlık ve yapı
Antimon pentaklorür, klor gazının erimiş antimon triklorür içine geçirilmesiyle hazırlanır :
- SbCl 3 + Cl 2 → SbCl 5
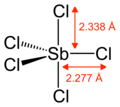
Gaz halindeki SbCl 5 , trigonal bipiramidal bir yapıya sahiptir.
Reaksiyonlar
Antimon pentaklorür hidroklorik asit ve antimon oksiklorürler vermek üzere hidrolize olur . Bu reaksiyon, heksakloroantimonat kompleks iyonunun oluşumu nedeniyle, büyük miktarda klorür varlığında bastırılır :
- SbCl 5 + Cl − → [SbCl 6 ] −
Mono- ve tetrahidratlar bilinmektedir, SbCl 5 ·H 2 O ve SbCl 5 ·4H 2 O.
Bu bileşik, birçok Lewis bazıyla adüktler oluşturur. SBCL 5 a, yumuşak Lewis asidi ve ECW modeli parametreleri D olan bir = 3.64 ve C A = 10.42. Lewis bazlığının Gutmann ölçeğinde standart Lewis asidi olarak kullanılır .
Aynı zamanda güçlü bir oksitleyici ajandır . Örneğin aromatik eterler, aşağıdaki stokiyometriye göre radikal katyonlarına oksitlenir:
- 3 SbCl 5 + 2 ArH → 2 (ArH+)(SbCl 6 - ) + SbCl 3
Uygulamalar
Antimon pentaklorür, polimerizasyon katalizörü olarak ve organik bileşiklerin klorlanması için kullanılır .
Önlemler
Antimon pentaklorür, ısıdan ve nemden uzakta saklanması gereken oldukça aşındırıcı bir maddedir. Klorlama maddesidir ve nem varlığında hidrojen klorür gazı açığa çıkarır. Bu nedenle, nemli bir ortamda tutulursa paslanmaz çelik aletleri (iğneler gibi) bile aşındırabilir. Plastik malzemeleri eritip karbonize ettiğinden, flor içermeyen plastiklerle (plastik şırıngalar, plastik septalar veya plastik bağlantılı iğneler gibi) kullanılmamalıdır.